
题目列表(包括答案和解析)
33. (2005年全国理综Ⅰ29)已知某纯碱试样中含
(2005年全国理综Ⅰ29)已知某纯碱试样中含
有NaCl杂质,为测定试样中纯碱的质量分数,
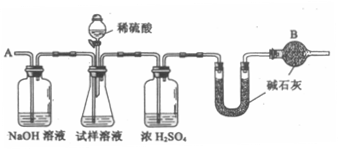
可用下图中的装置进行实验。
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将a g试样放人锥形瓶中,加适量蒸馏水
溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量得到b g
④从分液漏斗滴人6mol·L-1 的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓人一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到c g
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为d g
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明
(2)装置中干燥管B的作用是
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果 (填偏高、偏低或不变)
(4)步骤⑤的目的是 ,(5)步骤⑦的目的是 。
(6)该试样中纯碱的质量分数的计算式为 。
(7)还可以用其他实验方法测定试样中纯碱的质量分数。请简述一种不同的实验方法。
[答案](1)样品重,砝码轻 (2)防止空气中的CO2和水气进入U型管中
(3)偏高 (4)把反应产生的CO2全部导入U型管中
(5)判断反应产生的CO2是否全部排出,并被U型管中的碱石灰吸收
(6)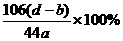 (7)答案略。
(7)答案略。
[以下答案仅供(7)参考:① 酸碱中和滴定法② 重量法 a.Ba2+法、b.Ca2+法、c.Ag+法 、d.HCl法
说明:① 滴定法,简述必须指明正确的指示剂或标准溶液
② 重量法,简述中必须指明所加入的试剂及结果处理方法。]
32.(2004年江苏卷 20)有两个实验小组的同学为
探究过氧化钠与二氧化硫的反应,都用如下图所
示的装置进行实验。通入SO2气体,将带余烬的
木条插入试管C中,木条复燃。
请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成了
Na2SO3和O2,该反应的化学方程式是:
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3。
。
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:
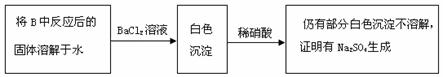
上述方案是否合理? 。请简要说明两点理由:
① ;② 。
[答案] (1)2Na2O2+2SO2=2Na2SO3+O2 (2)取白色固体,加稀硫酸,产生能使品红溶液褪色的气体。
(3)不合理 ; 稀硝酸能将亚硫酸钡氧化为硫酸钡;
如果反应后的固体中还残留Na2O2,它溶于水后能将亚硫酸根氧化成硫酸根
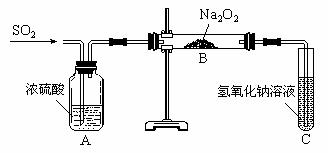
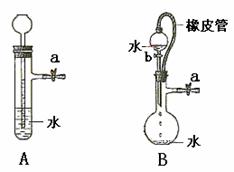
31.(204年全国理综28)根据下图及描述,回答下列问题:
(1)关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入
一定量的水,静置后如图所示。试判断:A装置是否漏气?
(填“漏气”、“不漏气”或“无法确定”) ,
判断理由:
。
(2)关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) ,
判断理由:
。
[答案] (1)不漏气;由于不漏气,加水后试管内气体体积减小,导致压强增大,长颈漏斗内的水面高出试管内的水面。
 (2)无法确定;由于分液漏斗和烧瓶间有橡皮管相连,使分液漏斗中液面上方和烧瓶中液面上方的压强相同,无论装置是否漏气,都不影响分液漏斗中的液体滴入烧瓶。
(2)无法确定;由于分液漏斗和烧瓶间有橡皮管相连,使分液漏斗中液面上方和烧瓶中液面上方的压强相同,无论装置是否漏气,都不影响分液漏斗中的液体滴入烧瓶。
30.(2003年广东卷19)(1)无水乙酸又称冰醋酸(熔点16.6℃)。在室温较低时,无水乙酸就会凝结成像冰一样的晶体。请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸。
答:
(2)要配制浓度约为2mol·L-1 NaOH溶液100mL,下面的操作正确的是 (填代号)。
A. 称取8g NaOH固体,放入250mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解
B. 称取8g NaOH固体,放入100mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL
C. 称取8g NaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀
 D. 用100mL量筒量取40mL 5mol·L-1NaOH溶液,倒入250mL烧杯中,再用同一量筒取60mL蒸馏水,不断搅拌下,慢慢倒入烧杯中
D. 用100mL量筒量取40mL 5mol·L-1NaOH溶液,倒入250mL烧杯中,再用同一量筒取60mL蒸馏水,不断搅拌下,慢慢倒入烧杯中
[答案](1)略 (2)A、D
9.(2004年广东卷21)A、B、C、D是四种可溶的化合物,分别由
阳离子K+、Ba2+、Al3+、Fe3+和阴离子OHˉ、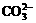 、
、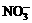 、
、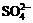
两两组合而成,它们的溶液发生如下反应:
A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会完
全消失。C与D反应生成有色沉淀。B与C反应生成白色沉淀。
写出它们的化学式:A: B: C: D:
[答案] Ba(OH)2;Al2(SO4)3;K2CO3;Fe(NO3)3
28.(2004年全国理综Ⅰ28)有A、B、C、D、E、F、G 7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba (OH )2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显变化。
试回答下面问题。
⑴A的化学式是 ,G的化学式是 。
判断理由是 。 ⑵写出其余几种物质的化学式。
|
|
A |
B |
C |
D |
E |
F |
G |
|
A |
- |
- |
- |
- |
- |
- |
↓ |
|
B |
- |
- |
- |
- |
↓ |
↓ |
↓ |
|
C |
- |
- |
― |
↓ |
|
↓ |
↓ |
|
D |
- |
- |
↓ |
- |
↓ |
↓ |
↓ |
|
E |
- |
↓ |
- |
↓ |
- |
↓ |
- |
|
F |
- |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
|
G |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
- |
B: ,C: ,D: ,
E: ,F: 。
[答案]
⑴ KCl;AgNO3;混合时只生成一种沉淀的是KCl,
生成的是AgCl,所以A是KCl,G是AgNO3。 ⑵ B:Na2SO4 C:MgCl2 D:Na2CO3 E:Ca(NO3)2 F:Ba(OH)2
27.(2005年全国理综 Ⅱ29)某有机化合物A的相对分子质量(分子量)大于110,小于150。经分析得知,其中碳和氢的质量分数之和为52.24%,其余为氧。请回答:
⑴该化合物分子中含有几个氧原子,为什么?
⑵该化合物的相对分子质量(分子量)是 。
⑶该化合物的化学式(分子式)是 。
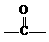
⑷该化合物分子中最多含 个 官能团。
[答案]⑴答案要点:4个氧原子。因为:110<A的相对分子质量<150
氧在分子中的质量分数为1-52.24%=47.76%所以 52.5<分子中氧原子的相对原子质量之和<71.6
又因为只有4个氧原子的相对原子质量之和(64)符合上述不等式,所以化合物A中含4个氧原子。(5分) ⑵134(4分) ⑶C5H10O4(4分) ⑷1(3分)
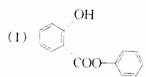
26.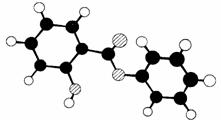 (06年全国理综Ⅰ)萨罗(Salol)是一种消毒剂,它的分子式
(06年全国理综Ⅰ)萨罗(Salol)是一种消毒剂,它的分子式
为C13H10O3,其分子模型如下图所示(图中球与球之间的连线代表化
学键,如单键、双键等):
(1)根据右图模型写出萨罗的结构简式:_______________;
(2)萨罗经水解、分离、提纯可得到纯净的苯酚和水杨酸
(邻羟基苯甲酸)。请设计一个方案,说明苯酚、碳酸、水杨酸的
酸性依次增强(用化学方程式表示)。
(3)同时符合下列四个要求的水杨酸的同分异构体共有______________种。
① 含有苯环 ② 能发生银镜反应,不能发生水解反应;
③ 在稀NaOH溶液中,1mol该同分异构体能与2mol NaOH发生反应;④ 只能生成两种一氯代物。
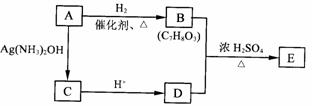 (4)从(3)确定的同分异构体中任选一种,
(4)从(3)确定的同分异构体中任选一种,
指定为下列框图中的A。
写出下列两个反应的化学方程式(有机物用
结构简式表示),并指出相应的反应类型:
① A → B: _______ __________;
反应类型:_____________ 。
② B + D →E:__________________________;
反应类型:_____________。
(5) 现有水杨酸和苯酚的混合物,它们的物质的量之和为n mol。该混合物完全燃烧消耗a L O2,并生成b g H2O和c L CO2(气体体积均为标准状况下的体积)。
① 分别写出水杨酸和苯酚完全燃烧的化学方程式(有机物可用分子式表示)。
② 设混合物中水杨酸的物质的量为x mol,列出x的计算式。
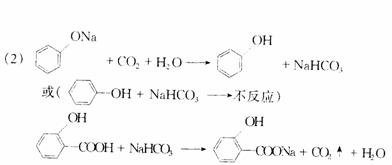 [答案]
[答案]
(3) 2

25.(2005年全国卷I 29)苏丹红一号(sudan Ⅰ)是一种偶氮染料,不能作为食品添加剂使用。它是由苯胺和2-萘酚为主要原料制备的,它们的结构简式如下所示:
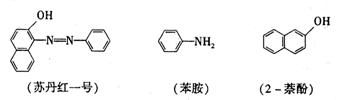
(1)苏丹红一号的化学式(分子式)为
(2)在下面化合物(A)-(D)中,与2-萘酚互为同分异构体的有(填字母代号)
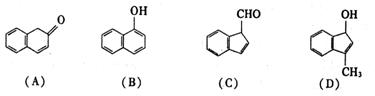
(3)上述化合物(C)含有的官能团是
(4)在适当的条件下,2-萘酚经反应可得到芳香化合物E(C8H6O4),1 mol E与适量的碳酸氢钠溶液反应可放出二氧化碳44.8L(标准状况),E与溴在有催化剂存在时反应只能生成两种一溴取代物,两种一溴取代物的结构简式分别是 ,E与碳酸氢钠反应的化学方程式是 。
(5)若将E与足量乙醇在浓硫酸作用下加热,可以生成一个化学式(分子式)为C12H14O4的新化合物,该反应的化学方程式是 反应类型是 酯化反应。
[答案](1)C16H12N2O(2)A B C(3)碳碳双键 醛基


(4)

(5)

(6)
24.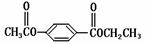 (2004年全国卷Ⅲ 27)芳香化合物A、B互为同分异构体,B的结构简式是:
(2004年全国卷Ⅲ 27)芳香化合物A、B互为同分异构体,B的结构简式是:
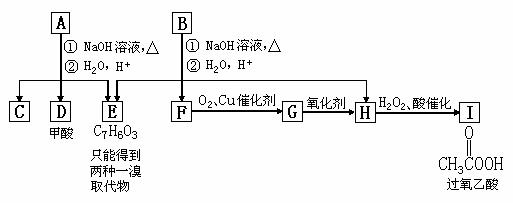
 A经①、②两步反应得C、D和E。B经①、②两步反应得E、F和H。上述反应
A经①、②两步反应得C、D和E。B经①、②两步反应得E、F和H。上述反应
过程、产物性质及相互关系如图所示。
(1)写出E的结构简式 。
(2)A有2种可能的结构,写出相应的结构简式 。
(3)F和小粒金属钠反应的化学方程式是 ,
 实验现象是 ,反应类型是
。
实验现象是 ,反应类型是
。
(4)写出F在浓H2SO4作用下在170℃发生反应的化学方程式:
,实验现象是 ,反应类型是 。
(5)写出F与H在加热和浓H2SO4催化作用下发生反应的化学方程式
,实验现象是 ,反应类型是 。
(6)在B、C、D、F、G、I化合物中,互为同系物的是 。
[答案]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com