
题目列表(包括答案和解析)
7. 某天然有机化合物,其结构如右图所示,关于该化合物的说法不正确的是 [原创] ( )
某天然有机化合物,其结构如右图所示,关于该化合物的说法不正确的是 [原创] ( )
A.该化合物无法发生消去反应
B.该化合物的分子式是C17H13O5
C.一定条件下,1mol该化合物最多可以和8molH2发生加成反应
D.一定条件下,该化合物可以发生银镜反应
第Ⅱ卷(非选择题 共58分)
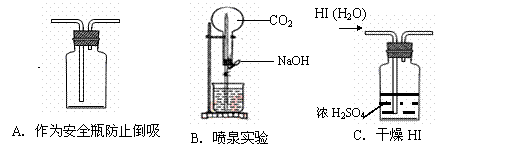
6.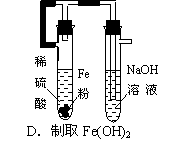 下列装置的设计能达到实验目的的是[根据09届高考化学易错题解题方法实验题大全改编]( )
下列装置的设计能达到实验目的的是[根据09届高考化学易错题解题方法实验题大全改编]( )
5、常温下,下列各溶液的叙述不正确的是[原创]( )
A.pH=7的醋酸钠和醋酸混合溶液中,c(Na+)=c(CH3COO-)
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1>10c2
C.pH=3的醋酸溶液和pH=11的氢氧化钠溶液等体积混合,混合后溶液显酸性
D.已知酸性HF> CH3COOH,则等体积等物质的量浓度的NaF和CH3COONa溶液所含的阴离子数后者较多
4、下列离子方程式正确的是[原创] ( )
A.KI溶液中滴加双氧水: 2I-+H2O2=I2 + 2H++ O2↑
B.用银氨溶液检验乙醛中的醛基:CH3CHO+2[Ag(NH3)2]++2OH-CH3COO-+NH4++3NH3+2Ag↓+H2O
C.向次氯酸钙溶液通入二氧化硫:Ca2++2ClO-+SO2+H2O ==2HClO+CaSO3
D.Fe(NO3)3溶液中加入过量HI溶液:2Fe3++2I-=2Fe2++I2
3、设阿伏加德罗常数为NA,则下列说法正确的是[原创]( )
A.标准状况下,2.24L乙醇中所含的氧原子数为0.1 NA
B.1molNaCl晶体中含有1.0 NA个NaCl分子
C.电解硫酸溶液时,4molOH-离子放电的同时有2.0NA个电子发生转移
D.常温下,浓度为1mol/L的Na2CO3溶液中含有2.0NA个Na+
2、下列化学用语表达正确的是[原创]( )
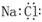 A.氯化钠的电子式 :
A.氯化钠的电子式 :

B.丙烷分子的比例模型:
C.NaHCO3的电离方程式NaHCO3=Na++H++CO32-
D.Na2O2中即含离子键又含共价键
1、化学与生活是紧密相联的,下列说法正确的是[原创]( )
A.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰
B.海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化
C.生铁在潮湿的空气中易生锈,其负极反应式为2H2O + O2 + 4e- = 4OH-
D.现用清洁燃料主要有压缩天然气和液化石油气两类,他们均属于碳氢化合物
11、(15分)(改编:2010·北京崇文模拟)
某种芳香族化合物A,其分子量为164.A由碳、氢、氧三种元素组成,经测定碳、氢的质量分数分别为73.2%和7.32%.
(1)A的分子式是________
 (2)已知:
(2)已知:

Ⅰ. + (R1、R2、R3代
表氢原子或烃基)
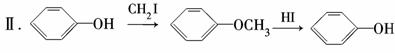
又知,A在一定条件下能发生如下转化,某些生成物(如H2O等)已略去.

请回答下列问题:
①步骤Ⅰ的目的是________;
②若G的相对分子质量是44,则E的结构简式是____________;E的核磁共振氢谱中有__________(填数字)个吸收峰;
③F→H的反应类型是________;
④F在一定条件下可发生酯化反应,生成M(M与FeCl3溶液反应,溶液呈紫色;且分子结构中含有苯环和一个七元环),请写出该反应的化学方程式_____________________;
⑤A的结构简式是________;上述转化中B→D的化学方程式是_________________.
(3)已知A的某种同分异构体N具有如下性质:
①N与FeCl3溶液反应,溶液呈紫色
②N在一定条件下可发生银镜反应,N与H2在苯环侧链上按照物质的量之比1∶1作用后的生成物不能发生消去反应
③在通常情况下,1 mol N能与含1 mol Br2的浓溴水发生取代反应
④N分子中苯环上的取代基上无支链
请写出满足以上条件的N的结构简式__________________________________________
10、(14分)(2010·山东高考)
聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m,广泛用于污水处理.实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:

(1)验证固体W焙烧后产生的气体含有SO2的方法是____________________.
(2)实验室制备、收集干燥的SO2,所需仪器如下.装置A产生SO2,按气流方向连接各仪器接口,顺序为a→________→________→________→________→f.装置D的作用是________,装置E中NaOH溶液的作用是________.

(3)制备绿矾时,向溶液X中加入过量________,充分反应后,经________操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾.
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为_______________________.若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏_______.
9、(15分)(2010·浙江温州)
甲醇被称为21世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇.
(1)将1.0 mol CH4和2.0 mol H2O(g)通入反应室(容积为100 L),在一定条件下发生反应:
CH4(g)+H2O(g)  CO(g)+3H2(g) Ⅰ
CO(g)+3H2(g) Ⅰ
CH4的转化率与温度、压强的关系如下图.

①已知100℃时达到平衡所需的时间为5 min,则用H2表示的平均反应速率为________.
②图中的p1________p2(填“<”、“>”或“=”),100℃时平衡常数为_________.
③在其他条件不变的情况下降低温度,逆反应速率将________(填“增大”、“减小”或“不变”).
(2)在压强为0.1 MPa条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:
CO(g)+2H2(g)  CH3OH(g) Ⅱ
CH3OH(g) Ⅱ
①该反应的ΔH________0,ΔS________0(填“<”、“>”或“=”).
②若容器容积不变,下列措施可增加甲醇产率的是________.
A、升高温度 B、将CH3OH(g)从体系中分离
C、充入He,使体系总压强增大 D、再充入1 mol CO和3 mol H2
③为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.

|
实验编号 |
T/℃ |
n(CO)/n(H2) |
p/MPa |
|
ⅰ |
150 |
1/3 |
0.1 |
|
ⅱ |
________ |
________ |
5 |
|
ⅲ |
350 |
________ |
5 |
A、请在上表空格中填入剩余的实验数据.
B、根据反应Ⅱ的特点,在给出的坐标图中,画出其在0.1 MPa和5 MPa条件下CO的转化率随温度变化的曲线示意图,并标明各条曲线的压强.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com