
题目列表(包括答案和解析)
11.(根据2011年富阳中学高考预测卷第17题改编)某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置先进行了有关实验:

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整。
(2)实验中他们取6.4g 铜片和12mL 18mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①写出铜跟浓硫酸反应的化学方程式:____________________________________;
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是____________________;
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是:________(填写编号)。
A.铁粉 B.氯化钡溶液 C.银粉 D.碳酸氢钠溶液
(3)为定量测定余酸的物质的量浓度,甲学生进行了如下设计学生设计的方案是:在反应后的溶液中加蒸馏水稀释至1000mL,取20mL与锥形瓶中,滴入2~3滴甲基橙指示剂,用标准氢氧化钠溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),通过测出消耗氢氧化钠溶液的体积来求余酸的物质的量浓度。假定反应前后烧瓶中溶液的体积不变,你认为他设计的实验方案能否求得余酸的物质的量浓度_______(填“能”或“不能”),其理由是_________________________________________________。ww.k@s@5@ 高#考#资#源#网
(4)现已确认,SO2和NOx的排放是造成酸沉降的两大罪魁祸首。汽车排放的尾气中含有未燃烧充分的CH、以及N2、CO2、NO、CO等。有人设计利用反应2NO + 2CO  N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
|
时间/h |
0 |
1 |
2 |
3 |
4 |
5 |
|
c(NO)/mol·L-1 |
1.00×10-3 |
4.5×10-4 |
2.5×10-4 |
1.5×10-4 |
1.00×10-4 |
1.00×10-4 |
|
c(CO)/mol·L-1 |
3.6×10-3 |
3.05×10-3 |
2.85×10-3 |
2.75×10-3 |
2.70×10-3 |
2.70×10-3 |
在上述条件下反应能够自发进行,则反应的 ______
0(“>”、“<”、“=”)。前2h内的平均反应速率v(N2)=
_____________,在该温度下,反应的平衡常数K= ____________ 。据此你认为将该反应从理论转化为现实的最重要的研究方向是___________________
______
0(“>”、“<”、“=”)。前2h内的平均反应速率v(N2)=
_____________,在该温度下,反应的平衡常数K= ____________ 。据此你认为将该反应从理论转化为现实的最重要的研究方向是___________________
10.已知:HCN的结构为H-C≡N;
 ①R-CN
RCOOH,
①R-CN
RCOOH,
 ②R-Cl+CN-
R-CN+Cl-(R为烃基)。
②R-Cl+CN-
R-CN+Cl-(R为烃基)。
 玉米芯、甘蔗渣等废物水解发酵后可制得糠醛
,它是重要的化工原料,它在一定条件下可发生以下变化:
玉米芯、甘蔗渣等废物水解发酵后可制得糠醛
,它是重要的化工原料,它在一定条件下可发生以下变化:


(1)写出反应类型:② ,④ 。
(2)写出反应③的化学方程式: ;
写出能证明糠醛中含有醛基的一个化学反应方程式及现象
现象为: 。
(3)若E为环状化合物,则其结构简式 。
(4)若E为高聚物,则其结构简式 。
9.(根据实验化学练习改编)牙膏是生活必需品,牙膏中某些主要成分的检验流程图如下

请回答下列问题:
(1)在①中加水、搅拌、静置后,接下来的实验操作名称是______________,所需要的主要玻璃仪器有 ______________
(2)在②中用pH试纸测溶液的pH的操作方法是 ____________________________。
(3)写出④中发生反应的化学方程式: __________________________________________
现象为:________________________________________________________
(4)在⑥中除了利用焰色反应外,还可用___________________检验Ca2+的存在
(5)在③中如果存在F-则加了氯化钙溶液后现象为__________________
8.(根据2011年金陵中学高考模拟第16题改编)下图中的反应①是重要的电化学工业反应,反应②可用于制备新型消毒净水剂Na2FeO4。常温下B、C为气态单质,G是当代社会使用量最大的金属,其余均为化合物。(反应时加入或生成的水,以及生成沉淀I时的其他产物均已略去) 。
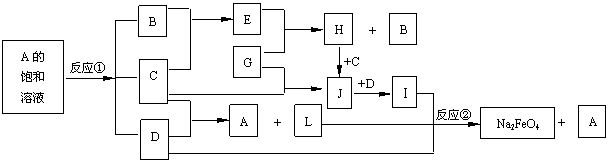
请回答下列问题:
(1)E的电子式为_______________。
(2)J溶液蒸干灼烧得到的物质是(填化学式) _______________。
(3)反应①的化学方程式是____________________________________。
(4)反应②的离子方程式是____________________________________。
(5)高铁酸钠(Na2FeO4)是一种新型、高效、无二次污染的绿色水处理剂。工业上干法制备高铁酸钠的主要反应方程式为: FeSO4+ Na2O2 → Na2FeO4+ Na2O+ Na2SO4 + O2↑(未配平)
下列有关说法不正确的是 ( )
A.高铁酸钠中铁显+6价
B.干法中每生成1 mol Na2FeO4转移4 mol电子
C.Na2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等
D.Na2FeO4处理水时还能吸附水中的悬浮杂质,所以自来水厂用高铁酸钠处理水后无需再用活性炭处理了ww.k@s@5@ 高#考#资#源#网
7.(原创) 设NA为阿伏加德罗常数,下列有关说法正确的是
A.10g质量分数为46%的乙醇溶液中,氢原子的总数为1.2NA ww.k@s@5@ 高#考#资#源#网
B.1molC10H22分子中含有的共价键数目为32NA
C.在含有NA个醋酸根离子(CH3COO-)的醋酸溶液中氢离子数目为NA
D. 标准状况下,22.4LCH4和CH3OH的混合物中含有NA个碳原子
6. (根据《苏州市2011届高三调研测试》第12题改编) 镍氢碱性电池的总反应式是MH + NiO(OH)
(根据《苏州市2011届高三调研测试》第12题改编) 镍氢碱性电池的总反应式是MH + NiO(OH) NiO + M + H2O(MH表示合金M贮存氢后的简式)。根据此反应式判断,下列叙述正确的是
NiO + M + H2O(MH表示合金M贮存氢后的简式)。根据此反应式判断,下列叙述正确的是
A.电池放电时,电池负极周围溶液的OH-不断增大
B.电池放电时,镍元素被氧化
C.电池放电时,每转移1mol电子,负极有1mol NiO(OH)被还原
D.电池充电时,阳极反应为 NiO - e- + OH- = NiO(OH )
5.(改编)新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式为:

下列说法正确的是
A.上述反应为取代反应 B.滴定时可用淀粉溶液作指示剂
C.滴定时应剧烈振荡锥形瓶 D.脱氢维生素C的分子式为C6H5O6
4.(原创)下列有关实验的叙述中,正确的有
A.可用分液漏斗分离苯和溴苯的混合物
B.给铁钉镀铜可采用CuSO4作电镀液
C.用10mL量筒量取8.58mL蒸馏水
D.如右图用铜片和稀硝酸制NO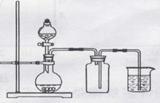
3.(原创)下列离子方程式中,正确的是
A.NaAlO2溶液中通入少量二氧化碳:AlO2- + CO2 + 2H2O = Al(OH) 3↓+ HCO3-
B.高锰酸钾酸性溶液与草酸溶液反应:
2MnO4-+ 5C2O42- + 16H+ = 2Mn2+ + 10CO2↑+ 8H2O ww.k@s@5@ 高#考#资#源#网
C.粗硅的制取:SiO2 + C Si + CO2
Si + CO2
D.同位素示踪法可用于反应机理的研究:
2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑ + 8H2O
2.(原创)下列有关化学用语正确的是
A.硫能形成分子晶体
B. 次氯酸钠的电子式是
 C.NH3分子比例模型:
D.二氧化硅的分子式
C.NH3分子比例模型:
D.二氧化硅的分子式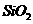
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com