
题目列表(包括答案和解析)
8.下图是某些实验的部分装置,其中所注明的实验能达到实验目的的是( )

A.②③④ B.①③ C.②③ D.②④

|
 4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是( )
4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是( )
A.若保持压强一定,当温度升高后,则图中θ>45°
B.若再加入B,则再次达到平衡时正、逆反应速率均逐渐增大
|
|
7.下列说法存在科学性错误的是( )
A.日本福岛核电站爆炸时释放的2种放射性同位素131I与137Cs的中子数相等
B.锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去
C.用丁达尔现象可以区分食盐水和淀粉溶液
D.Mg(OH)2和Al(OH)3热分解生成的气态水可覆盖火焰、驱逐O2、稀释可燃气体,分解产物MgO和Al2O3能较快地与塑料燃烧过程中产生的酸性及腐蚀性气体反应,所以它们可以作为未来发展方向的无机阻燃剂
30. (15分)X、Y都是芳香族化合物,均为常见食用香精,广泛用于化妆品、糖果及调味品中。1 mol X水解得到1 mol Y和1 mol CH3CH2OH, X、Y的相对分子质量都不超过200,完全燃烧都只生成C02和H20。且X分子中碳和氢元素总的质量百分含量约为 81.8%。
(1)X、Y相对分子质量之差为_____________________。
⑵1个Y分子中应该有_____________个氧原子。
⑶X的分子式是___________________________________
⑷G和X互为同分异构体,且具有相同的官能团,用芳香烃A合成G路线如下:
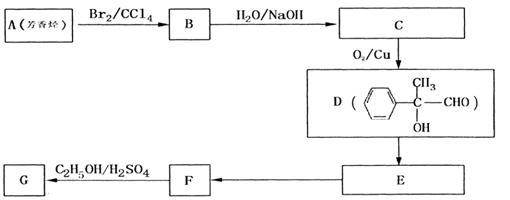
①写出A的结构简 式_____________________
② 的反应类型是______________反应,该反应的化学方程式为:______________________。
的反应类型是______________反应,该反应的化学方程式为:______________________。
③写出所有符合下列条件的F的同分异构体的结构简式:______________。
i .分子内除了苯环无其他环状结构,且苯环上有2个对位取代基。
ii. 一定条件下该物质既能与银氨溶液发生银镜反应又能和FeCl3溶液发生显色反应。
29. (15分)由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)。
(15分)由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)。
⑴若A是常温下的气态单质,X是 ,则D与A的水溶液反应的化学方程式____________
,则D与A的水溶液反应的化学方程式____________
⑵若E为难溶于水的白色沉淀、B与X的反应是中学化学中重要的化工反应;写出D与水反应所得的稀溶液与铜片反应的离子方程式________________________。
⑶若D为白色沉淀,且与A的摩尔质量相等,
(a) A的电子 式__________________。写出X与C反应生成D的离子方程式________________________
(b)将NaHCO3分解产生的气体用足量的A充分吸收得到固体混合物甲、将甲溶于V ml C mol• L-1的盐酸中,产生无色混合气体乙,溶液呈中性,则A的物质的量为_______mol,混合气体乙的物质的量为_______mol
28. (15分)W、X、Y、Z是原子序数依次增大的同一短同期元素,W、X是金属元素,Y、Z是非金属元素。回答下列问题:
⑴W、X对应的两种最高价氧化物的水化物可以反应生盐和水,该反应的离子方程式为____________________________________
(2)X的硝酸盐水溶液显____________性,用离子方程式解释原因________________________。
⑶Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为________________________
(4) W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是:____________ >____________>____________>____________。(填写离子符号)
(5) Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式:__________________。
27.
(15分)某研究性学习小组查阅资料:“氯气与硫在加热条件下生成二氯化二硫 ,该物质遇水迅速反应”。他们利用如下仪器和药品制取纯净的氯气与硫反应来制备
,该物质遇水迅速反应”。他们利用如下仪器和药品制取纯净的氯气与硫反应来制备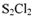
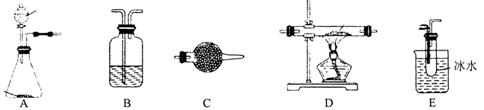
实验过程所提供的药品有:浓盐酸、浓H2S04、MnO2, KMn04(H+)、饱和NaHCO3溶液、碱石灰、硫磺、NaOH溶液、冰水、饱和食盐水。 回答下列问题:
⑴利用所提供的设备和药品,写出制备Cl2的离子方程式:_________ _____________________
_____________________
⑵在该实验过程中两次用到仪器B,第一次装置B 中的药品是__________________,第二次装置B的作用是__________________
中的药品是__________________,第二次装置B的作用是__________________
⑶能否省略装置C____________ (填“能”或“否”),原因是________________________
⑷实验幵始后,当______________________________,(填现象)点燃D处的酒精灯。
(5)某学生利用装置A制备一定量的Cl2,他收集到的Cl2的体积总比预期的要多,他经过认真分析后,认为应对装置A略作改进,你认为应怎样改进:__________________________________________
13.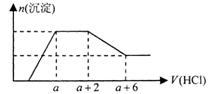 某溶液中可能含有
某溶液中可能含有 等离子。当向该溶液中加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如下图所示,下列说法正确的是
等离子。当向该溶液中加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如下图所示,下列说法正确的是
A. 原溶液中一定含有的阴离子是

B. 反应最后形成的溶液中的溶质为NaCl
C. 原溶液中一定含有Na2SO4
D. 原溶液中含有 与
与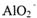 的物质的量之比为1 :1
的物质的量之比为1 :1
第II卷(非选择题共174分)
12. 2010年10月30日曲美减肥胶囊全国下架主要成分在欧美被禁。其主要成分盐酸西布曲明结构如右图所示,有关说法错误的是
A. 分子式:
 B. 水解产物之一可用FeCl3溶液检验
B. 水解产物之一可用FeCl3溶液检验
C. 该物质共平面的原子不少于12个原子
D. 属于芳香烃类,可与3mWH2加成,不溶于水
11.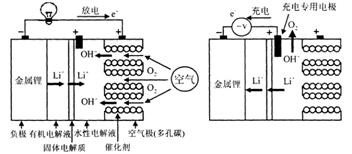 2009年2月,日本产业技术综合研究所能源技术研究部门能源界面技术研究小组组长周豪慎和日本学术振兴会(JSPS)外籍特别研究员王永刚共同幵发出了新构造的大容量锂空气电池。下列说法不正确的是
2009年2月,日本产业技术综合研究所能源技术研究部门能源界面技术研究小组组长周豪慎和日本学术振兴会(JSPS)外籍特别研究员王永刚共同幵发出了新构造的大容量锂空气电池。下列说法不正确的是
A. 放电时的正极反应为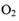

B. 充电时正极附近pH降低
C. 若用该电池作电源电解硫酸镁溶液,当电路中有0.02转移时,阴极增重0.24g
D. 在该电池中,放电反应生成的不是固体的Li2O,而是容易溶解在水性电解液中的LiOH (氢氧化锂)。因此,氧化锂在空气电极堆积后,不会导致工作停止
10. 在容积不变的密闭容器中存在如下反应: 某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
 A.图I表示的是t1时刻增大反应物的浓度对反应速率的影响
A.图I表示的是t1时刻增大反应物的浓度对反应速率的影响
B. 图II表示的一定是^时刻加入催化剂后对反应速率的影响
C. 图III表示的是温度对化学平衡的影响,且乙的温度较高
D. 图III表示的是催化剂对平衡的影响,且甲的催化效率比乙高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com