
题目列表(包括答案和解析)
3.2011年3月9日,美国“发现”号航天飞机结束它的最后一次飞行使命,于佛罗里达肯尼迪航天中心着陆,未来的航天科技又将翻开新的篇章,胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统。实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列说法或热化学方程式书写正确的是( )
A.胶状液氢的标准燃烧热比甲烷要高
B.CH4(g)+2O2(g) ====CO2(g)+2H2O(l);ΔH=-890.3 kJ·mol-1
C.一般H2加压后以液态形式保存,且液氢燃烧效果比氢气要好,释放热量更多
D.2H2(g)+O2(g) ====2H2O(l);ΔH=-285.8 kJ
[解析]此题为改编题。考察化学反应热方程的应用
2.化学是建立在实验基础上的学科。关于下列各实验装置的叙述中,不正确的是 ( )

A.装置①可用于实验室制取少量NH3或O2
B.可用从a处加水的方法检验装置②的气密性
C.实验室可用装置③收集H2、NH3
D.利用装置④制硫酸和氢氧化钠,其中b为阳离子交换膜、c为阴离子交换膜
[解析]此题为原创题。对新教材《实验化学》的强调,实验装置的熟悉度;电解池装置中离子交换膜的知识点
1.“砒霜”是我国古代一味重要的中药,其中含有一定量的砷元素,但同时它也具有剧毒。下列关于砷的说法不正确的是 ( )
A.水体的砷污染,会使水生生物体内砷含量超标,对人体造成危害
B.砷化氢的稳定性比溴化氢的弱,Mg3As2可以发生水解反应生成白色沉淀物质
C.砒霜可以用于癌症治疗,但服用过多可使人致命
D.砷、汞等都属重金属元素,对环境会造成污染。
[解析]此题为原创题。考察学生生活知识面是否丰富以及对元素周期律的应用
5、(12分)[改编]
A、B、C、D、E均为有机化合物,它们之间的关系如图所示(提示:RCH=CHR'在酸性高锰酸钾溶液中反应生成RCOOH和R'COOH,其中R和R'为烷基)。

(1)直链化合物A的相对分子质量小于90,A分子中碳、氢元素的总质量分数为0.814,其余为氧元素,则A的分子式为 ▲ 。
(2)已知B与NaHCO3溶液完全反应,其物质的量之比为1︰2,则在浓硫酸的催化下,B与足量的C2H5OH发生反应的化学方程式是
▲ ,
反应类型为 ▲ 。
(3)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是 ▲ 。
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有 ▲ 。种,其相应的结构简式是 ▲ 。
命题意图:能根据有机化合物结构预测其能发生的有机反应类型的一般思路;了解有机合成路线设计的一般程序;综合考查学生分析和运用能力。
4、(12分)[改编]
图中字母所代表的物质均为中学化学常见物质。其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料;常温下C、D、H为气体单质。单质E、M、N为金属,N是地壳中含量最大的金属元素。Y是红褐色沉淀。这些物质在一定条件下存在如下转化 关系,其中有些反应物或生成物已经略去。试回答下列问题:
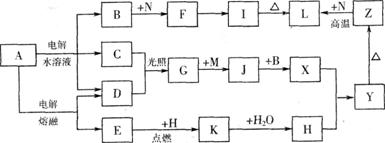
(1) 工业上,在电解A溶液的设备中将阴极区和阳极区用 ▲ 隔开。
(2) Z→L反应的名称是 ▲ ,K的电子式为 ▲ 。
(3) 写出B→F的离子方程式 ▲ 。(4) 写出K与CO2反应的化学方程式 ▲ 。
(5) Y与NaClO和B混合溶液作用,是制备绿色水处理剂(Na2MO4)的一种方法,请写出有关反应的离子方程式 ▲ 。
命题意图:考查电解食盐水的基本原理,并能写出相应的电极反应式和总反应的化学方程式;能列举实例说明氯碱工业产品的主要用途。
3、(7分)[改编]
某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为两者反应生成只有CuCO3一种沉淀;乙同学认为这两者相互促进水解反应,生成Cu(OH)2一种沉淀;丙同学认为生成CuCO3和Cu(OH)2两种沉淀。(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ在探究沉淀物成分前,须将沉淀从溶液中分离并净化。具体操作为①过滤②洗涤③干燥。
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。

⑴各装置连接顺序为 → → 。⑵装置C中装有试剂的名称是 ▲ 。
⑶能证明生成物中有CuCO3的实验现象是 ▲ 。
Ⅲ.若CuCO3和Cu(OH)2两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。

⑴ 实验开始时要通入过量的空气其作用是 ▲ 。
⑵若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO3的质量分数为: ▲ 。
命题意图:考查化学实验室常用仪器的主要用途和使用方法;能识别典型的实验装置图;实验室常用试剂的使用和保存方法。
2、(11分)[改编]
W、X、Y、Z是中学化学中四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,Z能形成红色(或砖红色)Z2O 和黑色的ZO两种氧化物。
(1)写出相关化学式:W ,X ,Y ,Z
(2)W位于元素周期表第_____周期第____族。W的气态氢化物稳定性比H2O (g)____ _(填“强”或“弱”)
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
________________________________________________________________________。
(4)已知下列数据:

X的单质和FeO反应的热化学方程式是____________________________。
命题意图: 考查元素周期律和周期表以及原子核外电子排布式,热化学方程式的书写。
1、(6分)[改编]
(1)天然气是人们日常生活中的清洁能源。
已知①CH4(g)+2O2(g)=CO2(g)+2 H2O(l); △H1=-890.3kJ·mol-1
②2 CO(g)+O2(g)=2CO2 (g); △H2=-566 kJ·mol-1
则反应2 CH4(g)+3O2(g)=2CO(g)+4H2O(l)的△H=_____________。
(2)甲烷燃料电池的化学方程式为CH4+2O2=CO2+2H2O。某甲烷燃料电池以甲烷为燃料,以空气为氧化剂,以熔融的K2CO3(其中不含O2-和 )为电解质,以具有催化作用和导电性能的稀土金属为电极。
)为电解质,以具有催化作用和导电性能的稀土金属为电极。
该燃料电池的负极电极反应式为:CH4-8e-+4 =5CO2+2H2O,则其正极电极反应式为____________;为使电解质的组成保持稳定,使该燃料电池长时间稳定运行,在通入的空气中必须加入________________物质。
=5CO2+2H2O,则其正极电极反应式为____________;为使电解质的组成保持稳定,使该燃料电池长时间稳定运行,在通入的空气中必须加入________________物质。
(3)以该燃料电池为电源,以铂作电极电解1000g 4.55%的NaOH溶液,一段时间后,溶液中溶质的质量分数变为5.00%,则阳极产生的气体在标准状况下的体积为________L。命题意图:考查电化学和热化学知识。在理解所学各部分化学知识的本质区别与内在联系的基础上,运用所掌握的知识进行必要的分析、类推或计算,解释、论证一些具体化学问题。
7、[改编]有4种混合溶液,分别由等体积0.1 mol/L的2种溶液混合而成:①CH3COOK与HCl;②CH3COOK与KOH;③CH3COOK与KCl;④CH3COOK与KHC03
下列各项排序正确的是
A.c(CH3C00一):②>④>③>① B.c(CH3COOH): ①>④>③>②
C.pH:②>③>①>④ D.溶液中C(H+):①>③>②>④学
命题意图:考察学生的守恒思想和综合分析能力,物料守恒+电荷守恒+原子守恒。
第Ⅱ卷
非选择题部分
6、[原创]“瘦肉精”是一类动物用药,在动物代谢中可促进蛋白质的合成,降低脂肪的沉积,加速脂肪的转化和分解。在中国,通常所说的“瘦肉精”则是指克伦特罗。它曾经作为药物用于治疗支气管哮喘,后由于其副作用太大而遭禁用。其结构简式如图所示。下列说法不正确的是
A.分子式为C12H18Cl2N2O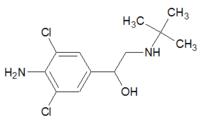
B.该物质最多有6个原子处于同一平面
C.该物质属于芳香族化合物
D.该物质既能发生消去,又能发生催化氧化
命题意图:结合生产、生活实际,了解某些烃、烃的衍生物的重要作用及对环境和健康可能产生的影响;化学在能源和资源的合理开发与安全利用方面的作用;将基础知识与“情感态度与价值观”有机结合,培养学生社会责任感。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com