
题目列表(包括答案和解析)
13.在KIO3、KHSO3的酸性混合溶液中加入少量KI和淀粉,不停地搅拌,有下列反应发生: ① IO3-+ 5I-+ 6H+ → 3I2 + 3H2O ② I2 + 2HSO3-+ H2O → 2I- + 2SO42-+ 4H+
当反应进行到15min时,溶液突然变为蓝色,随之又很快消失。这一反应被称做时钟反应,有人用它来解释生物钟现象。下列有关说法错误的是 ( )
A.在整个反应过程中,起催化作用的物质是KI
B.上述两个反应中,反应速率较快的是②
C.时钟反应的快慢由反应②决定
D.“溶液突然变为蓝色,随之又很快消失”这一现象与①②的反应速率有关
12. 搞好兴奋剂管理是确保2008年奥运会成功举办的主要措施之一。国家体育总局转发了世界兴奋剂机构《2008年禁用清单》,违禁药物有216种,甲异炔诺酮(tibolone)是其中之一,它的结构式如右图,下列有关说法不正确的是 (
)
搞好兴奋剂管理是确保2008年奥运会成功举办的主要措施之一。国家体育总局转发了世界兴奋剂机构《2008年禁用清单》,违禁药物有216种,甲异炔诺酮(tibolone)是其中之一,它的结构式如右图,下列有关说法不正确的是 (
)
A.甲异炔诺酮中含有的官能团有羟基、碳碳叁键、碳碳双键及羰基
B.甲异炔诺酮分子中含有4个手性碳原子
C.1mol甲异炔诺酮在浓硫酸作用下脱去1分子水,所得产物有两种
D.1mol甲异炔诺酮与足量的氢气催化加成,最多消耗4molH2
11. 下列现象或事实解释正确的是
下列现象或事实解释正确的是
A.铁制容器可盛装冷的浓硫酸,因为常温下铁和浓硫酸不反应
B.铝热反应提供一定的能量引发,因为铝热反应为吸热反应
C.增加炼铁高炉(右图)的高度并不能提高CO的转化率,因为化学平衡没有移动
D.鸡蛋清中加入2滴1%醋酸铅溶液后产生沉淀,因为蛋白质发生了盐析
10. MnO2和Zn是制造干电池的重要原料,工业上用软锰矿和闪锌矿联合生产MnO2和Zn的基本步骤为:
⑴ 软锰矿、闪锌矿与硫酸共热: MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O。
 ⑵ 除去反应混合物中的不溶物
⑵ 除去反应混合物中的不溶物
⑶电解混合液 MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4
下列说法不正确的是 ( )
A.步骤⑴中MnO2和H2SO4都是氧化剂 B.步骤⑴中每析出12.8g S沉淀共转移0.8mol电子
C.电解时MnO2在阳极处产生 D.硫酸在生产中可循环使用
9.下列离子方程式书写正确的是( )
A.三氯化铝溶液中加人过量氨水 Al3++3OH- Al(OH)3↓
Al(OH)3↓
B. 稀硝酸中加入过量的铁粉:Fe+6H++3NO3-=Fe3++3NO2↑+3H2O
C. 4mol/L的NaAlO2溶液和7mol/L的HCI等体积互相均匀混合
4AlO2-+7H++H2O 3Al(OH)3↓+Al3+
3Al(OH)3↓+Al3+
D. 盐酸洗涤铜器表面的碱式碳酸铜:Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O
8. A、B、C、D、E五种元素原子序数逐渐增大,且均不超过18。其中A与C、B与E分别为同族元素。原子半径A<B<E<D<C,B原子最外层电子数是次外层的3倍,C、D的核外电子数之和与B、E核外电子数之和相等。下列说法正确的是( ) A.原子电子层数:A<B B.气态氢化物的稳定性:B<E
C.简单离子半径:E<D D.最高价氧化物对应的水化物碱性:C>D
7. 下列描述错误的是
下列描述错误的是
A.单质硅可用于制造光纤和太阳能电池
B.将氯气通入冷的消石灰可制得漂白粉
C.右图所示的三种物质间的相互转化均可一步实现
D.Na2CO3饱和溶液中持续通入CO2气体有固体析出
不定项选择题:本题包括6小题,每小题4分,共计24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
6.下列各组离子在指定条件下一定不能大量共存的是 ( )
① 能使红色石蕊试纸变蓝的溶液中:Na+、K+、CO32-、NO3-、AlO2-
② c (H+)=0.lmol·L-1的溶液中:Cu2+、A13+、SO42-、NO3-
③ 能使碘化钾淀粉试纸变蓝的溶液中: Na+、NH4+、S2-、Br-
④ 由水电离出的c(H+)= 10-2mol·L-1的溶液中:Na+、Mg2+、Cl-、HCO3-
⑤ 在加入铝粉能产生氢气的溶液中:NH4+、 Fe2+、SO42-、NO3-
⑥ 在含有大量 Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
A.①②③ B.①③⑥ C.③④⑤⑥ D.②③④⑤
3.常温离子液体(Ionic Liquid)也称常温熔融盐。硝酸乙基铵((C2H5NH3)NO3)是人类发现的第一种常温离子液体,其熔点为12℃。已知C2H5NH2结合质子的能力比NH3略强,下列有关硝酸乙基铵的说法正确的是 ( )
A.可用作电池的电解质 B.水溶液呈碱性 C.是共价化合物 D.结构和性质类似于硝酸乙酯



 4.阿伏加德罗常数的值约6.02×1023mol-1,下列叙述中错误的是 ( )
4.阿伏加德罗常数的值约6.02×1023mol-1,下列叙述中错误的是 ( )





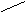 ①12.4g白磷晶体中含有的P-P键数是0.6×6.02×1023 白磷分子
①12.4g白磷晶体中含有的P-P键数是0.6×6.02×1023 白磷分子
②电解精炼铜时转移了6.02×1023个电子,阳极溶解32 g铜
③7.8 g Na2S和Na2O2的混合物中含有的阴离子数大于0.1×6.02×1023
④2mol SO2和1 mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2×6.02×1023 ⑤2.9g 2CaSO4·H2O含有的结晶水分子数为0.02×6.02×1023⑥含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1×6.02×1023
A.①②③④⑤ B.①③④⑤⑥ C.②③⑤⑥ D.③④⑤⑥
5关于下列各装置图的叙述中,不正确的是( )
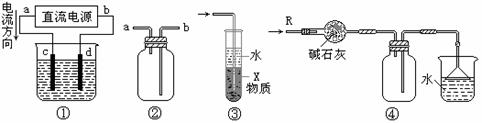
A.装置①中,d为阳极、c为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
2.下列物质的化学用语正确的是 ( )
A.NH4H的电子式: B.硝基苯的结构简式:
B.硝基苯的结构简式:
C.葡萄糖的实验式:CH2O D.甲烷分子的比例模型:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com