
题目列表(包括答案和解析)
8.下列关于S、Si、N、Cl等非金属元素化合物的说法正确的是 ( )
A.SiO2是制造太阳能电池板的主要材料
B.NO、NO2是大气污染物,能在空气中稳定存在
C.漂白精的有效成分是Ca(ClO)2
D.Fe与S化合生成Fe2S3
7.下列说法正确的是 ( )
A.丁达尔现象可以用来区别胶体和溶液 B.水银、水玻璃、胆矾都是纯净物
C.HCl、NH3、BaSO4都是电解质 D.H2、D2、T2属于同素异形体
21.(12分)(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容,请选择其中一题,并在相应的答题区域作答。若两题都做,则按A题评分。
A.短周期元素A、B、C、D、E、F原子序数逐渐增大。它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、角形(V形)、正四面体、角形(V形)、直线形。回答下列问题:
(1)E的核外电子排布式是 。
(2)A的最高价氧化物与B的一种氧化物为等电子体,写出B的氧化物的化学式 。
(3)A和E形成的化合物,其分子的空间构型为 ,A原子的轨道杂化方式是 。
(4)D与F构成物质的晶体类型为 晶体。
(5)写出一个验证E与F的非金属性强弱的离子反应方程式 。
(6)已知A的氢化物极难溶于水,B的氢化物极易溶于水,原因是:
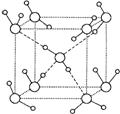
(7)C的氢化物在不同的温度和压力条件下可以形成多种不同
结构的晶体,密度从0.92g/cm3扩到1.5g/cm3。冰是人们迄
今已知的由一种简单分子堆积出结构花样最多的化合物。
其中冰-VII的晶体结构为一个如右图所示的立方晶胞,
每个水分子可与周围 个水分子以氢键结合,晶
体中,amol水可形成 mol氢键。
B.某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
步骤Ⅰ:称取0.4g花生油样品,置于两个干燥的碘瓶(如图)内,加入10mL四氯化碳,轻轻摇动使油全部溶解。向碘瓶中加入25.00mL含0.01mol IBr的无水乙酸溶液,盖好瓶塞,在玻璃塞与瓶口之间滴加数滴10%碘化钾溶液封闭缝隙,以免IBr的挥发损失。
步骤Ⅱ:在暗处放置30min,并不时轻轻摇动。30min后,小心地打开玻璃塞,用新配制的10%碘化钾10mL和蒸馏水50mL把玻璃塞和瓶颈上的液体冲洗入瓶内。
步骤Ⅲ:加入指示剂,用0.1mol·L-1硫代硫酸钠溶液滴定,用力振荡碘瓶,直至终点。
 测定过程中发生的相关反应如下:
测定过程中发生的相关反应如下:
① +IBr →
+IBr →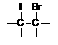
②IBr+KI=I2+KBr
③I2+2S2O32-=2I-+S4O62-
请回答下列问题:
⑴已知卤素互化物IBr的性质与卤素单质类似,实验中准确量取IBr溶液应用 ▲ ,用方程式表示碘瓶必须干燥的原因 ▲ 。
⑵步骤Ⅱ中碘瓶在暗处放置30min,并不时轻轻摇动的原因是 ▲ 。
⑶步骤Ⅲ中所加指示剂为 ▲ ,滴定终点的现象 ▲ 。
⑷反应结束后从液体混合物中回收四氯化碳,则所需操作有 ▲ 。
20.(8分)以天然气为原料合成氨是新的生产氮肥的方法,它具有污染小、成本低等诸多特点,其过程大体如下: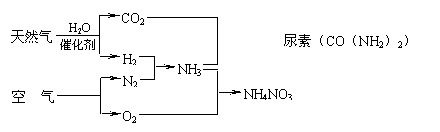
 .
.

某工厂以标准状况下的含CH4 89.6%的天然气100 m3为原料经过上述过程,生产尿素和硝酸铵。
⑴ 合成氨生产过程中氨的产率为60%,假设其它各步反应均完全且不考虑副反应,求100 m3的天然气可生产尿素的质量。(注:产率为实际产量与理论产量之比)
⑵ 为使硝酸生产过程中不再补充空气,假设各步反应均完全且氨中氮元素全部转化为HNO3,空气中氧气的体积分数设为20%,求由氨气和空气组成的原料气中 (不包含被硝酸吸收的氨气)氨气与空气的体积比。
⑶ 实际生产中,若氨的产率为60%,硝酸的产率为80%,求100 m3的天然气最多可生产硝酸铵的质量。
19.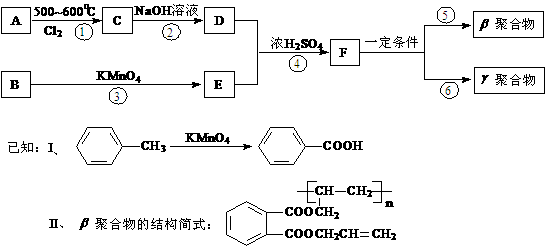 (10分)DAP-A树脂是一种优良的热固性树脂,被用作高级UV油墨的一种成分。用UV油墨印刷的优点是:印刷时油墨极快干燥;对环境及人员无损害;性价比较高。因此,适于大规模生产食品、酒类、洗条剂等包装纸盒。这种材料可采用右侧合成路线制备:
(10分)DAP-A树脂是一种优良的热固性树脂,被用作高级UV油墨的一种成分。用UV油墨印刷的优点是:印刷时油墨极快干燥;对环境及人员无损害;性价比较高。因此,适于大规模生产食品、酒类、洗条剂等包装纸盒。这种材料可采用右侧合成路线制备:
试回答下列问题:
(1)在①~④的反应中属取代反应的是 。
(2)写出反应②的化学方程式 。
(3)写出反应⑤的化学方程式 。
(4)工业上可由C经过两步反应制得甘油,这两步反应的反应类型依次是 和 。
(5)写出B苯环上的二氯代物结构简式: 。
18.(9分)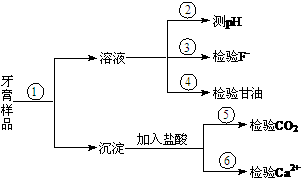 牙膏是生活必需品。下面是牙膏中某些主要成分的检验流程图。
牙膏是生活必需品。下面是牙膏中某些主要成分的检验流程图。
请回答下列问题:
(1)在①中加水、搅拌、静置后,接下来的实验操作名称是 ,所需要的主要玻璃仪器有 。
(2)在②中用pH试纸测溶液的pH的操作方法是 。
(3)已知邻二醇与新制的氢氧化铜悬浊液反应生成绛蓝色溶液,写出④中发生反应的化学方程式: 。
(4)写出⑤中发生反应的化学方程式: 。
(5)将⑤中放出的气体通入澄清的石灰水中时,未见沉淀出现,则可能的原因是:
、 (任答两条)。
(6)实验⑥中鉴定Ca2+的方法: 。
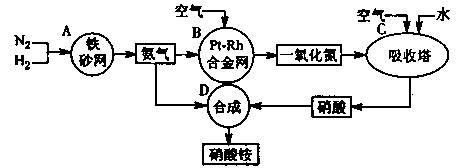
17.(11分)下图是工业生产硝酸铵的流程。
(1)吸收塔C中通入空气的目的是 。
A、B、C、D四个容器中的反应,属于氧化还原反应的是 (填字母)。
(2)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H= -1266.8kJ/mol
N2(g)+O2(g)=2NO(g) △H=+180.5 kJ/mol
写出氨高温催化氧化的热化学方程式: ,
氨催化氧化反应的化学平衡常数表达式K= 。
(3)已知:N2(g)+3H2(g)
 2NH3(g) △H=一92 kJ/mol。
2NH3(g) △H=一92 kJ/mol。
为提高氢气的转化率,宜采取的措施有 。(填字母)
A.升高温度 B.使用催化剂 C.增大压强
 D.循环利用和不断补充氮气 E.及时移出氨
D.循环利用和不断补充氮气 E.及时移出氨
(4)在一定温度和压强下,将H2和N2按3:1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为17.6%,此时H2的转化率为 。
16.(10分)钨是我国丰产元素,是熔点最高的金属 , 广泛用于拉制灯泡的灯丝 , 有“光明使者”的美誉。钨在自然界主要以钨 (+6价) 酸盐的形式存在。有开采价值的钨矿石是白钨矿和黑钨矿。白钨矿的主要成分是钨酸钙 (CaWO4);黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成(Fe,Mn)WO4 ,钨酸(H2WO4)酸性很弱,难溶于水。黑钨矿传统冶炼工艺的第一阶段是碱熔法:
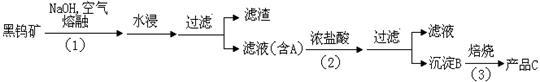 其中 A、B、C 都是钨的化合物。回答:
其中 A、B、C 都是钨的化合物。回答:
(1) 74W在周期表的位置是第 周期。
(2) 写出上述流程中B 、C 的化学式:B____________; C_____________
(3) 钨冶炼工艺的第二阶段则是用碳、氢等还原剂把氧化钨还原为金属钨。对钨的纯度要求不高时 , 可用碳作还原剂。写出用碳还原氧化钨制取金属钨的化学方程式:______________________________________________________________;
为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而必须用氢气作还原剂 ,为什么 ?_____________________________________________。
(4) 仲钨酸的阱盐在热分解时会发生内在氧化还原反应 ,我国钨化学研究的奠基人顾冀东先生采用这一反应制得了蓝色的、非整比的钨氧化物 WO3-x 。 这种蓝色氧化钨具有比表面大、易还原的优点 , 在制钨粉时温度容易控制 ,目前冶炼拉制钨丝的金属钨都用蓝色氧化钨为原料。经分析 , 得知蓝色氧化钨中钨的质量分数为 0.7985。
①计算 WO3-x中的x值。X=_______________ 。
②一般认为,蓝色氧化钨的颜色和非整比暗示了在化合物中存在五价和六价两种价态的钨。则蓝色氧化钨中这两种价态的钨原子数比为________:________。
14.下列各溶液中,微粒的物质的量浓度关系正确的是( )
A.10mL0.5mol/LCH3COONa溶液与6mL1mol/L盐酸混合:
c(Cl-)>c(Na+)>c(H+)>c(OH-)
B.0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
C.在NaHA溶液中一定有:c(Na+) + c(H+) = c(HA-) + c(OH-) + c(A2-)
D.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:
c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl)
非选择题
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com