
题目列表(包括答案和解析)
33.(16分)亚硫酸钠是食品加工中广泛使用的漂白剂、防腐剂和抗氧化剂,其在食品中的残留量通常以二氧化硫含量计算。
(1)亚硫酸盐具有一定的毒性,长期摄入过量的亚硫酸盐,红细胞和血红蛋白会减少,钙的吸收也会减少,原因是 。
检验某黑木耳中是否含有亚硫酸盐的简单方法是:将黑木耳样品剪成碎末放入烧杯,加入20mL水和10mL盐酸,加热一会儿,滴入试剂A,观察现象既可。
(2)加热的作用是 ,加热时间不能太长的原因是 。
(3)试剂A是 。
在足量的亚硫酸钠溶液中加入1-2滴液溴,振荡后溶液变为无色。
(4)写出以上反应的离子方程式 。
(5)以上反应后的溶液中含有SO32-、HSO3-、SO42-、Br-、OH-等阴离子。设计实验检验SO42- 和Br-,写出实验方法。试剂不限。
|
实验操作 |
预期现象与结论 |
|
步骤1: |
|
|
步骤2: |
|
32.(16分)工业上生产高氯酸(沸点:90oC)时还同时生产了亚氯酸钠,其工艺流程如下:
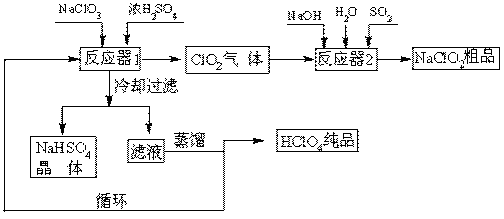
(1)冷却过滤的目的 。
(2)通入反应器2的SO2作用是
;反应器2中发生反应的离子方程式为
 。
。
(3)循环使用的物质是 。
(4)可以通过蒸馏滤液的方法得到高氯酸的原因可能是 。
(5)通过电解NaClO3水溶液的方法也可以制备NaClO4,进而可以制备HClO4,写出阳极的电极反应式 。
31.(16分) 氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300-1700oC的氮气流中反应制得3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)上述反应氧化剂是 ,已知该反应每转移1mole-,放出132.6kJ的热量,该方程式的∆H = 。
(2)能判断该反应(在体积不变的密闭容器中进行)已经达到平衡状态的是( )
A.焦炭的质量不再变化 B.N2 和CO速率之比为1:3
C.生成6molCO同时消耗1mol Si3N4 D.混合气体的密度不再变化
(3)下列措施中可以促进平衡右移的是( )
A.升高温度 B.降低压强
C.加入更多的SiO2 D.充入N2
(4)该反应的温度控制在1300-1700oC的原因是 。
(5)某温度下,测得该反应中N2和CO各个时刻的浓度如下,求0-20 min内N2的平均反应速率 ,该温度下,反应的平衡常数K= 。
|
时间/min |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
40 |
45 |
|
N2浓度/mol·L-1 |
4.00 |
3.70 |
3.50 |
3.36 |
3.26 |
3.18 |
3.10 |
3.00 |
3.00 |
3.00 |
|
CO浓度/mol·L-1 |
0.00 |
0.90 |
1.50 |
1.92 |
2.22 |
2.46 |
2.70 |
- |
- |
- |
30.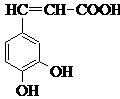 (16分) 咖啡酸(见右),存在于许多中药中,
(16分) 咖啡酸(见右),存在于许多中药中,
如野胡萝卜、光叶水苏、荞麦、木半夏等。咖啡酸
有止血作用,特别对内脏的止血效果较好。
(1)咖啡酸的化学式是 ,咖
啡酸中含氧官能团的名称为 。
(2)咖啡酸发生加聚反应的化学方程式 。
(3)下列关于咖啡酸的说法正确的是( )
A.1mol咖啡酸只与1mol溴反应
B.咖啡酸有一种同分异构体的苯环上连4个羟基
C.咖啡酸的水溶液中滴加氯化铁溶液显血红色
D.可以用高锰酸钾或溴水检验咖啡酸分子中所含的碳碳双键
(4)写出1分子咖啡酸与2分子CH3COCl在一定条件下发生反应生成酯的方程式
。
(5)A是咖啡酸的一种同分异构体,A中苯环上的取代基仅1个,1molA能与2molNaHCO3反应,A的结构简式为 。
23.下列叙述正确的是 ( )
A.0.1mol/L醋酸溶液中:c(H+) = c(CH3COO- ) +c(OH- )
B.中和pH与体积都相同的硫酸和醋酸,消耗NaOH的量后者大于前者
C.由水电离的H+浓度为1.0×10-4mol/L的溶液,pH一定等于4
D.NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3) >c(OH-)>c(H+)
22.下列反应的离子方程式正确的是 ( )
A.用氢氧化钠溶液除去镁粉中的铝粉:2Al+2OH-=AlO2-+H2↑
B.向碳酸氢钠溶液中加入少量氢氧化钙:2HCO3-+Ca2++2OH-==CaCO3↓+CO32-+2H2O
C.氧化铁溶于氢碘酸:Fe2O3 + 6H+=2Fe3++ 3H2O
D.Na2S溶液显碱性: S2-+ H2O HS-+OH-
HS-+OH-
12.短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,下列推测正确的是 ( )
|
|
Q |
R |
|
|
T |
|
|
W |
A.Q形成的化合物的种类最多
B.T位于元素周期表的第三周期第III族
C.Q和R的气态氢化物,前者比后者稳定
D.原子及简单离子半径均是T>W
11.设NA为阿伏加德罗常数的值,下列判断正确的是 ( )
A.含4molHCl的浓盐酸与足量MnO2混合加热,产生NA个Cl2
B.标准状况下,22.4L己烷中共价键数为19NA
C.0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3 NA
D.氧气和臭氧组成的4.8g混合气体中含有0.3 NA个氧原子
10.下列说法错误的是 ( )
A.乙醇可以由玉米制取 B.鸡蛋清中加入CuSO4溶液产生盐析
C.煤的气化可以得到水煤气 D.石油分馏可获得汽油、煤油
9.配制0.1mol/L的NaOH溶液,下列哪些操作会使实验结果偏高 ( )
A.用滤纸称量NaOH固体 B.移液前容量瓶内有水珠
C.摇匀后,液面低于刻度线,再加水至刻度线
D.定容时,俯视刻度线
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com