
题目列表(包括答案和解析)
4、某元素原子的最外层只有2个电子,则该元素
A.一定是ⅡA族元素 B.-定是金属元素
C.一定是正二价元素 D.可能是金属元素,也可能不是金属元素
3、13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,这项研究曾获2002年诺贝尔化学奖。下面有关13C、15N叙述正确的是
A、13C与15N有相同的中子数 B、13C与C60互为同素异形体
C、15N 与14N 互为同位素 D、15N的核外电子数与中子数相同
2、美国科学家将铅和氪两种元素的原子核对撞,获得了一种质子数为118、质量数为293的新元素,该元素原子核内的中子数和核外电子数之差为
A.47 B.57 C.61 D.175
1、下列关于能源和作为能源物质的叙述中不正确的是
A.人类利用的能源都是通过化学反应获得的
B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
C.物质的化学能可以在不同条件下转为热能、电能为人类所利用
D.化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能
24.某化学学习小组对连云港市的能源利用及污染问题进行了调查研究。请你参与并按要求完成下列研究报告。
[研究目的]连云港市的能源利用及污染问题。
[资料获悉]能源可分为一次能源和二次能源,直接从自然界取得的能源为一次能源,一次能源经过加工、转化得到的能源称为二次能源。在石油、煤、天然气、氢气中属于二次能源的是 ▲
[实地调查]该小组深入工厂和家庭进行了调查。
(1)海州电厂一直使用“石灰石--石膏”法对燃煤烟气进行脱硫处理,
请用有关化学方程式表示此方法的反应原理: ▲
(2)水煤气的主要成分是 ▲ ,水煤气经过催化反应可以得到液态烃或含氧有机物,请用化学方程式表示出其中的一例: ▲ 。
[交流讨论]某居民小区正在进行改用天然气作燃料的改造,原有的液化气灶需经怎样的改造才能使用天然气呢?答: ▲ 。(填字母)
A.增大进燃料气口,减小进空气口 B.增大空气进口,减小进燃料气口
C.增大进燃料气口,增大进空气口 D.减小进燃料气口,减小进空气口
[拓展延伸]农村污染也是该小组研究的内容之一,某种农家废料经发酵得到一种含甲烷、二氧化碳、氮气的混合气体2.016 L(标准状况)该气体通过盛有红热CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8 g。将反应后产生的气体通过过量的澄清石灰水中,充分吸收,生成沉淀8.5 g。
CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8 g。将反应后产生的气体通过过量的澄清石灰水中,充分吸收,生成沉淀8.5 g。
(1)原混合气体中甲烷的物质的量是 ▲ 。
(2)原混合气体中氮气的体积分数为多少?(写出计算过程)
赣榆高级中学2010--2011学年度第二学期期中考试
23. (9分)某研究小组为了探究甲烷和氯气反应情况,设计了几个实验。
(9分)某研究小组为了探究甲烷和氯气反应情况,设计了几个实验。
请填写下列空白:
[实验一]用如图所示装置,排水法收集一试管甲烷和氯气的混合气体,
光照后观察到量筒内形成一段水柱,认为有氯化氢生成。
(1)该反应的化学方程式为 ▲ ;(只写第一步)
(2)水槽中盛放的液体最好为 ▲ ;(填标号)
A.水 B.饱和石灰水 C.饱和食盐水 D.饱和NaHCO3溶液
[实验二]用排蒸馏水法收集一试管甲烷和氯气的混合气体,光照反应后,滴加AgNO3溶液,看到有白色沉淀生成,认为有氯化氢生成。
(3)该实验设计的错误之处 ▲
[实验三]
步骤一:收集半试管氯气,加入10 mL 蒸馏水,充分振荡,采用DIS系统的pH传感器测溶液的pH(下同)。测得pH = 3.26。
步骤二:收集一试管甲烷和氯气的混合气体(各占50%),在40 W的日光灯下光照6 min后,加入10 mL 蒸馏水,充分振荡,测得pH = 1.00。
(4)判断该反应中有氯化氢生成的依据是 ▲ ;
(5)假设氯气完全参与反应,且不考虑氯气溶解于水。往反应后的溶液中加水稀释到100.00 mL,取20.00 mL稀释液,加入10.00 mL浓度为0.01 mol·L-1的AgNO3溶液恰好完全反应,则试管中原有氯气在标准状况下的体积为 ▲ mL;
22.(7分)燃料电池是利用燃料(如CO、H2、CH4等)与氧气反应,将反应产生的化学能转变为电能的装置,通常用氢氧化钾作为电解质溶液。完成下列关于甲烷(CH4)燃料电池的填空:
(1)甲烷与氧气反应的化学方程式为: ▲
(2)已知燃料电池的总反应式为CH4+2O2+2KOH==K2CO3+3H2O,电池中有一极的电极反应为CH4+10OH--8e-== CO2-3+7H2O,这个电极是燃料电池的 ▲ (填“正极”或“负极”),另一个电极上的电极反应式为: ▲
(3)随着电池不断放电,电解质溶液的碱性 ▲ (填“增大”、“减小”或“不变”)
(4)通常情况下,甲烷燃料电池的能量利用率 ▲ (填“大于”、“小于”或“等于”)甲烷燃烧的能量利用率。
21.(6分)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
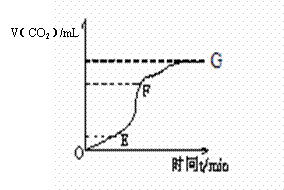
(1)(2分)实验过程如下图所示,分析判断:____▲____段化学反应速率最快,_▲______段收集的二氧化碳气体最多。
(2)(2分)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是( )
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)(2分)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答出两种) ▲ 。
20.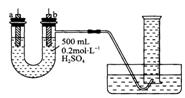 (7分)给你提供纯锌、纯铜片和500ml 0.2mol/L的H2SO4溶液、导线 、1000ml量筒。试用下图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量。
(7分)给你提供纯锌、纯铜片和500ml 0.2mol/L的H2SO4溶液、导线 、1000ml量筒。试用下图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量。
(1)如图所示,装置气密性良好,且量筒中已充满了水,则实验开始时,首先要 ▲ 。
(2)a极材料为 ▲ ,其电极反应式为 ▲ ;
b极材料为 ▲ ,其电极反应式为 ▲ 。
(3)当量筒中收集到672ml气体时,(标况下)通过导线的电子的物质的量是 ▲ 。
19.(4分)下列各组物质 ① O2和O3 ② H、D、T ③ 14N和14C ④ CH3CH2CH2CH3 和(CH3)2CHCH3 ⑤乙烷和丁烷 (请在横线上填写序号)
互为同系物的是 ▲ , 互为同分异构体的是 ▲ _,
互为同位素的是 ▲ , 互为同素异形体的是 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com