
题目列表(包括答案和解析)
5.算出S2(g)分子中键能(B.E):ΔH3=
4.算出S8(g)→4S2(g)的反应热:ΔH2=
3.算出S8(g)分子离解成S(g)原子的反应热:ΔH1=
2.由结构知识解释S8及S2分子中为何有不同健长?
斜方硫由绉环状S8分子组成如右图所示。可以通过简单杂化轨道知识来讨论它的空间结构。根据最简单的杂化轨道理论,sp杂化组成化学键的键角为180º;sp2杂化理想键角为120º; sp3杂化理想键角为109º28’。特别指出的是在sp2和sp3杂化中所生成的杂化轨道,如没有完全结合上其它原子,或者所结合的原子种类不同,则键角将在较小范围内偏离理想的值。S8分子中键角约为108º,S-S键长为205pm,平均键能(B.E)为266kJ/mol,ΔHf=102.3kJ/mol(ΔHf定义为在标准状况下由稳定单质生成1mol物质时的反应热)。高温下气态分子S8可离解成气态分子S2(ΔHf=128.37kJ/mol,S2分子中键长缩短为189pm)。请回答下列问题:
1.由结构知识解释S8为何为绉环状?
4.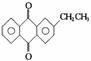 现在工业上常用2-乙基-9,10-蒽醌(结构式如右图所示)来生产H2O2。
①试写出合成H2O2的反应式。
②试以石油馏份中C9以下化合物合成2-乙基-9,10-蒽醌。
现在工业上常用2-乙基-9,10-蒽醌(结构式如右图所示)来生产H2O2。
①试写出合成H2O2的反应式。
②试以石油馏份中C9以下化合物合成2-乙基-9,10-蒽醌。
3.工业上以电解NH4HSO4来制备H2O2。已知某NH4HSO4溶液,以4.00×103A的电流电解2.00小时后,生成H2O2 3.00kg,同时阴极与阳极放出气体体积之比为6:1。设电解后测溶液中H2O2含量时,S2O82-时都已分解,且电解中H2O2不分解。①求电解生成H2O2的电流效率;②忽略电阻,指出电流主要损失在何处?写出有关反应式?
2.已知重金属离子Fe2+、Mn2+、Cu+和Cr3+等可催化H2O2分解。试写出H2O2被 Fe2+催化分解的机理。
1.H2O2的水溶液是一种常用的杀菌剂,其质量百分比一般为3%和30%,在分析上常用 KMnO4来标定H2O2的浓度。①写出 KMnO4滴定H2O2的离子方程式;②某同学在滴定H2O2时,先水浴加热到60℃-70℃,然后滴定,滴了几毫升后,忽然发现没加H2SO4,立即补加H2SO4,然后继续滴定。指出此同学操作中的错误,并解释之。
4.这些化合物的导电性属于 (金属、半导体或绝缘体)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com