
题目列表(包括答案和解析)
21.(8分)某人买了两瓶消毒液,不小心将两种液体混在一起,结果产生大量氯气而中毒。经测定:
(a)用pH试纸测量:甲瓶中消毒液pH=12,乙瓶中消毒液pH=2,且都能很快使pH试纸白。
(b)向乙中加入MnO2粉末,产生大量氧气,并闻到一股醋酸气味。
(c)向甲中加入硝酸酸化的AgNO3溶液,向乙中加入盐酸酸化的BaCl2溶液,均有白色沉淀产生。
(1)甲瓶中的消毒剂一定含有的阴离子是 和 ,乙瓶中的消毒剂的合成反应在一定条件下是可逆反应,此反应方程式为 。
(2)甲液与乙液混合时,产生氯气的离子方程式为 甲液与乙液混合时还产生了氧气,生成氧气的离子方程式为 。
20.某工业反应混合液中仅可能含有的组分是乙醚C4H10O、乙醇C2H6O和水,经分析液体中各原子数之比C:H:O=16:42:5。若混合液中只含两种组分,则可能的组合是
A.乙醚和乙醇 B.乙醚和水 C.乙醇和水 D.乙醛和丁醇
19.下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是:
A.NaClO (aq) 中通入少量CO2 : ClO- + CO2 + H2O = HClO +HCO3-
B.FeCl2在空气中被氧化:4Fe2+ + O2 + 2H2O = 4Fe3+ + 4OH-
C.Al Cl3 (aq)中投入过量Na:Al 3+ + 4Na + 2H2O = AlO2-+ 4Na+ + 2H2↑
D.FeBr2 (aq) 中通入少量Cl2:2Fe2+ + 4Br- + 3Cl2 = 2Fe3+ + 2 Br2 + 6Cl-
18.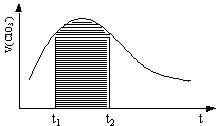 氯酸钾和亚硫酸氢钠发生氧化还原反应:ClO3-+3HSO3-=3SO42-+3H++Cl-,右图为该反应速率随时间变化的图像。图中V(ClO3-)是用ClO3-在单位时间内的物质的量浓度的变化来表示的反应速率。则下列说法不正确的是
氯酸钾和亚硫酸氢钠发生氧化还原反应:ClO3-+3HSO3-=3SO42-+3H++Cl-,右图为该反应速率随时间变化的图像。图中V(ClO3-)是用ClO3-在单位时间内的物质的量浓度的变化来表示的反应速率。则下列说法不正确的是
A反应开始时速率增大可能是c(H+)增大引起的
B若坐标改为υ(Cl-)时,速率时间曲线和右图曲 线完全重合
C后期反应速率下降的原因是反应物浓度减少
D图中阴影部分“面积”为 t1至t2时间内ClO3-的物质的量的减少值
17.用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是
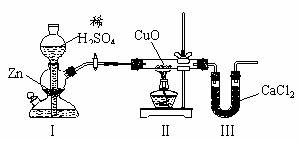
A.Ⅰ、Ⅱ装置之间缺少干燥装置 B.Ⅲ装置后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝 D.CuO没有全部被还原
16.CS2是一种恶臭气体,把它滴入用硫酸酸化的KMnO4溶液中,有一种淡黄色沉淀析出,同时把产生的CO2通入A mol Ca(OH)2的溶液中得到B mol白色沉淀,则CS2被氧化时,转移电子的物质的量为
A.白色沉淀物质的量的1/3 B.4Bmol或4(2A-B)mol
C.氧化产物的4倍 D.Ca(OH)2的物质的量的4倍或3倍
15.下列结晶水合物,不可用直接加热方法使其转变为无水盐的是
A.AlCl3·6H2O B.CuSO4·5H2O C.Hg(NO3)2·H2O D。Na2CO3·10H2O
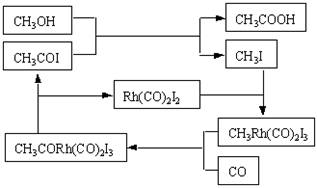
14.某工厂生产醋酸,由于使用新工艺, 使产率比旧工艺(乙醛氧化法或丁烷氧化法)提高了十几个百分点,大幅度降 低了成本,该新工艺的反应原理如下:根据图分析生产醋酸的起始原料和起始 催化剂都正确的是
A.CH3I、CO;CH3Rh(CO)2I3
B.CH3COI、CH3I;CH3CORh(CO)2I3
C.CH3OH、CO;Rh(CO)2I2
D.CH3OH、CH3I;CH3Rh(CO)2I3
13. 相同温度下,同物质的量浓度的Na2SO3和Na2CO3的两种溶液中,下列关系式正确的是
相同温度下,同物质的量浓度的Na2SO3和Na2CO3的两种溶液中,下列关系式正确的是
12.商品锂离子电池的正极材料是锂过渡金属氧化物(例如LiCoO2)混以一定量的导电添加物(例如C)构成的混合导体,负极材料是可插入锂的碳负极。两极反应为:
负极:C6+Li++e-→LiC6
正极:Li0.5CoO2+0.5Li++0.5e-→ LiCoO2
表示锂离子电池的总反应式为: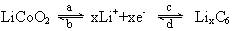 其中表示充电过程的是
其中表示充电过程的是
A.ac B.ad C.bc D.bd
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com