
题目列表(包括答案和解析)
28].(15分)67.0g某过渡金属元素A同134.4L(已换算成标准状况)CO完全反应生成羰基配合物B(A(CO)x),B是黄色油状液体,易挥发,沸点103℃;B在200℃时自燃,得到95.8g A的氧化物C。B与适量氯水反应得到D,元素分析得D中含A 23.4%;B也能被硝酸氧化。将B与2-丁炔一起在光照下反应,完毕后分离出产物E,元素分析得E中含A 18.4%、C 51.3%、H 3.9%,A分子中还检测到1个六元环。
(1)推断A-E各物质的化学式;
(2)预测B在水和CCl4中的溶解性;预测B在物质合成中的用途;
(3)分别写出B自燃、与氯水、硝酸反应的方程式;
(4)画出E的可能结构简式,并写出反应方程式。
27].(8分)如图,活塞的质量与筒壁的摩擦力不计,与K相连的细管的体积也忽略不计。在标准状况下:
(1)b中气体与水不接触,打开K,足够长时间后,a中气体体积减小的范围是:△V(减小) 。
(2)在上述(1)之后,快速推a中活塞至a中气体全部进入b中,观察到的现象是 ,原因是 。
(3)若固定a中活塞如图所示,打开K,移走b的密封套,足够长时间后,观察到的现象是 ,所得溶质的物质的量浓度为(设溶质不扩散到水槽中) 。
26].(10分)有机物A(A1-A5)与乙酸无论以何种比例混合,只要质量一定,完全燃烧后产生的水的质量也一定,试回答:
(1)若A1是烃,则A1应满足的通式是 ;
(2)若A2与聚酰胺、聚碳酸酯、改性聚苯醚、聚对苯二甲酸丁二醇酯并称为5大工程塑料,则A2的结构简式是 。
(3)若A3是一种我们熟知的物质,其与乙酸的最简式不同,相对分子质量小于90,则A3的结构简式为 。
(4)若A4和A5互为同分异构体,它们的相对分子质量小于200,A4分子每个碳原子都达到饱和而A5具有芳香性,A4能与金属钠反应而A5能与银氨溶液反应,则A4的结构简式为 ;满足条件的A5的同分异构体有 种。
25].(9分)有机物A由于其特殊的电子结构,一直受到理论化学家的注意,由于缺乏有效的合成途径,一度延缓对其反应的研究,直到1993年出现了可以大量制备的方法。A是非极性分子,化学式是C6H8,核磁共振标明分子中所有氢原子都等价。
(1)画出A的结构简式 ;A的二氯取代产物的位置异构体有 种。
(2)︰CX2为二卤卡宾(Carbene,碳烯,X=Cl,Br)是一类活性中间体,是合成三元环的常用试剂。A能与︰CX2反应生成B。
①写出B的结构简式 ;
②从A→B的化学反应类型是 。
③试分析︰CX2活泼的原因 。
④二氯卡宾可以由氯仿与叔丁醇钾等试剂制备。请写出该反应方程式 。
⑤B可以水解得更有用的衍生物,请写出水解产物 。
24].(9分)人们日常生活中广泛使用干电池,但电池中含有的重金属会严重污染环境,随着人们环保意识的加强,对废旧电池的无害化处理和综合利用显得越来越重要。
(1)锌-锰干电池表达式为:(-)Zn(s)∣ZnCl2(aq),NH4Cl(aq)∣MnO2(s),C(s)(+)
①请写出阳极和阴极的电极反应(MnO2在阴极上还原为三价的MnO(OH));
②次级反应的主要产物是微溶的Zn(NH3)2Cl2,请写出次级反应的离子反应方程式和总电池反应。
(2)采用湿法硫酸浸取锌锰干电池(并加入FeS)的处理工艺方法,制取的硫酸锌和硫酸锰用于配制复合微肥,具有一定的实用价值。
①该反应另外加入FeS,作用是 。
②请写出该反应的两个化学反应方程式
③硫酸锌和硫酸锰溶液中可能会引入的新杂质是什么,如何除去?
23].(9分)1919年,Langmuir提出:原子数相同、电子数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近,称为等电子原理。后来,该原理被推广使用于一些具有特殊功能的晶体的发现和人工合成等诸多领域。如:X是一种新型无机材料,它与碳化硅(SiC)结构相似、物理性质相近,符合该原理。X有如下的转变:
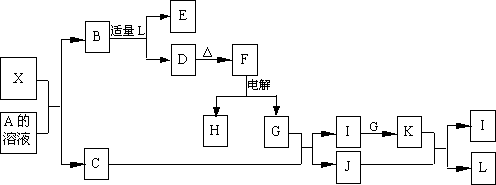
其中:C是气体,D为白色沉淀,E溶液的焰色反应中火焰呈黄色。回答以下问题:
(1)写出X的化学式: ,X属于 晶体(填“原子”、“分子”或“离子”)。
(2)①写出X与A溶液反应的化学方程式: 。
②写出K与J反应的离子方程式: 。
③H与L稀溶液反应的离子方程式 。
(3)X与SiC的复合粉末是新一代大规模集成电路的理想散热材料。最近日本科学家研究出一种新物质与气体单质(物质的量1︰2)制备该纳米级复合材料的方法,请将该反应补充完整。
(新物质)+2 (单质)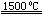 4X+SiC+3C。
4X+SiC+3C。
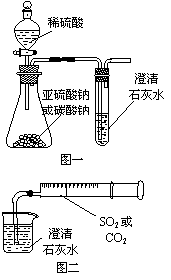 [21].(7分)某同学用如图一所示的装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2可以看到先浑浊后澄清的现象,但通入SO2没有能看到浑浊现象。经过思考分析后,该同学改用图二的装置,将气体收集在注射器,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,都能看到石灰水先变浑浊再澄清的现象,且通入SO2产生现象明显比通入CO2快。
[21].(7分)某同学用如图一所示的装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2可以看到先浑浊后澄清的现象,但通入SO2没有能看到浑浊现象。经过思考分析后,该同学改用图二的装置,将气体收集在注射器,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,都能看到石灰水先变浑浊再澄清的现象,且通入SO2产生现象明显比通入CO2快。
(1)对比分析两组实验,你认为用图一装置实验时,通入SO2不能出现浑浊的原因可能是 。
(2)用图二装置实验时,以相同速率通入CO2或SO2,SO2产生浑浊、澄清的现象比CO2快的原因是 。
(3)用图一进行SO2与石灰水反应的实验时,从安全角度考虑装置应做何改进? 。
22].(13分)某Na2SO3样品,其中可能含Na2SO4、K2SO4、K2CO3、NaCl中的一种或几种。为测定样品成分及其含量,称取样品5.0g,加入5mL 6mol/L的硫酸(过量),标准状况下测定气体的体积。向逸出气体后的溶液中滴加足量BaCl2溶液,过滤得沉淀9.32g。取滤液作焰色反应实验,隔着蓝色钴玻璃观察无紫色。
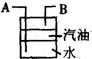
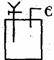
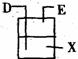

甲 乙 丙 丁
(1)用上图仪器组装实验,气流从左向右各管口联接顺序是 。
(2)丙中X液体是 ,丁中的玻璃容器最好用 ;甲中汽油的作用是 ,目的是 。
(3)要准确测定生成气体的体积,简述有关操作及注意事项。
(4)实验结束时测得丁中液体的体积为560mL,通过计算和推断,确定样品的组分及各组分的质量分数。
|
一 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
二 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
|
|
|
|
|
|
|
|
|
|
|
20].工业上由二氧化锰制备高锰酸钾可分二步进行,第一步:二氧化锰与氢氧化钾共熔并通入氧气2MnO2+4KOH+O2 2K2MnO4+2H2O;第二步:电解锰酸钾溶液:2K2MnO4+H2O
2K2MnO4+2H2O;第二步:电解锰酸钾溶液:2K2MnO4+H2O  2KMnO4+H2↑+2KOH下列说法叙述正确的是
2KMnO4+H2↑+2KOH下列说法叙述正确的是
A 氧化性:KMnO4>K2MnO4>O2
B 根据上述过程,每生成1mol KMnO4共转移6mol电子
C 第二步电解时,KMnO4在阳极区生成
D 第二步电解时阴极周围pH减小
2006年浙江省名校高二化学竞赛联考(十一)
(时间:120分钟 满分:150分)
班级: 姓名:
|
H 1.008 |
相对原子质量 |
He 4.003 |
|||||||||||||||
|
Li 6.941 |
Be 9.012 |
|
B 10.81 |
C 12.01 |
N 14.01 |
O 16.00 |
F 19.00 |
Ne 20.18 |
|||||||||
|
Na 22.99 |
Mg 24.31 |
Al 26.98 |
Si 28.09 |
P 30.97 |
S 32.07 |
Cl 35.45 |
Ar 39.95 |
||||||||||
|
K 39.10 |
Ca 40.08 |
Sc 44.96 |
Ti 47.88 |
V 50.94 |
Cr 52.00 |
Mn 54.94 |
Fe 55.85 |
Co 58.93 |
Ni 58.69 |
Cu 63.55 |
Zn 65.39 |
Ga 69.72 |
Ge 72.61 |
As 74.92 |
Se 78.96 |
Br 79.90 |
Kr 83.80 |
|
Rb 85.47 |
Sr 87.62 |
Y 88.91 |
Zr 91.22 |
Nb 92.91 |
Mo 95.94 |
Tc [98] |
Ru 101.1 |
Rh 102.9 |
Pd 106.4 |
Ag 107.9 |
Cd 112.4 |
In 114.8 |
Sn 118.7 |
Sb 121.8 |
Te 127.6 |
I 126.9 |
Xe 131.3 |
|
Cs 132.9 |
Ba 137.3 |
La-Lu |
Hf 178.5 |
Ta 180.9 |
W 183.8 |
Re 186.2 |
Os 190.2 |
Ir 192.2 |
Pt 195.1 |
Au 197.0 |
Hg 200.6 |
Tl 204.4 |
Pb 207.2 |
Bi 209.0 |
Po [210] |
At [210] |
Rn [222] |
|
Fr [223] |
Ra [226] |
Ac-La |
Rf |
Db |
Sg |
Bh |
Hs |
Mt |
Ds |
|
19].某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
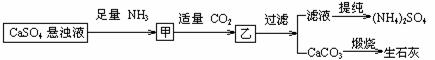
下列推断不合理的是
A 往甲中通CO2有利于(NH4)2SO4生成 B 生成1mol (NH4)2SO4至少消耗2mol CO2
C CO2可被循环使用 D 直接蒸干滤液能得到纯净的(NH4)2SO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com