
题目列表(包括答案和解析)
14].下列物质分离的过程中涉及共价键断裂的是
A 用碱液除去溴苯中的溴 B 用饱和食盐水洗去Cl2中的少量HCl
C 用CCl4萃取碘水中的碘 D 用升华法除去碘中混有的少量NaCl
13].将某些化学知识用数轴表示,可以收到直观形象、简明易记的效果。用数轴表示的下列化学知识中不正确的是
A 常温条件下,酚酞的变色范围: 
B 分散系的分类: 
C AlCl3和NaOH溶液反应后铝元素的存在形式: 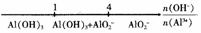
D CO2与NaOH溶液反应的产物: 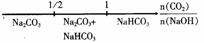
12].已知某溶液中只存在OH-、H+、CH3COO-、Na+四种离子,且其离子浓度的大小顺序为:c(Na+)>c(OH-)>c(CH3COO-)>c(H+),则原溶质可能为
A CH3COONa B CH3COONa、NaOH
C CH3COOH、CH3COONa D CH3COOH、NaOH
11].下列各组离子一定能大量共存的是
A 含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
B 在强碱溶液中:Na+、K+、AlO2-、CO32-
C 在pH=1的溶液中:K+、Fe2+、Cl-、NO3-
D 由水电离的c(H+)=10-14mol·L-1 的溶液中:K+、Na+、Ca2+、HCO3-
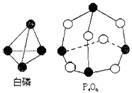
10].化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时放(或吸收)出的能量。已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(KJ·mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的反应热△H为
A -1638KJ/mol B +1638KJ/mol C -126KJ/mol D +126KJ/mol
8].某可逆反应A(g)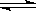 2B(g)+C(g),在甲、乙两个容积相同的密闭容器中进行,开始时在两个容器中均放入0.16mol A,甲容器中3min后B的浓度达到0.12mol/L保持不变,乙容器中2min后C的浓度达到0.06mol/L,且保持不变,下列说法中正确的是
2B(g)+C(g),在甲、乙两个容积相同的密闭容器中进行,开始时在两个容器中均放入0.16mol A,甲容器中3min后B的浓度达到0.12mol/L保持不变,乙容器中2min后C的浓度达到0.06mol/L,且保持不变,下列说法中正确的是
A 甲容器中温度比乙容器中高 B 乙容器中温度比甲容器中高
C 乙容器中使用了催化剂 D 甲容器中使用了催化剂
 [9].2005年诺贝尔化学奖被授予“在烯烃复分解反应研究方面作出贡献”的三位科学家。“烯烃复分解反应”是指在金属钼、钌等催化剂的作用下,碳碳双键断裂并重新组合的过程。如2分子烯烃RCH=CHR'用上述催化剂作用会生成两种新的烯烃RCH=CHR和R'CH=CHR'。则分子式为C4H8的烯烃中,任取两种发生“复分解反应”,生成新烯烃种类最多的一种组合中,其新烯烃的种类为
[9].2005年诺贝尔化学奖被授予“在烯烃复分解反应研究方面作出贡献”的三位科学家。“烯烃复分解反应”是指在金属钼、钌等催化剂的作用下,碳碳双键断裂并重新组合的过程。如2分子烯烃RCH=CHR'用上述催化剂作用会生成两种新的烯烃RCH=CHR和R'CH=CHR'。则分子式为C4H8的烯烃中,任取两种发生“复分解反应”,生成新烯烃种类最多的一种组合中,其新烯烃的种类为
A 5种 B 4种 C 3种 D 2种
7].下列实验操作、目的、结论正确的是
A 浓H2SO4与乙醇的混合液 制乙烯气体
制乙烯气体
B 试液 颜色无明显变化
颜色无明显变化 溶液变血红色,证明试液中含Fe2+
溶液变血红色,证明试液中含Fe2+
C 稀盐酸溶液 对照比色卡,pH为0.5
对照比色卡,pH为0.5
D 乙酸乙酯与乙酸的混合物 弃去上层,除去杂质乙酸
弃去上层,除去杂质乙酸
6].若把质量数为12的碳原子(12C)的对原子质量定为24,并以此确定相对原子质量,以0.024kg 12C所含的碳原子数为阿伏加德罗常数,则原来下列数值肯定不变的有
①浓硫酸的物质的量浓度 ②氧气的溶解度 ③气体摩尔体积 ④阿伏加德罗常数
⑤氧元素的相对原子质量 ⑥2g氢气在标准状况下的体积
A 1个 B 2个 C 3个 D 4个
5].某学生利用厨房中的用品进行家庭小实验研究,现有:鸡蛋壳、食醋、纯净水、食盐、干电池、石墨电极及导线,你认为不能完成的家庭小实验有
A 除去鸡蛋白中的少量食盐 B 自制家用含次氯酸钠溶液的消毒剂
C 检验自来水中是否含氯离子 D 除去热水瓶胆内的水垢
4].对下列对硝酸事实的解释正确的是
A 浓硝酸通常保存在棕色的试剂瓶中,说明浓硝酸不稳定
B 不用浓硝酸与铜屑反应来制取硝酸铜,说明浓硝酸具有挥发性
C 足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
D 锌与稀硝酸反应得不到氢气,说明稀硝酸能使锌钝化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com