
题目列表(包括答案和解析)
18、同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的是( )
A.2Na218O2 + 2H2O == 4Nal8OH + O2↑
B.2KMnO4 + 5H218O2 + 3H2SO4 == K2SO4 + 2MnSO4 + 518O2↑+ 8H2O
C.NH4Cl + 2H2O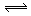 NH3·2H2O + HCl
NH3·2H2O + HCl
D.K37ClO3 + 6HCl == K37Cl + 3Cl2↑+ 3H2O
17、下列离子反应方程式正确的是 ( )
A.用碳酸钠溶液吸收少量二氧化硫气体:2CO32-+SO2+H2O ==2HCO3-+SO32-
B.二氧化硫气体通入到过量Ca(ClO)2溶液中:
SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.在亚硫酸氢铵稀溶液中加入足量的氢氧化钠稀溶液
NH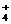 +H++2OH-
+H++2OH- NH3·H2O+H2O
D.KHS的水解:HS-+H2O
 H3O ++S2-
H3O ++S2-
16、对于某些离子的检验及结论一定正确的是 ( )
A. 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有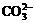
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有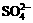
C. 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
15、叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是 ( )
A.
HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(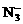 )>c(OH-)
)>c(OH-)
B. HN3与NH3作用生成的叠氮酸铵是共价化合物
C.
NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(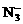 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
D.
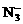 与CO2含相等电子数
与CO2含相等电子数
13、阿伏加德罗常数约为6.02×1023 mol-1,下列叙述中正确的是
A.常温常压下,18.0 g重水(D2O)所含的电子数约为10×6.02×1023
B.室温下,42.0 g乙烯和丙烯的混合气体中含有的碳原子数约为3×6.02×1023
C.标准状况下,22.4 L甲苯所含的分子数约为6.02×1023
D.标准状况下,a L甲烷和乙烷混合气体中的分子数约为 ×6.02×1023
×6.02×1023
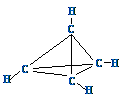
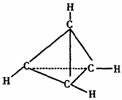 14、一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,
14、一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,
生成的卤代烃的种类共有 ( )
A.2 B.4
C.5 D.6
12、对某酸性溶液(可能含有Br-,SO42-,H2SO3,NH4+)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸
对于下列物质不能确认其在溶液中是否存在的是 ( )
A、Br- B、SO42- C、H2SO3 D、NH4+
11、下列说法正确的是 ( )
A、难失去电子的原子,易形成阴离子
B、单质分子中不存在化学键,化合物的分子才存在化学键
C、含有金属元素的离子不一定是阳离子
D、由不同种原子所形成的纯净物一定是化合物
10、有M、R两种主族元素,已知M2-离子与R+离子核外电子数之和为20,则下列说法不正确的是( )
A、M与R的质子数之和一定等于19
B、M、R可能分别处于第二周期和第三周期
C、M、R可能分别处于第三周期和第二周期
D、M和R的质子数之差可能等于7
9、 Ba(OH)2溶液滴入明矾溶液中,使SO42ˉ全部转化成BaSO4沉淀,此时铝元素的主要存在形式是 ( )
A、Al3+ B、Al(OH)3 C、AlO2ˉ D、Al3+和Al(OH)3
8、下列实验操作正确的是 ( )
A. 将氢氧化钠固体放在滤纸上称量
B.用10mL量筒量取8.58mL蒸馏水
C.制取氯气时,用二氧化锰与浓盐酸在常温下反应,并用排水集气法收集
D.配制氯化铁溶液时,将一定量氧化铁溶解在较浓的盐酸中,再用水稀释到所需浓度
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com