
题目列表(包括答案和解析)
27.(16分)已知,当羟基与双键碳原子相连接时,易发生如下转化:
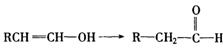
化学式为C8H8O2的有机物有如下的转化关系:
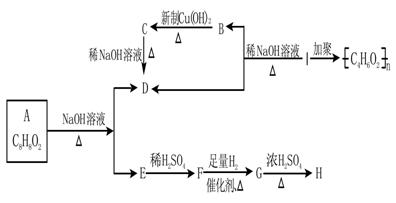
其中F能与FeCl3溶液显紫色。
回答:
(1)结构简式E B I
(2)写出反应类型
B→C G→H
(3)写出下列反应的化学方程式
①A→D+E 。
②B→C 。
(4)写出与A具有相同的官能团且含甲基的A的芳香族化合物的同分异构体的结构简式(不含A):
26.(14分)有A、B、C三种常见的短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半,A元素最外层电子数比B多一个。甲、乙、丙是3种含氧酸的钠盐,甲中含B元素,乙中含C元素,丙中含A元素,甲、丙溶液pH>7,乙溶液pH<7;丁为气体,戊为淡黄色固体。甲、乙、丙、丁、戊、己六种物质之间的相互反应关系如下图:
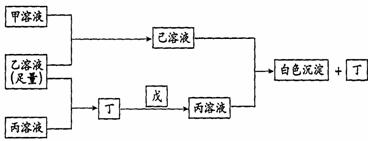
请回答:
(1)写出C元素的原子结构示意图__________,写出丁和戊的电子式__________、__________;
(2)用有关化学用语解释:乙溶液呈酸性的原因___________________;
丙溶液呈碱性的原因_____________________________;
(3)写出有关反应的离子方程式:
① 乙溶液+丙溶液→丁______________________________;
② 己溶液+丙溶液→丁______________________________。
13.将一定质量的锌与10ml18.5mol/L浓硫酸充分反应,锌完全溶解,同时生成标准状况下的气体3.36L。将反应后的溶液稀释至100ml,测得溶液中C(H+)=0.1mol/L。则投入的锌的质量是………………( )
A.6.5g B. 9.75g C. 13g D. 15g
12. 有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是……………………………………………………………( )
A.若HnXOm为强酸,则X的氢化物溶于水后一定显酸性
B.若X(OH)m为强碱,则Y(OH)n一定是强碱
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定是+m
11. 下列离子方程式书写正确的是:………………………………………………………………………( )
A. 向石灰乳中通入Cl2制漂白粉
Cl2 + 2OH- = Cl- + ClO- + H2O
B. 次氯酸钙溶液中通入过量的二氧化碳
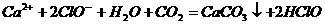
C. 向100mL 0.1moL /L的溴化亚铁溶液中通入0.015 mol的氯气
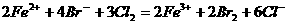
D. 用铁做电极电解稀硫酸溶液的阳极电极式
 4OH- - 4e- = 2H2O + O2
4OH- - 4e- = 2H2O + O2
10.
若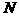 表示阿伏加德罗常数的数值,以下说法中正确的是…………………………………………( )
表示阿伏加德罗常数的数值,以下说法中正确的是…………………………………………( )
A. 标况下,22.4L氟化氢中含2N个原子
B. 12g金刚石中有4N个C-C
C. 1L0.5mol/LNH4Cl溶液中含粒子总数约为N
D. 常温常压下,0.5mol氩气含0.5N个原子
9. 下列叙述正确的是……………………………………………………………………………………( )
A. 由于水分子间存在氢键,所以水很稳定
B. 能与酸反应生成盐和水的氧化物一定是碱性氧化物
C. 原子晶体中,共价键的键能越大,其熔、沸点越高
D. 某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体
8. 下列氢化物不能由单质直接化合制取的是……………………………………………………………( )
A.H2S B. HI C.H2Se D. H2Te
7. 能大量共存的离子组是…………………………………………………………………………………( )
A.HCO3-、NH4+、K+、Ca2+
B.Na+、ClO-、SO32-、SO42-
C.Mg2+、Fe3+ 、 Cl-、SCN-
D.AlO2-、K+、Al3+、NO3-
6. 据报道,科学家发现了一种新的氢微粒,它是由三个氢原子核和二个电子构成的。关于这种氢微粒的叙述正确的是………………………………………………………………………………………… ( )
A. 与氢气是同素异形体 B. 是一种新型化合物
C. 其中含有离子键 D. 能被还原成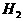
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com