
题目列表(包括答案和解析)
3、用游码托盘天平(1克以下用游码)称量,已知药品的真实质量为9.5g,称量时,错误地把药品放在右盘,法码放在左盘,按这种方法称得的物品的质量是
A、10.0g B、10.5g C、11.0g D、11.5g
2、有关物质的用途叙述不正确的
A、碘化银、干冰均可用于人工降雨; B、皓矾、水玻璃均可做木材防腐剂
C、白磷、磷矿粉均可用于制磷酸 D、纯碱、小苏打均常用作洗涤剂
1、“飘尘”是物质燃烧时产生的粒状飘浮物,颗粒很小(直径小于10-7m)不易沉降(可飘浮数小时甚至数年)。它与空气中的SO2、O2等接触时,SO2会部分转化成SO3,使空气酸度增加,飘尘所起的主要作用是
A、氧化剂 B、还原剂 C、吸附剂 D、催化剂
18.质量分数不等的两种硫酸钠溶液等质量混合时,其质量分数为a %,而等体积混合后的质量分数为b %;质量分数不等的两种乙醇溶液等质量混合时,其质量分数为a %,,而等体积混合后的质量分数为c %。则a、b、c的大小关系正确的是:
A.a>b>c B. b>a>c C. c>a>b D. c>a>b
17.某化工厂工业废水中含H2SO4的质量分数为1%,采用边排放边中和的方法将它处理使之基本呈中性,处理方法如图所示。若处理后废水pH=7,则1%NaOH溶液的流量为:A
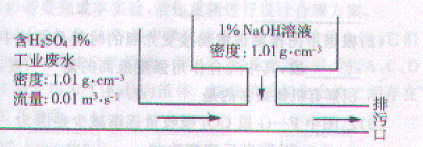
A.0.00816 m3/s B. 0.01 m3/s C.0.01632 m3/s D.0.02 m3/s
16.某盐酸的浓度为12.0 mol·L-1,其密度为1.19 g·cm-3。现有该浓度的盐酸100 m3,则用于吸收HCl形成该盐酸的水的体积是:
A.75.2 m3 B.85.5 m3 C.90.8 m3 D.100 m3
15.体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2 2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率:
2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率:
A、等于p% B、大于p% C、小于p% D、无法判断
14. 酸式盐NaHB在水溶液中,HB–的电离程度小于HB–的水解程度,下列说法正确的是:
 A.HB–水解方程式:HB–+H2O H3O++B2–
A.HB–水解方程式:HB–+H2O H3O++B2–
B.溶液中离子浓度大小为:c (Na+)>c(HB–)>c(OH–)>c(H+)
C.NaHB的存在抑制了水的电离
D.相同物质的量浓度溶液的pH值:Na2B>NaHB
13. 用1kg溶剂中所含溶质的物质的量表示的溶液的浓度叫质量物质的量浓度,其单位是mol/kg。某物质的溶液的质量分数为1.96%,质量物质的量浓度为0.2 mol/kg,则该物质可断为:
A.NaHCO3 B.CaCO3 C.KHCO3 D.Na2CO3
12. 用NA表示阿伏加德罗常数,则下列说法错误的是:
A.1 molCH5+所含的电子数为10NA B.1 molC20H42中含有61 NA个共价键
C.25℃时1 mL纯水中含有10–10NA个OH–离子 D.22.4 L的NH3中含有4 NA个原子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com