
题目列表(包括答案和解析)
1.( )“纳米技术”广泛应用于催化及军事科学中,“纳米技术”是指粒子直径在几纳米(nm)到几十纳米的材料,如将“纳米材料”分散到液体分散剂中,所得混合物具有的性质是(已知1nm=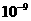 m)
m)
A.能全部通过半透膜 B.具有丁达尔现象
C.所得液体一定能导电 D.所得物质一定为悬浊液或乳浊液
31.甲、乙、丙是三种常见的单质,X、Y、Z是它们的化合物,它们之间有如下图所示的转化关系:
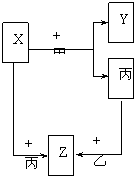 (1)若甲是具有还原性的金属单质,X、Y、Z中有一种是离子晶体,试推断:
(1)若甲是具有还原性的金属单质,X、Y、Z中有一种是离子晶体,试推断:
①X、Y、Z中含有丙元素的是 ;
②写出Y的电子式 ;
③写出X与甲反应的化学方程式,并标出电子转移的方向和数目:
(2)若甲是具有氧化性的黄绿色气体单质,丙通常是暗红色的液体,Y和Z
具有相同的阳离子,X与Z含有相同的离子。
①写出乙物质的化学试 ;
②写出X与足量的甲在溶液中完全反应的离子方程式:
30.将多磷酸钠溶液通过氢型阳离子交换柱,进行Na+与H+的交换,得到多磷酸。经科学研究表明,磷酸和多磷酸的结构分别为:
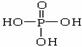 (磷原子几乎处在四面体的中心,三个羟基性质几乎完全相同)
(磷原子几乎处在四面体的中心,三个羟基性质几乎完全相同)
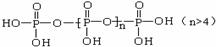
交换后的溶液用0.1 mol·L-1的NaOH溶液滴定。在消耗NaOH溶液 42.00mL和50.00mL时各有一个滴定终点。请回答:
⑴有2个滴定终点的原因是 。
⑵n的值为 ,写出计算依据 。
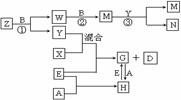
29.A、B、C、D、E是五种中学常见的单质,已知A、B、C、D在常温下均为气态,其中D能分别跟A、B、C在一定条件下两两化合,生成化合物X、Y、Z;A与B、C均不能直接化合,有关的转化关系如下图所示(反应条件均已略去)回答下列问题:
⑴Z分子的空间构型为
⑵反应③中被氧化的物质与被还原的物质的物质的量之比为 。
⑶Z和W在催化剂作用下,反应生成C和Y,这是一个很有实际意义的反应,可以消除W对环境
的污染,该反应的方程式为 。
⑷将过量的E加到N的稀溶液中,若过程中转化的电子数目为3.02×1023个,则参加反应的E的物质的量为 mol。
⑸将Z和N反应后的产物溶于水中,则溶液的pH值(填“<”或“>”) 7,其原因是(用离子
方程式表示) 。
28.某一反应体系中反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。已知水是反应产物之一。
(1)该反应中还原剂是 ;(2)该反应中还原产物是 ;
 (3)若反应过程中转移了0.3mol电子,则生成水的质量是
g。
(3)若反应过程中转移了0.3mol电子,则生成水的质量是
g。
27.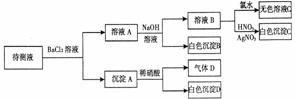 某待测溶液(阳离子为Na+)中只可能含有
某待测溶液(阳离子为Na+)中只可能含有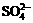 、
、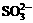 、Cl-、Br-、
、Cl-、Br-、 、
、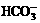 中的一种或若干种,进行下列实验(每次实验所加试剂均足量):
中的一种或若干种,进行下列实验(每次实验所加试剂均足量):
回答下列问题:
(1)待测液中是否含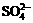 、
、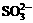 离子
离子
(2)气体D的化学式为 ,反应生成沉淀B的离子方程式为:
(3)根据以上实验,待测液中肯定没有的离子 ;肯定存在的离子是 。
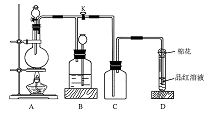
26.下图所示装置为铜跟浓硫酸反应制取二氧化硫的实验装置,请回答下列问题:
 Ⅰ.(1)盛放药品前,检验此装置的气密性的操作方法和现象是:
Ⅰ.(1)盛放药品前,检验此装置的气密性的操作方法和现象是:
_______________
(2)在装置A中放入有关药品后,打开活塞K,将分液漏斗中的液体加入烧瓶中,关闭分液漏斗的活塞,点燃酒精灯,烧瓶中反应的化学方程式为:
(3)装置D中试管口放置的棉花中应浸有一种液体,这种液体是 其作用是:
(4)装置B的作用是贮存多余的二氧化硫和防止其污染环境,则B中应盛放的液体是(填写字母代号)________; a.水 b.浓溴水; c.KMnO4酸性溶液 d.NaHSO3饱和溶液
 Ⅱ.两位同学设计了下述两个方案,并都认为如果观察到的现象和自己设计的方案一致,即可确证无色混合气体中含有CO2和SO2.
Ⅱ.两位同学设计了下述两个方案,并都认为如果观察到的现象和自己设计的方案一致,即可确证无色混合气体中含有CO2和SO2.
试评价上述各方案是否严密,并说明理由:
25. (1) 下列有关实验操作或判断不正确的是 _________
A.用10 mL量筒量取稀硫酸溶液 8.0 mL B.用干燥的pH试纸测定氯水的pH
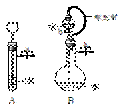 C.用碱式滴定管量取KMnO4溶液 19.60 mL
C.用碱式滴定管量取KMnO4溶液 19.60 mL
D.使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度偏大
E.圆底烧瓶、锥形瓶、蒸发皿加热时都应垫在石棉网上
(2)根据右图描述回答下列问题:
①关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填序号)
A.漏气 B.不漏气 C.不能确定
②关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?(填序号) A.漏气 B.不漏气 C.不能确定
24.( )把CO2和NO的混合气体VL缓缓通过足量的Na2O2固体,充分反应后,测得剩余气体体积大约只有原来的一半,则混合气体中CO2和NO的体积比不可能是
A.2∶1 B.3∶2 C.3∶4 D.5∶4
23.( )将a mol纯铁粉投入含HNO3 b mol的稀溶液里,恰好完全反应并放出NO气体,则a和b的关系是
A.a/b=1/4 B.a/b=3/8 C.1/4≤a/b≤3/8 D.a/b的值无法确定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com