
题目列表(包括答案和解析)
20.(5分)物质的分离是化学研究中常用的方法,填写下列物质分离时需使用的方法(不必叙述操作细节)。
(1)两种互不相溶的液体的分离 ▲ 。
(2)固体和液体的分离 ▲ 。
(3)含固体溶质的溶液中除去部分溶剂 ▲ 。
(4)胶体中分离出可溶电解质 ▲ 。
(5)几种沸点相差较大的互溶液体的分离 ▲ 。
19.(7分)中学化学中几种常见物质的转化关系如下:
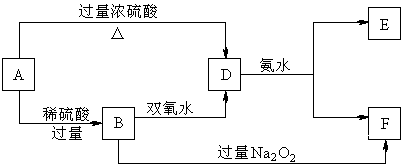
已知A→D的反应必须加热,否则会发生钝化现象。请回答下列问题:
(1)B、D、E的化学式依次为 ▲ 、 ▲ 、 ▲ 。
(2)写出B的酸性溶液与双氧水反应的离子方程式: ▲ 。
(3)写出B和过量过氧化钠反应生成F的化学方程式 ▲ 。
18.(7分)某二元酸(H2A)在水中的电离方程式是:
H2A=H++HA-
HA- H++A2-
H++A2-
回答下列问题:
⑴请判断H2A是强电解质还是弱电解质? ▲ ,理由是 ▲ 。
⑵已知0.1mol·L-1NaHA溶液的pH=2,则0.1mol·L-1 H2A溶液中氢离子的物质的量浓度应 ▲ 0.11 mol·L-1(填“<”,“>”或“=”),理由是: ▲
⑶Na2A溶液显 ▲ (填“酸性”,“中性”或“碱性”)。理由是 ▲ (用离子方程式表示)
⑷H2A溶液和Na2A溶液能否发生反应?能反应的写出离子方程式 ▲ 。
17.(7分) A、B、C三种元素都是短周期元素,它们的原子核外电子层数相同。A、B元素各自形成的A离子和B离子均和Ne元素的原子电子层结构相同,A元素的氢氧化物比B元素的氢氧化物碱性强。5.8gB的氢氧化物恰好能与100mL 2mol/L盐酸完全反应。C元素的单质化学性质活泼但不能直接和氧气反应。根据上述条件,回答下列问题:
(1)A元素和C元素形成化合物的晶体类型是____▲____晶体。
(2)C元素在元素周期表中的位置是 ▲ ;C的最高价氧化物的分子式为 ▲ 。
(3)B的氢氧化物与盐酸反应的离子方程式: ▲ 。
(4)C元素的单质,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为 ▲ 。
16.下表中实验操作能达到实验目的的是
|
|
实验操作 |
实验目的 |
|
A |
向甲酸钠溶液中加新制的Cu(OH)2并加热 |
确定甲酸钠中含有醛基 |
|
B |
向苯酚的饱和溶液中滴加稀溴水 |
制备三溴苯酚 |
|
C |
向酒精和醋酸的混合液中加入金属钠 |
确定酒精中混有醋酸 |
|
D |
将溴乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 |
检验水解产物中的溴离子 |
15.下列各组离子水溶液中能大量共存的是
A.I-、ClO-、NO3-、H+ B.Fe3+、Cu2+、SO42-、Cl-
C.H+、K+、AlO2-、HSO3- D.Ca2+、Na+、SO42-、CO32-
14. 将0.2mol·L-1HCOOH溶液和0.1mol·L-1的NaOH溶液等体积混合后,溶液显酸性,下列关系式中正确的是
A.c(HCOOH)<c(HCOO-) B.c(Na+)>c(HCOO-)
C.c(HCOOH)-c(HCOO-)=c(OH-) D.c(HCOOH)+c(HCOO-)=0.2mol·L-1
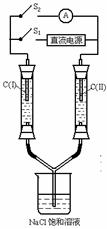
13.如右图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,说明此时该装置形成了原电池,关于该原电池的叙述正确的是
A. C(I)的电极名称是阴极
B.C(II)的电极名称是负极
C.C(I)的电极反应式是2H++2e-=H2↑
D.C(II)的电极反应式是Cl2+2e-=2Cl-
12.下列离子方程式书写正确的是
A.硫酸铝溶液中滴加过量浓氨水:Al3++4OH-=AlO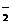 +2H2O
+2H2O
B.NaHCO3溶液水解:HCO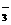 +H2O=H2CO3+OH-
+H2O=H2CO3+OH-
C.浓氢氧化钠溶液吸收少量SO2气体:SO2+2OH-=SO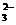 +H2O
+H2O
 D.向小苏打溶液中加入醋酸溶液:HCO
D.向小苏打溶液中加入醋酸溶液:HCO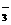 + H+ = CO2↑+ H2O
+ H+ = CO2↑+ H2O
11.阿伏加德罗常数约为6.02×1023mol-1,下列说法正确的是
A.1.0L 1mol/L氨水中,NH3·H2O的分子数为6.02×1023
B.2.4g金属镁变为镁离子时失去的电子数为0.2×6.02×1023
C.白磷分子(P4)呈正四面体结构,31g 白磷中含有P-P键个数为6×6.02×1023
D. 20g 重水(2H216O)中含有的中子数为8×6.02×1023
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com