
题目列表(包括答案和解析)
8.下列各溶液中的离子组能大量共存的是 ( )
A.pH = 0的溶液中:K+、Fe2+ 、Cl-、NO3-
B.使蓝色石蕊试液变红的溶液中:Na+、K+、SO32-、HCO3-
C.c ( H+) = c (OH- )的溶液中:Na+、Ba2+、C1-、SO42-
D. 强碱性溶液中:Na+、K+、AlO2-、CO32-
7.不具有放射性的同位素称之为稳定同位素,稳定同位素分析法在近20年来植物生理学、生态学和环境科学研究中获得广泛应用。如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境分析指示物。下列说法正确的是 ( )
A.34S原子核内中子数为16
B.1H216O在相同条件下比1H218O更易蒸发
C.13C和15N原子核内的质子数相差2
D.2H+的酸性比1H+的酸性更强
6.X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是
A.Y、Z两元素形成的简单阴离子的还原性Z>Y
B.原子半径大小的顺序为W>X>Y>Z
C.X与W形成的化合物W2X2中含有离子键和共价键
D.Y、Z两种元素最高价氧化物的水化物的酸性Z>Y
5.下列说法中正确的是(NA为阿伏加德罗常数) ( )
A.1.5 g CH 中含有的电子数为0.99NA
中含有的电子数为0.99NA
B.34 g氨中含有12 NA个N-H键
C.8.4 g NaHCO3晶体中所含阴阳离子的总数为0.2NA
D.常温下,100 mL 1mol·L-1AlCl3溶液中阳离子总数等于0.1NA
2008.2.20
科学家对H2O2结构的认识经历了较为漫长的过程,最初,科学家提出了两种观点:①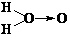 、②H-O-O-H。式中O→O表示配位键,即共用电子对由某原子单方面提供(在化学反应中氧氧键遇到还原剂时易断裂)。
、②H-O-O-H。式中O→O表示配位键,即共用电子对由某原子单方面提供(在化学反应中氧氧键遇到还原剂时易断裂)。
化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a、将C2H5OH与浓H2SO4反应,生成(C2H5)2SO4和水;
b、将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c、将生成的A与H2反应(已知该反应中H2作还原剂)。
⑴用电子式表示①、②两种结构:①______________、②_____________。
⑵如果H2O2的结构如①所示,实验c中化学反应方程式为(A写结构简式,下同)
____________________________________________________;
假如H2O2的结构如②所示,实验c中化学反应方程式为
_____________________________________。
⑶为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案
_________________________________________________________________
2008.2.29
有机物A(C10H20O2)具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。已知:

①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被Cl取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有 (选填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称依次是 、 。
(3)写出与D、E具有相同官能团的同分异构体的可能结构简式:
。
(4)E可用于生产氨苄青霉素等。已知E的制备方法不同于其常见的同系物,据报道,可由2-甲基-1-丙醇和甲酸在一定条件下制取E。该反应的化学方程是
。
2008.3.3
[研究课题]: 探究草酸晶体受热分解的产物。
[查阅资料]: 该小组同学通过查询,获得草酸及草酸晶体的相关知识:
|
名称 |
化学式 |
颜色、状态 |
溶解性 |
熔点(℃) |
密度(g/cm3) |
|
草酸 |
H2C2O4 |
- |
易溶于水 |
189.5 |
1.900 |
|
草酸晶体 |
H2C2O4·2H2O |
无色晶体 |
- |
101.5 |
1.650 |
备注:草酸晶体175℃以上开始分解。
[提出猜想]:请根据草酸晶体的组成对分解可能生成的产物进行猜想。
⑴ ;
⑵分解产物中的气体可能是CO、CO2或它们的混合物。
[设计方案]①为验证“猜想⑴”,请在方框内画出实验设计装置图,并标明所需药品:

②该小组利用下图装置继续进行“猜想⑵”的探究。A、C、F中盛澄清石灰水,B中盛浓NaOH溶液,D中装碱石灰(CaO、NaOH固体混合物),E中装CuO粉末。
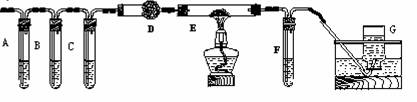
①证明草酸晶体分解产物中有CO2的现象: ;
证明分解产物中有CO的现象: 。
②若未连接G,要达到同样目的,可采取的措施: 。
[交流讨论]:小李同学查阅资料发现:草酸是二元弱酸,但比碳酸强,受热分解时有少量升华,草酸钙和草酸氢钙均为白色不溶物,因此对实验中CO2的检验提出质疑,试根据信息,指出原设计的存在的问题,并提出改进措施 .
2008.3.4
某学习小组做以下实验:在溴水中加入足量乙醛溶液,充分反应,溴水褪色;为探究褪色的原因,他们提出了如下猜想:
①溴水中的Br2可能与乙醛发生取代反应,产生HBr;
②乙醛分子中含有不饱和键,溴水可能与乙醛发生加成反应;
③乙醛具有还原性,溴水可能将乙醛氧化为乙酸,Br2转化为HBr
设计如下方案进行探究:
方案(一):检验褪色后溶液的酸碱性,确定其发生哪类反应;
方案(二):测定反应前溴水中Br2的物质的量和反应后 Br-的物质的量确定其发生哪类反应;
(1)假设测得反应前溴水中Br2的物质的量为a mol,
若测得反应后n(Br-)= 0 mol, 说明溴水与乙醛发生了 反应;
若测得反应后n(Br-) = a mol,说明溴水与乙醛发生了 反应;
若测得反应后n(Br-)= 2a mol,说明溴水乙乙醛发生了 反应。
(2)向含Br2 0.005mol的溴水中加入足量乙醛使其褪色,然后加过量的AgNO3溶液,过滤、洗涤、干燥、称量,得到固体1.88克。已知CH3COOAg易溶于水,通过计算,判断溴水与乙醛发生的反应为 (填序号):
①氧化反应 ②取代反应 ③加成反应
[反思与评价]:方案(一)是否可行?______ 是: 。
A.NaOH溶液 B.酸性KMnO4溶液 C.Na2SO3溶液 D.BaCl2溶液
2008.3.5
某研究性学习小组的一个课题是“NO2能否支持木条的燃烧?”由于实验室中没有现成的NO2气体,该小组的同学设计了两个方案(忽略N2O4的存在,图中铁架台等夹持仪器均已略去):
Ⅰ.实验装置如下图1所示

图1 图2
(1)浓硝酸受热分解的化学方程式是 。
(2)实验开始后木条上的火星逐渐熄灭,有的同学得出“NO2不能支持木条的燃烧”的结论。你认为这一结论是否正确? (填“正确”或“不正确),理由是 。
Ⅱ.实验装置如上图2所示
(1)硝酸铜固体加热分解的产物有氧化铜、二氧化氮和氧气,该反应的化学方程式是
。
(2)当集气瓶中充满红棕色气体时,木条复燃了,有的同学得出“NO2能支持木条的燃烧”的结论。你认为这一结论是否正确? (填“正确”或“不正确”),理由是 。
Ⅲ.为了更直接说明“NO2能否支持木条的燃烧”这一问题,请你重新设计一个简单的实验方案,简述实验原理和主要操作。
2008.3.6
某学生取纯净的Na2SO3·7H2O 50.00g,在密闭容器中经6000C以上的强热至恒重,分析及计算表明,恒重后的样品质量相当于无水亚硫酸钠的计算值,而且各元素的组成也符合计算值,但将它溶于水,却发现溶液的碱性大大高于同时配制的亚酸钠溶液。经过他的实验和思考,这位同学解释了这种反常现象。
(1)他将恒重后的样品溶于水配成溶液,为加速溶解,可采取
的措施,观察发现样品全部溶解,溶液澄清。
(2)取少量(1)中所配溶液,加入足量的用 (填一种酸)酸化的氯化钡溶液有白色沉淀,说明产物中含有 (填离子符号)。
(3)另取少量(1)中所配溶液于试管中,滴加少量盐酸,看到气泡产生,通过 方法闻到臭鸡蛋气味,说明生成 气体,写出生成该气体的离子反应方程式: ;同时发现溶液变浑浊,原因是:(用离子方程式表示) 。
(4)根据以上实验,该同学经分析解释了以上实验中的反常现象,请你用一个化学方程式表示: 。这一反应在上述实验
中 (填“是”或“否”)能确定反应完全。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com