
题目列表(包括答案和解析)
12、在恒温恒容的密闭容器中放入一定量的NO2,发生反应2NO2(g)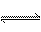 N2O4(g);ΔH<0,达到平衡后,若分别单独改变下列条件,重新达到平衡后,能使该反应的平衡混合气体平均相对分子质量减小的是( )
N2O4(g);ΔH<0,达到平衡后,若分别单独改变下列条件,重新达到平衡后,能使该反应的平衡混合气体平均相对分子质量减小的是( )
A.降低温度 B.通入NO2 C通入N2O4 D.升高温度
11.下列溶液中有关微粒的物质的量浓度关系正确的是( )
A.NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):
c(Na+)=c(HRO3-)+2c(RO32-)
B.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:
c(Na+)>c(Cl-)>c(CH3COOH)
C.常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③NH4HSO4三种溶液中
c(NH4+):③<②<①
D.相同条件下,pH=5的 ①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③
10.用高铁酸钠(Na2FeO4)对江河湖水消毒水消毒是城市饮
水处理的新技术。已知反应Fe2O3+3Na2O2 2Na2FeO4+Na2O有关该反应的叙述正确
的是 ( )
|
B.Na2FeO4是一种氧化性比Na2O2更强的氧化剂
C.3molNa2O2发生反应时,有12mol电子发生转移
D.在Na2FeO4中Fe为+6价,其还原产物为Fe3+,Fe3+水解生成氢氧化铁胶体还有净水作用
9.下列反应的离子方程式正确的是 ( )
A.少量的盐酸逐滴滴入碳酸钠溶液:CO32- +2H+==== CO2↑+H2O
B.过氧化钠与水反应:2Na2O2+2H2O=4Na++4OH-+O2↑
C.少量SO2通入漂白粉溶液中:Ca2++2ClO-+H2O+SO2=CaSO4↓+2HclO
|
D.用惰性电极电解MgCl2溶液:2H2O+2Cl- Cl2↑+H2↑+2OH-
8、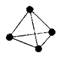 最近罗马大学Fulvio
Cacace等人获得了极具理论研究意义的N4分子,N4分子结构如右图所示(与白磷P4相似)。已知断裂1mol N-N吸收167kJ热量,生成1mol
最近罗马大学Fulvio
Cacace等人获得了极具理论研究意义的N4分子,N4分子结构如右图所示(与白磷P4相似)。已知断裂1mol N-N吸收167kJ热量,生成1mol  放出942kJ热量。由此判断下列说法正确的是
放出942kJ热量。由此判断下列说法正确的是
A.N4属于一种新型的化合物 B.N4与N2互为同分异构体
C.N4沸点比P4(白磷)高 D.1molN4气体转变为N2将放出882kJ热量
7、2008年北京奥运会拟用臭氧、活性炭对游泳池进行消毒和净化,下列说法不正确的是
A、臭氧能杀死水中的病菌,而不影响水质。
B、漂粉精长期露置在空气中会失效。
C、广谱高效杀菌剂二氧化氯的消毒(生成氯离子)效果是等质量的氯气的2.5倍。
D、活性炭能吸附水中的悬浮杂质,对水进行净化
6.食品卫生与人类的身体健康密切相关,下列做法对人体无害的是 ( )
A.使用“瘦肉精”饲料(一种含激素的饲料)养猪,增大猪的瘦肉产量
B.用福尔马林(50%的甲醛)使鱼肉等食品长时间保鲜
C.在鸭饲料里添加工业染料“苏丹红”使鸭子生产红心鸭蛋
D.在食盐中加乳酸锌以防止儿童缺锌
29.(16分)(1)O2- ……………(1分) O22-(或O2-、O3-)………………(1分)
(2)Si ……………………………………………………………………………(2分)
(3)甲烷……………………(1分) H-O-H ………………………(1分)
(4)SiO2+4HF=SiF4↑+2H2O ………………………(2分)
(5)ClO2 (2分) 分子晶体(2分)
(6)三角锥形 (2分) 20Mpa-50Mpa、500℃、铁触媒作催化剂………(2分)
28.(14分)
(1)羧基(2分)、羟基(2分)
(2)①②③④(2分)
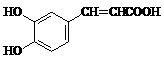
(3) (2分)
(4)448(2分)
(5)(3分)
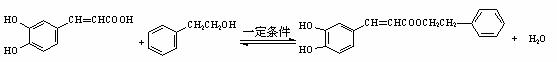
27.(15分)(1)MnO2+2Ci+4H+ Mn2++Cl2↑+2H2O(3分)
(2)饱和食盐水 (2分)
(3)安全瓶,防止倒吸(2分)
|
(4)3Fe+4H2O Fe3O4+4H2
(3分)
(5)2OH-+Cl2=Cl-+ClO-+H2O(2分)
(6)D E C(3分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com