
题目列表(包括答案和解析)
13.在密闭容器中,将1.0 mol
CO与1.0 mol
H2O混合加热到800℃,发生下列反应:CO(g)+H2O(g) CO2(g)+H2(g)。一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol。则下列说法正确的是
CO2(g)+H2(g)。一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol。则下列说法正确的是
A.800℃下,该反应的化学平衡常数为0.25
B.427℃时该反应的平衡常数为9.4,则该反应的△H<0
C.同温下,若继续向该平衡体系中通入1.0 mol的H2O(g),则平衡时CO转化率为66.7%
D.同温下,若继续向该平衡体系中通入1.0 mol的CO(g),则平衡时CO物质的量分数为33.3%
12.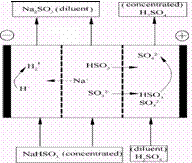 某研究小组用NaOH溶液吸收二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图,则下列有关说法错误的是
某研究小组用NaOH溶液吸收二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图,则下列有关说法错误的是
A.阳极区酸性增强
B.阴极区电极反应式为:2H++2e-=H2↑
C.diluent和concentrated的中文含义为浓缩的、稀释的
D.该过程中的副产品主要为H2SO4
11.已知25℃时有关弱酸的电离平衡常数:
|
弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
|
电离平衡常数(25℃) |
1.8×l0_5 |
4.9×l0_10 |
K1=4.3×l0_7 K2=5.6×l0_11 |
则下列有关说法正确的是
A.等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.a mol·L-1 HCN溶液与b mol·L-1 NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b
C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定存在c(Na+)+ c(H+)=c(OH-)+ c(HCO3-) +2c(CO32-)
10.下列离子方程式中正确的是
A.NaHSO4溶液中加Ba(OH)2溶液至中性: Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
B.NH4HCO3溶液与过量NaOH溶液反应: NH4++OH-=NH3↑+H2O
C.高锰酸钾与乙醇制备Mn3O4纳米粉体,同时生成乙醛:
6MnO4-+13CH3CH2OH→2Mn3O4+13CH3CHO+6OH-+10H2O
D.AlCl3溶液中滴加浓氨水至过量:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
9.某溶液中存在XO3―,且X为短周期元素,则一定能在该溶液中大量共存的离子组是
A.Na+、H+、SO42―、I― B.Na+、Ca2+、CO32―、Al3+
C.Na+、K+、Fe2+、H+ D.K+、SO42―、Cl―、CO32―
8.质量分数为ω的NaOH溶液,其物质的量浓度为a mol·L-1,加热蒸发水份使其质量分数变为2ω,此时,该溶液中NaOH的物质的量浓度为b mol·L-1,则a与b的关系正确的是
A.b=2a B.a=2b C.b<2a D.b>2a
7.一定条件下用甲烷可以消除氮氧化物(NOx)的污染。已知:
① CH4 ( g )+4NO2( g )=4NO( g ) +CO2( g )+2H2O( g ) △H=一574 kJ·mol-1
② CH4 ( g )+4NO( g )=2N2( g )+CO2( g )+2H2O( g ) △H=一1 160 kJ·mol一1。
下列正确的选项是
A.CH4 ( g )+2NO2 ( g )= N2( g )+CO2 ( g )+2H2O ( l) △H=一867 kJ·mol-1
B.CH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子总数为3.2 mol
C.若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ
D.若用标准状况下4.48L CH4 还原NO2至N2,整个过程中转移的电子总数为3.2 mol
6.下列关于工业生产说法正确的是
A.在侯氏制碱工业中,向饱和氯化钠溶液中先通氨气,后通二氧化碳
B.在硫酸工业、合成氨工业、硝酸工业中,均必须对尾气进行吸收处理
C.工业上用电解熔融氧化物的方法制金属镁和铝
D.氯碱工业中的阳离子交换膜阻止阳离子通过
5.用NA表示阿伏加德罗常数,下列说法正确的是
A.8.2 g Na218O2与过量的H216O作用,生成的氧气中含有的中子数为0.8 NA
B.1.4 g乙烯和丙烯的混合物中含碳原子数为0.l NA
C.2.24 L(标准状况)Cl2与足量NaOH溶液在常温下反应.转移的电子数为0.2 NA
D.6.4g CaC2晶体中含有阴阳离子总数为0.3 NA
4.下列有关说法正确的是
A.100 mL 0.02 mol·L-1 的NaCl溶液配制:需要使用天平、100 mL容量瓶等仪器
B.化学反应方向判断:某反应的△H<0、△S<0,则该反应一定是自发反应
C.分离乙醇和苯酚:加NaOH溶液后进行分液
D.硫酸铜晶体制备:结晶,过滤,无水乙醇淋洗并灼烧
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com