
题目列表(包括答案和解析)
10.一定条件下,在体积为10L的密闭容器中,1molX和1molY进行反应:
 2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是
2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是
A.以X浓度变化表示的反应速率为0.001mol·L-1·s-1
B.其它条件不变,将容器体积变为20L,Z的平衡浓度变为原来的1/2
C.其它条件不变,若增大压强,则物质Y的转化率减小
D.其它条件不变,若升高温度,X的体积分数增大,则该反应的△H>0
9.一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
① CH4 (g)+4NO2 (g)=4NO (g) +CO2 (g)+2H2O (g) ;△H=―574 kJ·mol-1
② CH4 (g)+4NO (g)=2N2 (g)+CO2 (g)+2H2O (g) ;△H=―1160 kJ·mol一1。
下列选项正确的是
A.CH4 (g)+2NO2 (g)= N2 (g)+CO2 (g)+2H2O (l) ;△H=―867 kJ·mol-1
B.若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ
C.CH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子为3.2 mol
D.若用标准状况下2.24L CH4还原NO2至N2,整个过程中转移的电子为1.6 mol
8.常温下,0.1mol·L-1某一元酸(HA)溶液中c(OH-)/c(H+)=1×10-8,下列叙述正确的是
A.该溶液中由水电离出的c(H+)=1×10-3 mol·L-1
B.由pH=3的HA与pH=11的NaOH溶液等体积混合,溶液中c(Na+)>c(A-)>c(OH-)>c(H+)
C.浓度均为0.1mol/L的HA和NaA溶液等体积混合后,若溶液呈酸性,则
c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-)
D.0.1mol·L-1HA溶液与0.05mol·L-1NaOH溶液等体积混合后所得溶液中
2c(H+)+c(HA)=c(A-)+2c(OH-)
7.有人认为CH2 = CH2与Br2的加成反应,实质是Br2先断裂为Br+和Br-,然后Br+首先与CH2 = CH2一端碳原子结合,第二步才是Br-与另一端碳原子结合。根据该观点如果让CH2 = CH2与Br2在盛有NaCl和NaI的水溶液中反应,则得到的有机物不可能是
A.BrCH2CH2Br B.ClCH2CH2Cl C.BrCH2CH2I D.BrCH2CH2Cl
6.在试管中注入某红色溶液,给试管加热,溶液颜色逐渐变浅,则原溶液可能是
①滴有石蕊的H2SO4溶液 ②滴有酚酞的氨水溶液
③滴有酚酞的氢氧化钠溶液 ④滴有酚酞的饱和氢氧化钙溶液
⑤滴有酚酞的Na2CO3溶液 ⑥溶有SO2的品红溶液
A.②⑥ B.②④ C.①③⑤ D.②④⑥
5.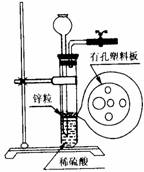 右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是
右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是
①食盐水 ②KNO3溶液 ③适量稀硫酸铜溶液
④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
A.①③⑤
B.②⑥
C.③⑤
D.①②④
4.在给定条件下,下列加点的物质在化学反应中完全消耗的是
A.用50mL 8mol/L的浓盐酸与10g二氧化锰共热制取氯气
B.向100mL 3mol/L的硝酸中加入5.6g铁
C.标准状况下,将1g铝片投入20mL 18.4mol/L的硫酸中
D.在5×107 Pa、500℃和铁触媒催化的条件下,用氮气和氢气合成氨
3.在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高B
A.所用NaOH已经潮解 B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里 D.称量时误用“左码右物”
2.NA表示阿伏加德罗常数,下列叙述正确的是
A.如果5.6LN2含有n个氮分子,则阿伏加德罗常数一定约为4n
B.46gNO2和N2O4混合气体中含有原子数为3NA
C.含有1mol碳原子的金刚石,C-C共价键数为2NA
D.常温下1mol氯气与熟石灰完全反应转移电子数为2NA
1.化学用语是学习化学的重要工具。下列用用来表示物质变化的化学用语中正确的是
A.K37C1O3与浓盐酸(HC1)在加热条件时生成氯气的化学方程式:
K37C1O3+6HC1=K37C1+3C12↑+3H2O
B.表示氢气燃烧的热化学方程式:H2(g)+1/2O2(g)=H2O(g);△H=-241.8kJ/mol
|
Fe3++3H2O
Fe(OH)3(胶体)+3H+
D.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com