
题目列表(包括答案和解析)
7、(2005年广东)下列反应的现象描述与离子方程式都正确的是
A.金属镁与稀盐酸反应,有氢气产生;Mg+2H++2Cl-=MgCl2+H2 ↑
B.氯化钡溶液与硫酸反应,有白色沉淀产生;Ba2++SO42-=BaSO4 ↓
C.碳酸钠溶液与盐酸反应,有气泡逸出;Na2CO3+2H+=2Na++H2O+CO2↑
D.过量铁粉与氯化铁溶液反应,溶液变浅绿色;Fe+Fe3+=2Fe2+
6.(2005年广东)下列反应离子方程式正确的是
A.向氯化铝溶液中加入过量氢氧化钠溶液:Al3+ + 4OH- == AlO2- + 2H2O
B.向苯酚钠溶液中通入二氧化碳:CO2 + H2O + 2C6H5O- →2C6H5OH + CO32-
C.向小苏打溶液中加入醋酸溶液:HCO3- + H+ == CO2↑+ H2O
D.向溴化亚铁溶液中通入过量氯气:Fe2+ + 2Br- + 2Cl2 == Fe3+ + Br2 + 4Cl-
5、(2004上海卷)下列离子方程式中正确的是
A.硫化亚铁放入盐酸中 S2- + 2 H+ → H2S ↑
B.硫酸铜溶液中通入硫化氢 Cu2+ + H2S → CuS↓ + 2 H+
C.氯化铝溶液中加入过量氯水 Al3+ + 4NH3•H2O → AlO2- + 4NH4+ +2H2O
D.碳酸氢铵溶液中加入过量氢氧化钠溶液 HCO3- + OH- → CO32- + H2O
4、(2004年江苏卷)下列反应的离子方程式书写正确的是
A.硫酸铝溶液中加入过量氨水 Al3++30H-══Al(OH)3↓
B.电解饱和食盐水 2Cl-+2H2O H2↑+C12↑+20H-
H2↑+C12↑+20H-
C.碳酸钙与盐酸反应 CaCO3+2H+═Ca2++CO2↑ +H2O
D.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液 Fe2++2H++H2O2══Fe3++2H2O
3、(2004年广东卷)下列离子方程式中,正确的是
A、在氯化亚铁溶液中通入氯气 Fe2+ + Cl2 = Fe3+ + 2Clˉ
B、三氯化铁溶液跟过量氨水反应 Fe3+ + 3NH3•H2O = Fe(OH)3↓ + 3NH4+
C、碳酸氢钙溶液跟稀硝酸反应 Ca(HCO3)2 + 2H+ = Ca2+ + 2H2O + 2CO2↑
D、氯气通入冷的氢氧化钠溶液中 2Cl2 + 2OHˉ = 3Clˉ + ClOˉ + H2O
2、(2004年北京春).下列离子方程式中,正确的是
A.硫酸亚铁溶液与过氧化氢溶液混合 Fe2++2H2O2+4H+ Fe3++4H2O
B.小苏打溶液与稀硫酸混合
CO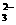 +2H+
+2H+ CO2↑+H2O
|
D.明矾溶液加热水解生成沉淀 Al3++3H2O Al(OH)3↓+3H+
1.(2004年全国)下列离子方程式正确的是 ( )
A.澄清的石灰水与稀盐酸反应Ca(OH)2 + 2H+ === Ca2+ + 2H2O
B.钠与水的反应Na + 2H2O === Na+ + 2OH -+ H2↑
C.铜片插入硝酸银溶液中Cu + Ag+ === Cu2+ + Ag
D.大理石溶于醋酸的反应CaCO3 + 2CH3COOH === Ca2+ + 2CH3COO- +CO2↑+ H2O
25.(08北京卷)由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样进行下列实验(部分产物略去):
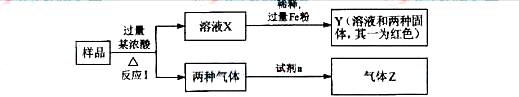
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填化学式)________________。
(2)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是______________________________。
②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是________________。
(3)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)________________。
(4)取Y中的溶液,调节pH约为7,加入淀粉KI和H2O2,溶液呈蓝色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是_________________________________。
(5)另取原样品,加入足量稀硫酸充分反应,若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中物质用化学式表示)__________________________。
24.(08北京卷)通常状况下,X、Y和Z是三种气态单质。X的组成元素是第三周期原子半径最小的元素(稀有气体元素除外);Y和Z均由元素R组成,反应Y+2I-+2H+===I2+Z+H2O藏作为Y的鉴定反应。
(1)Y与Z的关系是(选填字母)___________。
a、同位素 b、同系物 c、同素异形体 d、同分异构体
(2)将Y和二氧化硫分别通入品红溶液,都能使品红褪色。简述用褪色的溶液区别二者的实验方法_____________________________________________________________________________________。
(3)举出实例说明X的氧化性比硫单质的氧化性强(用化学方程式表示)。
______________________________________________________。
(4)气体(CN)2与X化学性质相似,也能与H2反应生成HCN(其水溶液是一种酸)。
①HCN分子中含有4个共价键,其结构式是____________________。
②KCN溶液显碱性,原因是(用离子方程式表示)_________________________________。
(5)加热条件下,足量的Z与某金属M的盐MCR3(C为碳元素)完全反应生成CR2和MmRn(m、n均为正整数)。若CR2质量为w1g,MmRn质量为w2g,M的相对原子质量为a,则MmRn中m∶n=__________________(用含w1、w2、和a的代数式表示)。
23. (2008年广东卷)(12分)
某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色。一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理并说明理由 。
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3 mol·L-1H2SO4/3% H2O2、6 mol·L-1HNO3/0.01 mol·L-1KmnO4、NaOH稀溶液、0.1 mol·L-1Kl、20% KSCN、蒸馏水。
① 提出合理假设
假设1: ;
假设2: ;
假设3: 。
② 设计实验方案证明你的假设(不要在答题卡上作答)
③ 实验过程
根据②的实验方案,进行实验。请在答题卡上按下表格式写出实验操作步骤、预期现象与结论。
|
实验操作 |
预期现象与结论 |
|
步骤1: |
|
|
步骤2: |
|
|
步骤3: |
|
|
… |
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com