
题目列表(包括答案和解析)
6.(2004年全国)久置空气中会发生颜色变化,但颜色变化不是由于跟氧气反应引起的物质是( )
A.过氧化钠固体 B.亚硫酸钠固体 C.硫酸亚铁晶体 D.苯酚晶体
5.(2004年江苏卷)铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH物质的量之比为
A.1:1 B.2:1 C.3:1 D.1:3
4.(2004年广东卷)下列有碱金性铷(Rb)的叙述中,正确的是
A、灼烧氯化铷时,火焰有特殊颜色 B、硝酸铷是离子化合物,易溶于水
C、在钠、钾、铷三种单质中,铷的熔点最高 D、氢氧化铷是弱碱
3.(2004年北京春)在食品加工或餐饮业中使用量特别要注意严加控制的物质是
A.氯化钠 B.谷氨酸钠(味精)C.碳酸氢钠 D.亚硝酸钠
2. (2004上海卷)等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2物质的量之比为
A.3:4:1 B.3:3:2 C.6:7:3 D.6:9:0
1.(2004年全国)取a g某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了a g。下列物质中不能满足上述结果的是 ( )
A.H2 B.CO C.C6H12O6 D.C12H22O11
23.(08江苏卷)“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
⑴下列措施中,有利于降低大气中CO2浓度的有: 。(填字母)
a.减少化石燃料的使用 b.植树造林,增大植被面积
c.采用节能技术 d.利用太阳能、风能
⑵将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2 + 6H2O C6H12O6 b.CO2 + 3H2
C6H12O6 b.CO2 + 3H2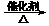 CH3OH +H2O
CH3OH +H2O
c.CO2 + CH4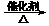 CH3COOH
d.2CO2 + 6H2
CH3COOH
d.2CO2 + 6H2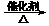 CH2==CH2 + 4H2O
CH2==CH2 + 4H2O
以上反应中,最节能的是 ,原子利用率最高的是 。
⑶文献报道某课题组利用CO2催化氢化制甲烷的研究过程如下:
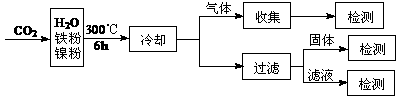
反应结束后,气体中检测到CH4和H2,滤液中检测到HCOOH,固体中检测到镍粉和Fe3O4。
CH4、HCOOH、H2的产量和镍粉用量的关系如下图所示(仅改变镍粉用量,其他条件不变):
研究人员根据实验结果得出结论:
HCOOH是CO2转化为CH4的中间体,
即:CO2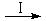 HCOOH
HCOOH CH4
CH4

①写出产生H2的反应方程式 。
②由图可知,镍粉是 。(填字母)
a.反应的催化剂
b.反应的催化剂
c.反应的催化剂
d.不是催化剂
③当镍粉用量从1mmol增加到10mmol,反应速率的变化情况是 。(填字母)
a.反应Ⅰ的速率增加,反应Ⅱ的速率不变
b.反应Ⅰ的速率不变,反应Ⅱ的速率增加
c.反应ⅠⅡ的速率均不变
d.反应ⅠⅡ的速率均增加,且反应Ⅰ的速率增加得快
e.反应ⅠⅡ的速率均增加,且反应Ⅱ的速率增加得快
f.反应Ⅰ的速率减小,反应Ⅱ的速率增加
22. (2008年广东卷)(11分)
硅单质及其化合物应用范围很广。请回答下列问题:
(1) 制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:

①写出由纯SiHCl3制备高纯硅的化学反应方程式 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式 ;H2还原SihCl3过程中若混02,可能引起的后果是 。
(2)下列有头硅材料的详法正确的是 (填字母)。
A.碳化硅化学性质稳定,可用于生产耐高温水混
B.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
C.普通玻璃是由纯碱、石灰石和石英砂的,其熔点很高
D.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
(3)硅酸钠水溶液俗称水玻璃。取少量硅酸钠溶液于试管中,逐滴加入饱和氯化铵溶液,振荡。写出实验现象并给予解释 。
21. (2008年全国I)(15分)V、W、X、Y、Z是由周期表中1-20号部分元素组成的5倍化合物,其中V、W、X、Z均为两种元素组成,上述5种化合物涉及的所有元素的原子序数之和等于35。它们之间的反应关系如下图: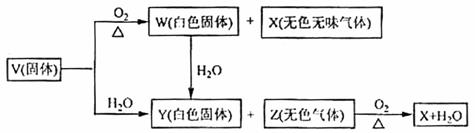
(1)5种化合物分别是V 、W 、X 、Y 、Z :(填化学式)
(2)由上述5种化合物中2种化合物反应可生成一种新化合物,它包含了5种化合物中的所有元素,生成该化合物的化学方程式是 :(3)V的电子式是 。
20.(15分)以下一些氧化物和单质之间可发生如右图所示的反应: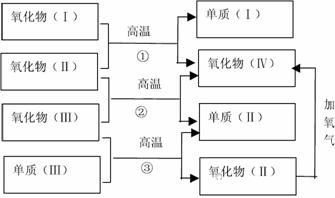
其中,氧化物(Ⅰ)是红棕色固体、氧化物(Ⅱ)、(Ⅲ)、(Ⅳ)在反应条件下都是气体。
(1)氧化物(Ⅰ)的化学式(分子式)是 。
氧化物(Ⅱ)的化学式(分子式)是 。
(2)反应①的化学方程式是 。
反应②的化学方程式是 。
反应③的化学方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com