
题目列表(包括答案和解析)
4. (08广东卷)某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水蒸气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。上述说法正确的是(
)
(08广东卷)某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水蒸气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。上述说法正确的是(
)
A.①②③④ B.①②⑤⑥
C.③⑤⑥⑦ D.①③④⑦
解析:1.显然正确;2.沼气属于↑↑可再生资源。水煤气由炽热的煤同水
蒸气反应制得,而煤为不再生资源,所以水煤气为不可再生资源,故
错误; 3.冰为固态水,干冰为固态CO2,均为纯净物和化合物,正确; 4.显然正确。 5.盐酸和食醋为混合物,不是化合物,错误; 6.纯碱为Na2CO3不是碱,错误; 7.豆浆和雾都能发生丁达尔现象,均属于胶体,正确。综上所述,选D。
3.(08上海卷)下列关于化学学习和研究的说法错误的是( )
A.化学模型有助于解释一些化学现象
B.质量守恒定律是大量实验事实的总结
C.化学家提出的假设都能被实验证实
D.化学基本原理的应用是有一定条件的
解析:化学家提出的假设只要是正确的,随着科学的发展可能被实验证实,也可能不能证实。
答案:C
2.(08上海卷)下列化学式既能表示物质的组成,又能表示物质的一个分子的是( )
A.NaOH B.SiO2 C.Fe D.C3H8
解析:NaOH是离子晶体,SiO2是原子晶体,Fe为金属晶体,它们均只表示物质的组成,不能表示物质的一个分子。答案:D
2008高考化学分类解析1-化学用语及其规律
1.(08上海卷)化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )

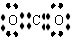
解析:CO2的中的C最外层上只有4个电子正确的电子式为: 。答案:B
18.(15分)(1)1、5、3、3、3、3
(2)①I2+SO32-+H2O===2I-+SO42-+2H+
②在步骤b后,增加操作:将分液漏斗充分振荡后静置
(3)①溶液由蓝色恰好变为无色②1.0×10-5③4.2 ×102/w
17.(18)
(1) BDE
(2)过滤 蒸馏
 (3)
(3)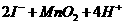
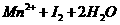
(4)苯与水互不相溶;碘在苯中的溶解度比在水中大
(5)取少量提取碘后的水溶液于试管中,加入几滴淀粉试液;观察是否出现蓝色(如果变蓝,说明还有单质碘)
16.(8 分)(1)①KI+IBr======KBr+I2
②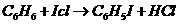 或
或 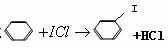
(2)相对分子质量越大,分子间作用力越强(3)介于Br2的沸点和IBr的沸点之间
15.(共9分)
(1)HCl(1分) Fe3O4(1分) FeCl3(1分)
(2)催化(1分) 氧化(1分)
(3)KClO3(1分) H2O2(1分)
(4)MnO2+4HCl(浓) MnCl2+C12↑+2H2O(2分)
MnCl2+C12↑+2H2O(2分)
12.解:AgNO3 + NaCl = AgCl↓+ Na NO3
n(AgNO3) = 0.100 mol·L-1×0.02 L = 0.002 mol
m (NaCl) = 0.002 mol×58.5 g·mol-1 = 0.117 g
V容器 = 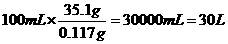
13:ⅠA,物理变化。585t。NaOH+SO3==NaHSO3 NaHSO3+HCl==NaCL+H2O+SO2 ↑。CD
14,答案(1)根据题意
n(HCl) = 12 mol/L×0.2 L = 2.4 mol
n(MnO2) = 17.4 g÷87 g/mol = 0.2 mol
MnO2 + 4 HCl(浓) △ MnCl2 + Cl2↑+ 2H2O
n(MnO2)∶n(HCl) = 2.4 mol∶0.2 mol = 12∶1 > 4∶1
所以浓HCl过量,应根据MnO2计算。
根据制备氯气的化学方程式
n(Cl\2) = n(MnO2) = 0.2 mol
又因为:2Cl2 + 2Ca(OH)2 = Ca(ClO)2 + CaCl2 + 2H2O
n[Ca(ClO)2] = 1/2 n(Cl2) = 1/2×0.2 mol = 0.1 mol
m[Ca(ClO)2] = 143 g/mol × 0.1 mol = 14.3 g
(2)①随着反应进行,温度升高,会产生副产物Ca(ClO3)2;
6Cl2 + 6Ca(OH)2 △ 5CaCl2 + Ca(ClO3)2 + 6H2O
②Cl2未与石灰乳完全反应,残余Cl2被NaOH溶液吸收
Cl2 + 2NaOH = NaCl + NaClO + H2O
11. (1) B E F
(2)将灰烬转移到烧杯中,加适量蒸馏水,用玻棒充分搅拌,煮沸,过滤
(3) D
(4) 过氧化氢是绿色氧化剂,在氧化过程中不引进杂质、不产生污染(不会进一步氧化单质碘)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com