
题目列表(包括答案和解析)
5.(08重庆卷)下列做法中用到物质氧化性的是( )
A.明矾净化水 B.纯碱除去油污
C.臭氧消毒餐具 D.食醋清洗水垢
解析:臭氧能够杀菌,是由于臭氧具有强氧化性,能使细菌结构被破坏。答案:C。
4.(08上海卷)已知在热的碱性溶液中,NaClO发生如下反应:3NaClO 2NaCl+NaClO3。在相同条件下NaClO2也能发生类似的反应,其最终产物是( )
2NaCl+NaClO3。在相同条件下NaClO2也能发生类似的反应,其最终产物是( )
A.NaCl、NaClO B.NaCl、NaClO3 C.NaClO、NaClO3 D.NaClO3、NaClO4
解析:在已知反应中氯元素的化合价:+1→+5和+1→-1,既然NaClO2也有类似的反应,即氯元素的化合价既有升高,也有降低,选项A中均降低;选项B、C与题意相符;选项D化合价均升高,但选项C中NaClO不是最终产物。答案:B
3.(08上海卷)下列物质中,只有氧化性、只有还原性,既有氧化性又有还原性的顺序排列的一组是( )
A.F2、K、HCl B.Cl2、Al、H2 C.NO2、Na、Br2 D.O2、SO2、H2O
解析:元素具有最高价时只有氧化性,注意F2没有最高化合价,元素具有最低化合价时只有还原性,而处于中间价态时既具有氧化性又具有还原性。答案:A
2.(08海南卷)锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为( )
A.2mol B.1 mol C.0.5mol D.0.25mol
解析:此题主要考查氧化还原反应的配平:Zn+HNO3(稀) Zn(NO3)2+NH4NO3+H2O,Zn:0→+2,化合价改变值为:(2-0)×1=2,N:+5→-3,化合价的改变值为:(5+3)×1=8,根据化合价升降总值相等得:在Zn(NO3)2前配4,NH4NO3前配1,然后根据反应前后各元素的原子个数相等,找出其他物质的系数。配平后的化学方程式为:4Zn+10HNO3(稀)===4Zn(NO3)2+NH4NO3+3H2O,当生成1mol的Zn(NO3)2时,被还原的HNO3为0.25mol。答案:D。
Zn(NO3)2+NH4NO3+H2O,Zn:0→+2,化合价改变值为:(2-0)×1=2,N:+5→-3,化合价的改变值为:(5+3)×1=8,根据化合价升降总值相等得:在Zn(NO3)2前配4,NH4NO3前配1,然后根据反应前后各元素的原子个数相等,找出其他物质的系数。配平后的化学方程式为:4Zn+10HNO3(稀)===4Zn(NO3)2+NH4NO3+3H2O,当生成1mol的Zn(NO3)2时,被还原的HNO3为0.25mol。答案:D。
1.(08全国Ⅱ卷)(NH4)2SO4在高温下分解,产物是SO2、H2O、N2和NH3。在该反应的化学方程式中,化学计量数由小到大的产物分子依次是( )
A.SO2、H2O、N2、NH3 B.N2、SO2、H2O、NH3
C.N2、SO2、NH3、H2O D.H2O、NH3、SO2、N2
解析:此题实际上是考查化学方程式的配平,(NH4)2SO4 NH3+N2+SO2+H2O,反应中:N:-3→0,化合价变化总数为6,S:+6→+4,化合价变化数为2,根据化合价升高和降低的总数相等,所以应在SO2前配3,(NH4)2SO4前面配3,NH3前面配4,H2O前面配6,最后计算反应前后的O原子个数相等。配平后的化学方程式为:3(NH4)2SO4
NH3+N2+SO2+H2O,反应中:N:-3→0,化合价变化总数为6,S:+6→+4,化合价变化数为2,根据化合价升高和降低的总数相等,所以应在SO2前配3,(NH4)2SO4前面配3,NH3前面配4,H2O前面配6,最后计算反应前后的O原子个数相等。配平后的化学方程式为:3(NH4)2SO4 4NH3↑+N2↑+3SO2↑+6H2O。答案:C。
4NH3↑+N2↑+3SO2↑+6H2O。答案:C。
18.(08江苏卷)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
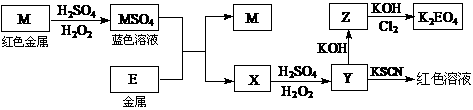
⑴写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
⑵某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式: 、 。
⑶写出Cl2将Z氧化为K2EO4的化学方程式: 。
 ⑷由E制备的E(C2H5)2的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为:
⑷由E制备的E(C2H5)2的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为: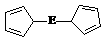 。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
答案:⑴Cu + H2O2 + H2SO4 == CuSO4 + 2H2O
⑵4Fe2+ + O2 + 4H+ == 4Fe3+ + 2H2O 2Fe3+ + 2I- == 2Fe2+ + I2
⑶10KOH + 3Cl2 + 2Fe(OH)3 == 2K2FeO4 + 6KCl + 8H2O
⑷1 3
2008高考化学分类解析3-氧化还原反应
17、(08宁夏卷)
某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
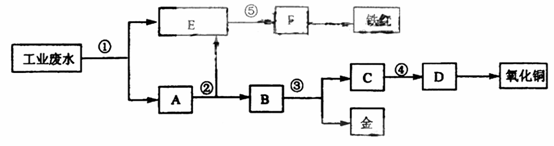
填写下面空白。
(1)图中标号处需加入的相应物质分别是① 、② 、③ 、④ 、⑤ 。
(2)写出①处发生反应的离子方程式 。写出③处发生反应的化学方程式 。
(3)铁红的化学式为 ;分别写出铁红和氧化铜在工业上的一种主要用途:铁红 ;氧化铜 。
答案:(1)①铁屑;②稀硫酸;③稀硝酸;④氢氧化钠;⑤氢氧化钠。
(2)Fe+2H+=Fe2++H2↑;2Fe3++Fe=3Fe2+。
Cu2++Fe=Cu+Fe2+ ;2Au3++3Fe=2Au+3Fe2+。
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(3)Fe2O3;用作红色涂料;用作制造铜盐的原料。
16.(广东理科基础30)下列反应的离子方程式正确的是
A.钠与水的反应:Na+H2O=Na++OH-+H2↑
B.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
C.氢氧化铝中和胃酸:Al(OH)3+3H+=Al3++3H2O
D.用FeCl3溶液腐蚀印刷电路板:Fe++Cu=Fe2++Cu2+
解析:钠与水的反应:Na+H2O=Na++OH-+H2↑H原子个数不平,故A错;氯气与水反应:Cl2+H2O=2H++Cl-+ClO-中HClO是弱酸,在离子方程式中不能拆,故B错;氢氧化铝中和胃酸:Al(OH)3+3H+=Al3++3H2O,C对;用FeCl3溶液腐蚀印刷电路板:Fe++Cu=Fe2++Cu2+电荷不等,故D错。答案C
15.(广东理科基础29).下列各组离子一定能大量共存的是
A.在含有大量[Al(OH)3]-的溶液中:NH4+、Na+、Cl-、H+
B.在强碱溶液中:Na+、K+、CO32-、NO3-
C.在pH=12的溶液中:NH4+、Na+、SO42-、Cl-
D.在c(H+)=0.1mol·L-1的溶液中:K+、I-、Cl-、NO3-
解析:含有大量Al(OH)3-的溶液中不可能含有H+,故A错;在强碱溶液中Na+、K+、CO32-、NO3-可以共存,故B对;在pH=12的溶液中含有OH-所以不能与NH4+共存,故C错;在c(H+)=0.1mol·L-1的溶液中含有大量的H+而在酸性溶液中NO3-具有强氧化性,I-具有强还原性,NO3-把I-氧化为碘单质,故D错. 答案B
14.(08四川卷)能正确表示下列反应的离子方程式是( )
A.足量的硫酸铝与纯碱反应:2Al3++3CO32-+3H2O===2Al(OH)3↓+3CO2↑
B.硫酸铜与烧碱反应:CuSO4+2OH-===Cu(OH)2↓+SO42-
C.苯酚与碳酸钠反应:2C6H5OH+CO32-===2C6H5O-+CO2↑+H2O
D.碳酸钡与硫酸反应:Ba2++SO42-===BaSO4↓
解析:选项B中CuSO4为溶于水的盐,可以改写;选项C中正确的离子方程式为C6H5OH+CO32-===C6H5O-+HCO3-;选项D中的BaCO3不能改写。答案:A。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com