
题目列表(包括答案和解析)
33.(东莞一模)中学化学教材中有大量数据,下列为某同学对数据的利用情况,其中不正确的是( )
A.用NaOH和HCl 反应测得的中和热,推算一定量稀H2SO4和NaOH 溶液反应的反应热
B.用沸点数据推测两种液体混合物用蒸馏方法分离开来的可能性
C.用沸点数据来分析分子的稳定性
D.用原子(或离子)半径数据推断某些原子(或离子)氧化性或还原性强弱
32.(东莞一模)旨在限制发达国家温室气体排放量、抑制全球范围内气候持续变暖的《京都议定书》随着俄罗斯的加入,将于2005年2月16日正式生效。我国二氧化碳的排放量位居世界第二,为减少二氧化碳这种温室气体的排放,下列措施不切实际的是( )
A.大力开发氢能源 B.充分利用太阳能
C.不使用含碳能源 D.提高能源利用率
18.(广东省肇庆一模)符合下列各种条件的溶液中,各组离子可能大量共存的是
A.滴加石蕊试液呈红色的溶液:K+、SO42-、NO3-、NH4+
B.25℃,pH=0的溶液中:Al3+、NH4+、NO3-、Fe2+
C.加入铝粉后能产生气体的溶液中:Cu2+、Ba2+、Cl-、NO3-
D.水电离出来的c(OH-)=10-13mol/L的溶液:K+、HCO3-、Br-、Ca2+
17.(广东省肇庆一模)下列有关反应热的叙述正确的是
A.已知2H2(g)+O2(g) 2H2O(g);△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol
B.C(s,石墨)=C(s,金刚石);△H=+1.9kJ·mol-1,说明金刚石比石墨稳定
C.X(g)+Y(g) Z(g)+W(s);△H>0,恒温恒容条件下达到平衡后加入X,
Z(g)+W(s);△H>0,恒温恒容条件下达到平衡后加入X,
上述反应的△H增大
D.已知C(s)+O2(g)=CO2(g);△H1 , C(s)+1/2O2(g)=CO(g);△H2,
则△H1<△H2
14.(广东省肇庆一模)下列说法中,正确的是( )
A.硫只能做还原剂
B.SO3只有氧化性,SO2只有还原性
C.置换反应一定是氧化还原反应
D.化合反应一定是非氧化还原反应
A.氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3+3H+=Fe3++3H2O
B.用醋酸除去水垢中的碳酸盐: 2CH3COOH+CO32- 2CH3COO-+H2O+CO2↑
2CH3COO-+H2O+CO2↑
C.氯化铵溶液中滴入烧碱稀溶液: NH4++OH-===NH3·H2O
D.NaHSO4溶液中滴加NaHCO3溶液:H+ + HCO3- == H2O + CO2↑
13.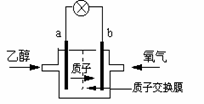 (广东省肇庆一模)一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍。电池总反应为:C2H5OH
+3O2= 2CO2 +3H2O,电池示意图如右下图。下面对这种电池的说法正确的是
(广东省肇庆一模)一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍。电池总反应为:C2H5OH
+3O2= 2CO2 +3H2O,电池示意图如右下图。下面对这种电池的说法正确的是
A.b极为电池的负极
B.电池工作时电子由a极沿导线经灯泡再到b极
C.电池正极的电极反应为:4H+ +O2 +4e- =2H2O
D.设每个电子所带电量为q库仑,则1mol乙醇被氧化产生6NAq库仑的电量
4.(广东省肇庆一模)将足量稀盐酸到加到下列固体混合物中,只能发生一种反应的是
A.Al、CuSO4、Na[Al(OH)4] B.NaClO、Na2SO3、BaCl2
C.KNO3、NaCl、NaHCO3 D.NaNO3、FeSO4、NH4HCO3
31.(广东省阳江市一模)我国采用长征三号甲运载火箭成功发射了 “嫦娥一号” 卫星。肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,反应生成N2和水蒸气。已知:
N2(g)+2O2(g)===N2O4(g) △H=+8.7kJ/mol
N2H4(g)+O2(g)==N2(g)+2H2O(g) △H= -534kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是
A.2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g) △H=–1076.7 kJ/mol
B.N2H4(g) + 1/2N2O4(g) =3/2N2(g) + 2H2O(g) △H=–542.7 kJ/mol
C.2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g) △H=–542.7 kJ/mol
D.2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(l) △H=–1059.3 kJ/mol
30.(广东省阳江市一模)常用的锌锰干电池在放电时总反应可表为:
Zn(s) + 2MnO2(s) + 2NH4+ = Zn2+ + Mn2O3 + 2NH3 + H2O
放电时负极区发生反应的物质或微粒是:
A.MnO2 B.MnO2和NH4+ C.Zn D.Zn2+和NH3
29.(广东省阳江市一模)下列各组离子中,一定能大量共存的是:
A.加入铝粉有氢气产生的溶液中:Na+、SO42-、C1-、K+
B.PH = 0的无色溶液中:Na+、K+、MnO4-、NO3-
C.在0.1mol/L的盐酸溶液中:Fe2+、Na+、ClO-、Ca2+
D.在c(H+)/c(OH-)= 1×1013的溶液中:NH4+、Ca2+、C1-、K+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com