
题目列表(包括答案和解析)
8.有五瓶溶液分别是:①10 mL 0.6 mol·L-1 NaOH水溶液;②20 mL 0.50 mol·L-1 H2SO4水溶液;③30 mL 0.40 mol·L-1 HCl水溶液;④40 mL 0.3 mol·L-1 CH3COOH水溶液;⑤50 mL 0.20 mol·L-1蔗糖水溶液。以上各瓶溶液所含离子、分子总数的大小顺序是
A.①>②>③>④>⑤
B.②>①>③>④>⑤
C.②>③>④>①>⑤
D.⑤>④>③>②>①
7.在无土栽培中,需配制一定量含50 mol NH4Cl,16 mol KCl和24 mol K2SO4的营养液。若用KCl、NH4Cl和(NH4)2SO4三种固体为原料来配制,三者的物质的量依次是(单位为mol)
A.2,64,24 B.64,2,24
C.32,50,12 D.16,50,24
6.已知甲、乙溶质质量分数与密度的关系如下表:
|
溶质质量分数 |
甲溶液密度(g/cm3) |
乙溶液密度(g/cm3) |
|
1% |
0.95 |
1.02 |
|
5% |
0.92 |
1.04 |
|
10% |
0.90 |
1.07 |
甲物质的1%的溶液与9%的溶液等体积混合,乙物质的1%的溶液与9%的溶液等体积混合后,下列叙述正确的是
A.混合后甲、乙溶液质量分数均大于5%
B.混合后乙溶液质量分数大于5%,甲溶液质量分数小于5%
C.混合后甲溶液质量分数大于5%,乙溶液质量分数小于5%
D.混合后甲、乙溶液质量分数均等于5%
5.设NA为阿伏加德罗常数,下列关于0.2 mol·L-1的Ba(NO3)2溶液不正确的说法是
A.2 L溶液中有阴、阳离子总数为0.8 NA
B.500 mL溶液中NO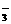 浓度为0.2 mol·L-1
浓度为0.2 mol·L-1
C.500 mL溶液中Ba2+浓度为0.2 mol·L-1
D.500 mL溶液中NO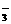 浓度为0.2 NA
浓度为0.2 NA
4.a mol氨完全氧化成HNO3,并且全部溶于反应生成的水中,得HNO3的质量分数约为
A.78% B.42% C.50% D.63%
3.在100 g浓度为18 mol·L-1,密度为ρ(g·cm-3)的浓硫酸中加入一定量的水稀释成9 mol·L-1的硫酸,则加入水的体积
A.小于100 mL B.等于100 mL
C.大于100 mL D.小于 mL
mL
2.以下各结论,错误的是
A.溶质的质量分数为30%的NaCl溶液,加入等质量的水稀释后,其溶质的质量分数为15%
B.物质的量浓度为10 mol·L-1的H2SO4溶液,用等体积的水稀释后,其物质的量浓度为5 mol·L-1
C.室温时,某物质在1 L水中最多能溶解0.09 g,此物质应属于“不溶物质”
D.常温常压下,1体积水约溶解700体积的氨气,这里氨气的体积,是指标准状况下的体积
1.20℃时,将某盐R的溶液蒸发掉10 g水后恢复到20℃,需再加6 g盐R(无水),溶液即达饱和,若将原溶液蒸发掉30 g 水,只需加1 g盐R就可在20℃时达饱和。则20℃时盐R的溶解度是
A.20 g B.25 g C.30 g D.35 g
25.(广东省深圳一模)(7 分 )水煤气 (主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s) + H2O(g) CO (g) +H2
(g);△H =+131.3kJ•mol-1
CO (g) +H2
(g);△H =+131.3kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
|
容器编号 |
c(H2O)/mol·L-1 |
c(CO)/mol·L-1 |
c(H2)/mol·L-1 |
V正、V逆比较 |
|
I |
0.06 |
0.60 |
0.10 |
V正=V逆 |
|
II |
0.06 |
0.50 |
0.40 |
? |
|
III |
0.12 |
0.40 |
0.80 |
V正<V逆 |
|
IV |
0.12 |
0.30 |
? |
V正=V逆 |
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气 (H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为 ;向该容器中补充 a mol 炭,水蒸气的转化率将 (填 “增大”、“减小”、“不变”),再补充 a mol 水蒸气 (H218O), 最终容器中C16O和C18O 的物质的量之比为 。
(3)己知:C (s) + 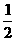 O2(g)=CO (g);△H = -110.5kJ·mo1-1
O2(g)=CO (g);△H = -110.5kJ·mo1-1
CO(g) + 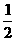 O2(g) =CO2 (g);△H =-283.0 kJ·mo1-1
O2(g) =CO2 (g);△H =-283.0 kJ·mo1-1
H2
(g) + 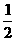 O2 (g) =H2O (g);△H = -241.8kJ·mo1-1
O2 (g) =H2O (g);△H = -241.8kJ·mo1-1
那么,将2.4 g 炭完全转化为水煤气,然后再燃烧,整个过程△H = kJ·mo1-1
25 (8分)
(1)(3分)
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V正 < V逆(1分) |
|
|
|
|
|
|
|
|
|
|
0.40(2分) |
|
(2)25%(1分);不变(1分);1:a(1分); (3)-78.7 (2分)
26、(12分) (1) Mo和S;形成酸雨(合理即得分)。(每空各 l 分)
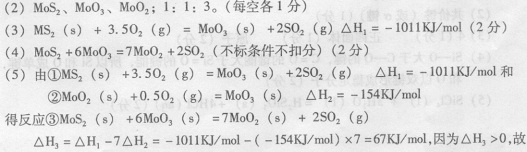 反应③是吸热反应,因其发生在中间层,故炉温降低。( 4 分)
反应③是吸热反应,因其发生在中间层,故炉温降低。( 4 分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com