
题目列表(包括答案和解析)
10.(12分)用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.1 mol·L-1的溶液 100 mL;②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;②分别取这两种溶液各10 mL,加水稀释为100 mL;③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)。
乙方案中,说明HA是弱电解质的现象是 (多选扣分)
a.装HCl溶液的试管中放出H2的速率快;
b.装HA溶液的试管中放出H2的速率快;
c.两个试管中产生气体速率一样快:
(3)请你评价乙方案中难以实现之处和不妥之处。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
9.在RNH2·H2O RNH
RNH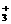 +OH-形成的平衡中,要使RNH2·H2O的电离程度及c(OH-)都增大,可采取的措施是
+OH-形成的平衡中,要使RNH2·H2O的电离程度及c(OH-)都增大,可采取的措施是
A.通入HCl B.加少量NaOH固体
C.加水 D.升温
8.当溶液中HS-+H2O S2-+H3O+达到平衡时,欲使c(S2-)增大,应加入
S2-+H3O+达到平衡时,欲使c(S2-)增大,应加入
A.Cu2+ B.CO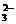
C.H2O D.HCl
7.下列各电离方程式中书写正确的是
A.CH3COOH H++CH3COO-
H++CH3COO-
B.KHSO4 K++H++SO
K++H++SO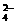
C.Al(OH)3 Al3++3OH-
Al3++3OH-
D.NaH2PO4 Na++H2PO
Na++H2PO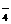
6.用水稀释0.1 mol·L-1氨水时,溶液中随着水量的增加而减小的是
A.c(OH-)/c(NH3·H2O)
B.c(NH3·H2O)/c(OH-)
C.c(H+)和c(OH-)的乘积
D.OH-的物质的量
5.甲酸的下列性质中可以证明它是弱电解质的是
A.1 mol·L-1的甲酸溶液的c(H+)约为0.01 mol·L-1
B.甲酸与水以任意比例互溶
C.10 mL 1 mol·L-1甲酸恰好与10 mL 1 mol·L-1NaOH溶液完全反应
D.在相同条件下,甲酸的导电性比一元强酸溶液的弱
4.在浓度均为1 mol·L-1的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2三种溶液中,若测得其中c(NH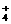 )分别为a、b、c(mol·L-1),则下列判断正确的是
)分别为a、b、c(mol·L-1),则下列判断正确的是
A.a=b=c B.c>a>b
C.b>a>c D.a>c>b
3.在无土栽培中,需配制一定量含50 mol NH4Cl,24 mol K2SO4的营养液。若用KCl,NH4Cl和(NH4)2SO4三种固体为原料来配制,三者的物质的量依次是(单位为mol)
A.2,64,24 B.48,2,24
C.32,50,12 D.16,50,24
2.当不考虑水的电离时,在氢硫酸溶液中,下列的离子浓度关系中正确的是
A.c(H+)=c(HS-)+2c(S2-)
B.c(H+)=c(HS-)+c(S2-)
C.2c(S2-)=c(H+)
D.c(S2-)=c(HS-)
1.(2001年全国高考题)在含有酚酞的0.1 mol·L-1氨水中加入少量的NH4Cl晶体,则溶液颜色
A.变蓝色 B.变深
C.变浅 D.不变
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com