
题目列表(包括答案和解析)
5.在一个固定容积的密闭容器中,保持一定温度进行如下反应:H2(g)+Br2(g) 2HBr(g),已知加入1
mol H2和2 mol Br2达到平衡后,生成了a mol HBr。在相同条件下,若起始时加入的H2、Br2、HBr分别为x mol、y mol、z
mol(均不为0)且保持平衡时,各组分含量都不变。以下推断中一定正确的是
2HBr(g),已知加入1
mol H2和2 mol Br2达到平衡后,生成了a mol HBr。在相同条件下,若起始时加入的H2、Br2、HBr分别为x mol、y mol、z
mol(均不为0)且保持平衡时,各组分含量都不变。以下推断中一定正确的是
①x,y,z应满足的关系为:4x+z=2y
②达到平衡时HBr的物质的量为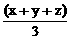 a mol
a mol
③达到平衡时HBr的物质的量为a mol
④x、y、z应满足的关系为x+y=z?
A.①② B.②③ C.③④ D.①②③
4.在一个容积为V L的密闭容器中放入2 L A(g)和1 L B(g),在一定条件下发生下列反应:
3A(g)+B(g)  nC(g)+2D(g)
nC(g)+2D(g)
达到平衡后,A物质的量浓度减少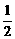 ,混合气体的平均摩尔质量增大
,混合气体的平均摩尔质量增大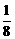 ,则该反应的化学方程式中n的值是
,则该反应的化学方程式中n的值是
A.1 B.2 C.3 D.4
3.在一定温度下的定容密闭容器中,当下列物理量不再改变时,表明反应:A(s)+2B(g)  C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.气体的总物质的量
2.(2001年全国理综题)在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是

A.反应的化学方程式为:2M N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
1.(2003年春季高考题)反应:A(g)+3B(g) 2C(g),ΔH<0达平衡后,将气体混合物的温度降低,下列叙述中正确的是
2C(g),ΔH<0达平衡后,将气体混合物的温度降低,下列叙述中正确的是
A.正反应速率加大,逆反应速率变小,平衡向正反应方向移动
B.正反应速率变小,逆反应速率加大,平衡向逆反应方向移动
C.正反应速率和逆反应速率都变小,平衡向正反应方向移动
D.正反应速率和逆反应速率都变小,平衡向逆反应方向移动
15.(6分)为测定人呼出气体中二氧化碳的含量,将1000 mL呼出的气体通入50.0 mL氢氧化钡溶液中,使其完全吸收,过滤后取20.0 mL澄清溶液,用0.100 mol·L-1盐酸滴定,当耗去20.4 mL盐酸时恰好完全反应。另取20.0 mL原氢氧化钡溶液,用同种盐酸滴定,耗去36.4 mL盐酸时,恰好反应完全。试计算人呼出气体中二氧化碳的体积百分含量(气体体积在标准状况下测定)。
14.(8分)在a、b两支试管中,分别装上形态相同、质量相等的一颗锌粒,然后向两支试管中分别加入相同物质的量、相同体积的稀盐酸和稀醋酸。填写下列空白:
(1)a、b两支试管中的现象:相同点是 ;不同点是 。原因是 。
(2)a、b两支试管中生成气体的体积开始时是a 于b,反应完毕后生成气体的总体积是a b,原因是 。
13.(8分)在稀氨水中存在平衡:NH3+H2O NH
NH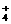 +OH-,如进行下列操作,则NH3、NH
+OH-,如进行下列操作,则NH3、NH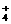 、H+、OH-浓度如何变化?试用“增大”“减小”“不变”填写。
、H+、OH-浓度如何变化?试用“增大”“减小”“不变”填写。
(1)通适量HCl气体时,c(NH3) ,c(H+) 。
(2)加入少量NaOH固体时,c(NH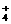 )
,c(OH-)
。
)
,c(OH-)
。
(3)加入NH4Cl晶体时,c(NH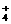 )
,c(OH-)
。
)
,c(OH-)
。
12.(12分)已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度大于第二步电离程度,第二步电离程度远大于第三步电离程度……
今有HA、H2B、H3C三种一元、二元、三元弱酸,根据“较强酸+较弱酸盐=较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:
①HA+HC2-(少量)===A-+H2C-
②H2B(少量)+2A-===B2-+2HA
③H2B(少量)+H2C-===HB-+H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中酸性最强的是 。
(2)A-、B2-、C3-、HB-、H2C-、HC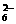 种离子中,最易结合质子的是
,最难结合质子的是
。
种离子中,最易结合质子的是
,最难结合质子的是
。
(3)判断下列反应的离子方程式中正确的是(填写标号) 。
A.H3C+3A-===3HA+C3-
B.HB-+A-===HA+B2-
C.H3C+B2-===HB-+H2C-
(4)完成下列反应的离子方程式。
A.H3C+OH-(过量) ;
B.HA(过量)+C3- 。
11.(9分)如下图,在一烧杯中盛有200 mL 0.1 mol·L-1的H3PO4溶液,同时一光滑小球悬浮在液体中间。
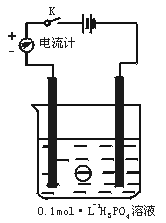
(1)合上电键K时,电流计指针向 边偏转。
(2)向烧杯里逐滴滴入0.4 mol·L-1的Ba(OH)2溶液至刚好完全反应,可观察到的现象有:
① ,② ,③ 。
(3)磷酸可用磷矿石[Ca3(PO4)2]来制取,写出该反应的化学方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com