
题目列表(包括答案和解析)
9.甲、乙、丙三种溶液各含有一种X-离子(X-为Cl-、Br-、I-),向甲中加淀粉和氯水,则溶液变为橙色,再加丙溶液,颜色无明显变化。则甲、乙、丙依次含有 B
A.Br-、Cl-、I- B.Br-、I-、Cl- C.I-、Br-、Cl- D.Cl-、I-、Br-
8.在甲、乙两烧杯溶液中,含有大量的Cu2+、Na+、H+、SO42-、CO32-、OH-等6种离子。已知甲烧杯的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是( B )
A.Cu2+、H+、SO42- B.Na+、OH-、CO32-
C.CO32-、OH-、SO42- D.Na+、H+、SO42-
7. 今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、
Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是 ( A )
A. K+一定存在 B. 100mL溶液中含0.01mol CO32-
C. Cl-一定存在 D. Ba2+一定不存在,Mg2+可能存在
6.某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断:该溶液中肯定不存在的离子组是A
A.Al3+、Mg2+、I-、SO32- B.Mg2+、Na+、CO32-、I-
C.Al3+、Na+、SO32-、I- D.Al3+、CO32-、Br-、SO32-
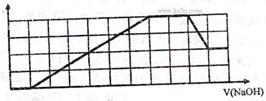
5.某溶液中可能含有H+、Na+、NH4+、Mg2+、
Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液
中加入一定物质的量浓度的NaOH溶液时,发
现生成沉淀物质的量随NaOH溶液的体积变
化的图象如右所示,下列说法正确的是 (C )
A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
B.原溶液中一定含有SO42-和Na+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D.反应最后形成的溶液中含有的溶质为Na2SO4
4、某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2─、MnO4─、CO32─、SO42─中的若干种组成。取该
溶液进行如下实验:⑴取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液;⑵ 在
⑴所得溶液中加入过量NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;⑶ 在⑵所得溶液
中加入过量Ba(OH)2溶液也有气体生成,同时析出白色沉淀乙。则下列离子在原溶液中一定
存在的有:B
A.SO42-、AlO2─、Na+ B.Na+、CO32─、AlO2─
 C.CO32─、Na+ 、Al3+ D.MnO4─、Na+、CO32─
C.CO32─、Na+ 、Al3+ D.MnO4─、Na+、CO32─
3.现有含NaCl、Na2SO4和NaNO3的混合溶液,采用下列实验流程加入适当的试剂将其转化为相应的沉淀或固体,实现Cl-、SO42-和NO3-的相互分离:
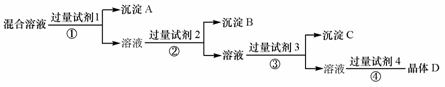
其中试剂1、2、4分别为A
A.氯化钡溶液 硝酸银溶液 稀硝酸
B.氯化钡溶液 稀硝酸 硝酸银溶液
C.氢氧化钠溶液 硝酸银溶液 稀硝酸
D.硝酸银溶液 硝酸钡溶液 稀硝酸
2.在甲、乙两烧杯溶液中,共含有Cu2+、K+、H+、Cl-、CO32-、OH-6种离子。已知甲烧杯的溶液含其中3种离子并呈蓝绿色,则乙烧杯的溶液中含有的另3种离子是C
A.Cu2+、H+、Cl- B.K+、CO32-、Cl-
C.K+、OH-、CO32- D.K+、H+、Cl-
1.某溶液中含有NO3-、SiO32-、AlO2-、S2-等四种离子,若向其中加入过量的盐酸溶液,微热并搅拌,再加入过量NaOH溶液,溶液中大量减少的阴离子是 ( D )
A.NO3- SiO32- B.SiO32- S2- C.AlO2- NO3- D.S2- NO3-
10. (1) 滤渣的主要成分为Mg(OH)2、Fe(OH)3、CaCO3。
(2) “趁热过滤”的原因是使析出的晶体为Na2CO3·H2O,防止因温度过低而析出Na2CO3·10H20晶体,令后续的加热脱水耗时长。
(3) 若在实验室进行“趁热过滤”,可采取的措施是用已预热的布氏漏斗趁热抽滤。
(4) 若“母液”循环使用,可能出现的问题及其原因是问题:溶解时有大量沉淀生成,使Na2CO3损耗且产物Na2CO3混有杂质;原因:“母液”中,含有的离子有Ca2+,Na+,Cl-,SO42-,OH-,CO32-,当多次循环后,使用离子浓度不断增大,溶解时会生成CaSO4,Ca(OH)2,CaCO3等沉淀。
(5) 写出Na2CO3·H2O脱水反应的热化学方程式
Na2CO3·H2O(S)==== Na2CO3(s) + H2O(g)&8710;H= +58.73kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com