
题目列表(包括答案和解析)
11.(10分) (1)CO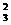
 AlO
AlO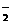 (2)NO
(2)NO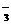 (3)Mg2+ Al3+
(3)Mg2+ Al3+
(4)Ba2+
, SO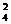
 (5)H+、I-、Ba2+; NH4+。
(5)H+、I-、Ba2+; NH4+。
11.(10分)
有一瓶澄清的溶液,其中可能含有H+、NH4+、Mg2+、Ba2+、Al3+、I-、NO3-、CO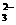 、SO
、SO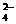 、AlO
、AlO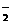 ,取该溶液进行以下实验:
,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈酸性,可以排除 的存在。
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4呈紫红色,可以排除 的存在。
(3)另取出部分溶液逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,反应过程中均无沉淀产生,则又可排除 的存在。
(4)取出部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成,证明有 的存在,又可以排除 的存在。
(5)根据上述实验事实可以确定,该溶液中肯定存在的离子是 ,还不能确定是否存在的离子是 。
10.(13分)(2) 乙
|
|
选用试剂 |
实验现象 |
|
第一种方法 |
C |
有机层无色 |
|
第二种方法 |
D |
溶液变红 |
(3)①不可行,因为Br2和Fe3+都能把I- 氧化成I2
10.(13分) 在足量的稀氯化亚铁溶液中加入1-2滴液溴,振荡后溶液变为黄色。
(1)甲同学认为是Br2溶于水变成黄色溶液; 乙认为是Fe2+被氧化成Fe3+使溶液变成黄色。
(2)现提供试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
请判断 (填“甲”或“乙”)的推断正确,并用两种方法加以验证,写出选用的试剂编号及实验中观察到的现象:
|
|
选用试剂 |
实验现象 |
|
第一种方法 |
|
|
|
第二种方法 |
|
|
(3)若选用淀粉碘化钾溶液判断哪位同学的推断正确,是否可行?(填“可行”或“不可行”): ;理由: 。
9.(1)①HCO3-和SO32-可能存在,因为它们水解呈碱性。
②HCO3-不存在,因为滴加新制氯水没有气体产生。Br-存在,因为有溴的四氯化碳溶液颜色出现橙色。同时肯定存在SO32-。
③分液后的溶液中含有SO42-,可以是SO32-被氯水氧化生成的,不能说明原溶液中含有SO42-。
④Cl-不能判断,因为Cl-可能是原来溶液就有的,也有可能是加入氯水带来的。
(2)存在Na+ SO32- Br- 不能确定SO42- Cl-
9.(12分)某溶液中存在Na+、SO42-、SO32-、Cl-、HCO3-、Br-中的若干种,依次进行下列实,观察到现象记录如下。
①用pH试纸检验,溶液的pH>7;
②向溶液中滴加新制氯水,无气体产生,加入四氯化碳振荡、静置,四氯化碳层呈橙色,用分液漏斗分液;
③向分液后所得的水溶液中加入硝酸钡和稀硝酸的混合液,只有白色沉淀产生,过滤;
④在滤液中加入硝酸银和稀硝酸的混合液,有白色沉淀产生。
(1)分析上述5个实验,写出每一实验鉴定离子的结论与理由。
实验①_______________________。
实验②______________________________。
实验③_______________________。
实验④______________________________。
(2)结论:一定存在的离子__________________,不能确定的离子____________。
8.(5分)(每空1分)
(1)Cu2+ (2)Cl-、Ag++Cl-==AgCl↓ (3)Mg2+ (4)B
8、(5分)某无色透明溶液中可能大量存在Ag+,Mg2+,Cu2+中的几种离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是_________。
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定有的离子是___________,有关的离子反应式为______________。
(3)取(2)的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子有_______________。
(4)原溶液中可能大量存在的阴离子是下列A-D中的(填序号)_________。
A.Cl- B.NO3- C.CO32- D.OH-
7.为确定某溶液的离子组成,分别进行如下实验:
①测定溶液的pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。根据实验以下推测正确的是 B
A.一定有SO32-离子 B.一定有CO32-离子
C.一定有C1-离子存在 D.不能确定HCO3-离子是否存在
6、有一无色溶液,可能含有K+、Al3+、Mg2+、NH4+、Cl-、S O42- 、HCO3-、Mn O4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2 O2固体,产生无色无味的气味和白色沉淀,再加入足量的N a OH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是(C )
A、肯定有Al3+、Mg2+、NH4+、Cl- B、可能有K+、Cl-、Mn O4-
C、肯定有Al3+、Mg2+、S O42- D、肯定有K+、HCO3-、Mn O4-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com