
题目列表(包括答案和解析)
28.(Ⅰ)(6分)采用惰性电极从NO3-、SO42-、Cl-、Cu2+、Ba2+、H+中选出适当的离子组成电解质,并对其溶液进行电解(少写多写均不得分)。
(1)若两极分别放出H2和O2,则电解质的化学式为 ;
(2)若阴极析出金属,阳极放出O2,则电解质的化学式为 ;
(3)若两极分别放出气体,且体积比为1:1,则电解质的化学式为 。
27、(5分)( 4×l0-3 mol / L)
0.064 g(设电解时该电极无氢气析出,且不考虑水解和溶液体积变化)。计算此时溶液中氢离子浓度
约为多少?
27、(5分)将两个铂电极插入500 mL CuSO4溶液中进行电解,通电一定时间后,某一电极增重
26.(10分)(1)+1、+2 (1分,不写“+”不得分) Cu2O (2分)
(2)2H++2e-=H2↑ (或2H2O+2e-=H2↑+2OH- ) (1分)
Cu+Cl-- e-=CuCl↓ (2分)(不写“↓”不扣分)
(仅答 Cu- e-=Cu+ 或 Cu+OH-- e-=CuOH↓给1分)
(3)①:3Cu2O + 14H+ + 2NO3- = 6Cu2+ + 2NO↑ + 7H2O (2分)
②:Cu2O + 2H+ = Cu + Cu2+ + H2O (2分)
26.(10分)某化学研究小组以铜为电极电解饱和食盐水,探究过程如下:
 [实验1]:如右下图装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细。电解开始30s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10。随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,溶液始终未出现蓝色。
[实验1]:如右下图装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细。电解开始30s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10。随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,溶液始终未出现蓝色。
[实验2]:将实验1中试管底部的橙黄色沉淀取出,分装在两支小试管中,以后的操作和现象如下:
|
序号 |
操 作 |
现 象 |
|
① |
滴入稀硝酸溶液 |
沉淀溶解,有无色气泡产生,最终得到蓝色溶液。 |
|
② |
滴入稀硫酸溶液 |
橙黄色沉淀转变为紫红色不溶物,溶液呈现蓝色 |
[有关资料]常见铜的化合物颜色如下:
|
物质 |
颜 色 |
物质 |
颜 色 |
|
氯化铜 |
固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 |
氢氧化亚铜 (不稳定) |
橙黄色 |
|
碱式氯化铜 |
绿色 |
氢氧化铜 |
蓝色 |
|
氧化亚铜 |
砖红色或橙黄色 |
氯化亚铜 |
白色 |
请回答下列问题:
(1)铜的常见正化合价为 、 ,最终试管底部橙黄色沉淀的化学式
(2)阴极上发生的反应为:
阳极上发生的反应为:
(3)写出实验2中①、②的离子方程式
①
②
25、(重庆卷12)如题12图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是B
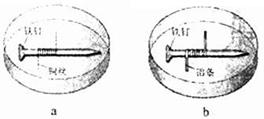 A.a中铁钉附近呈现红色
A.a中铁钉附近呈现红色
B.b中铁钉上发生还原反应
C.a中铜丝上发生氧化反应
D.b中铝条附近有气泡产生
24、(天津卷12.)下列叙述正确的是C A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应 B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1∶2
C.用惰性电极电解饱和NaCl溶液,若有1 lmol电子转移,则生成1 mol NaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
23、(宁夏卷10.)一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳。 该电池负极发生的反应是C
A.CH3OH(g)+O2(g)=H2O(1)+CO2(g)+2H+(aq)+2e_
B.P2(g)+4H+(aq)+4e_=2H2C(1)
C.CH3OH(g)+H2O(1)=CO2(g)+6H+(aq)+6e_
D.O2(g)+2H2O(1)+4e_=4OH
22、(北京卷5)据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供腺务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是D
A. 正极反应式为:O3+2H2O+4e-=4OH-
B. 工作一段时间后,电解液中KOH的物质的量不变
C. 该燃料电池的总反应方程式为:2H2+O2=2H2O
D. 用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com