
题目列表(包括答案和解析)
3.如图所示,四个装置中电极反应式相同的一组是B ( )

A.①⑦ B.②⑥ C.③④ D.⑤⑧
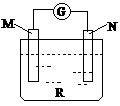
2.如右图:电流计的指针会偏转,M极变粗,
N极变细符合这种情况的是 ( C)
 A.M是铜,N是锌,R是硫酸溶液
A.M是铜,N是锌,R是硫酸溶液
B.M是锌,N是铜,R是硫酸铜溶液
C.M是银,N是锌,R是硝酸银溶液
D.M是铁,N是铜,R是硝酸铜溶液
1. 1L0.1mol/LAgNO3溶液在以Fe作阳极,Ag作阴极的电解槽中电解,当阴极增重2.16g时,下列判断正确的是(设电解按理论进行,溶液不蒸发) ( C )
A.溶液的浓度不变 B.阳极上产生112mLO2(标准状况)
C.转移的电子数是1.204×1022个 D.反应中有0.02mol的Ag+被氧化
31.负极;CH3OH-6e-+H2O=CO2+6H+
本资料由《七彩教育网》 提供!
31.下图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图。甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O。则c电极是 (填“正极”或“负极”),c电极上发生的电极反应是 。

30.(14分)
(1)Fe;Fe-2e-=Fe2+;
(2)(B)、(C)
(3)隔离空气 ②
(4)(B)、(C)
(5)白色沉淀迅速变为灰绿色,最后变为红褐色。
30.(14分)由于Ca(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色
纯净的Fe(OH)2沉淀。用如图所示电解实验可制得的白色纯净的Fe(OH)2沉淀。两电极
 的材料分别为石墨和铁。
的材料分别为石墨和铁。
(1)a电极材料应为 ,电极反应式为 。
(2)电解液c可以是(填编号) 。
A.纯水 B.NaCl溶液
C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为 ,在加入苯之前对c溶液作何简单处理 (填编号)
①加入冰块降温处理 ②将c溶液加热煮沸处理 ③将c溶液无限稀释
(4)为了在较短时间内看到白色沉淀,可采取的措施 (填编号)
A.改用稀硫酸作电解液 B.适当增大电源的电流
C.适当减少两电极间距离 D.适当降低电解液的温度
(5)若c为Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,沉淀物的另一明显现象为 。
29.①2Cl- -2e-==Cl2↑(2分) 2H++2e-==H2↑(2分)
②HCO3- +OH-==CO32-+H2O(2分)
29.(6分)用惰性电极电解NaCl与NaHCO3混合溶液,测得
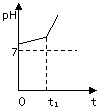 溶液pH变化如下图所示。
溶液pH变化如下图所示。
① 在0→t1时间内,两个电极上的电极反应式为:
阳极 ;
阴极 。
②用离子方程式表明0→t1时间内,溶液pH升高比较缓
慢的原因:
。
28.(Ⅰ)(6分)(1)Ba(NO3)2 HNO3 H2SO4;(2)CuSO4 Cu(NO3)2;(3)HCl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com