
题目列表(包括答案和解析)
13.(14分)
A、B、 C、 D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们
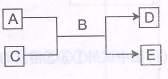 之间有如下的反应关系:
之间有如下的反应关系:
(1)常温下,若A为气态单质,C为非金属氧化物,A、C均能使
品红溶液褪色,相对分子质量E>D,则该反应的反应方程
式为: ,检验D中 阴离子所用试剂为: 。
(2)若A为短周期的金属单质,D为气态单质,C溶液呈酸性或强碱性时,该反应都能进行。
写出反应的离子方程式: 、
。(3)若A、C均为化合物,E为白色沉淀,C为引起温室效应的主要气体,写出E可能的物质
的化学式(写两种) , 。写出生成E的一个离子方程式:
。
12.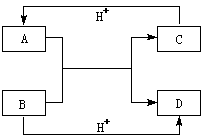 已知A、B、C、D是中学化学中常见的四种不同的微粒。他们之间存在如下转化关系:
已知A、B、C、D是中学化学中常见的四种不同的微粒。他们之间存在如下转化关系:
(1)如果A、B、C、D均是含10个电子的粒子,请写出:
A的结构式_______________________________,
D的电子式_____________。
(2)如果A和C是含18个电子的粒子,B和D是含10个电子的粒子,请写出:
①A与B在溶液中反应的离子方程式_______________________________________。
②根据上述离子方程式,可判断C与B结合质子的能力大小是(用化学式或离子符号表示)_____________________________________。
(3)已知肼(H2N-NH2)和甲胺(H2N-CH3)都是含有18个电子的分子。分析肼和甲胺的结构特点并从中受到启发,写出其具有相同电子数的有机化合物的结构简式(至少写两个)______________________________________________________________________。
11. (14分)W是一种正盐,X、A、E都是中学化学中学过的气体,同温同压下,A、E的密度比为2 :1,D、H是强酸。据以下转变关系回答问题。
(14分)W是一种正盐,X、A、E都是中学化学中学过的气体,同温同压下,A、E的密度比为2 :1,D、H是强酸。据以下转变关系回答问题。
(1)写出下列物质的化学式:
W__________、 X___________、 A__________ 、 E_________
(2)W与NaOH溶液反应的离子反应方程式:
__________________________________________________________
(3)E → F反应的化学方程式:
__________________________________________________________
10.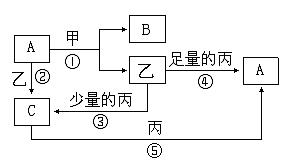 (12分)甲、乙、丙是三种常见的单质;A、B、C均是由两种元素组成中学化学中常见的无机物;上述物质间存在如下图所示转化关系(反应条件未注明)。
(12分)甲、乙、丙是三种常见的单质;A、B、C均是由两种元素组成中学化学中常见的无机物;上述物质间存在如下图所示转化关系(反应条件未注明)。
回答下列问题:
(1)若反应①中甲是常见金属,乙是常见非金属固态单质,则A的结构式是 ,B的电子式是 ,C在日常生活中的用途是 。
(2)若反应①中甲是常见非金属气态单质,丙是常见金属,甲由短周期元素组成,乙与甲同主族、与丙同周期,且反应①、②、⑤通常在溶液中进行。请写出下列化学反应的离子方程式:
反应①: ;
反应②: ;
反应⑤: 。
9.(11分)
 右图所示物质转化中,常温下E为无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)。
右图所示物质转化中,常温下E为无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)。
回答下列问题:
(1)在反应②中,每生成2.24L气体G(标准状况)时,该反应转移电子的物质的量是 ;
(2)若反应①在加热条件下进行,且C、D是两种均能使澄清石灰水变浑浊的无色气体,则反应①的化学方程式是 ;
(3)若反应①在溶液中进行,A是一种强碱,B是一种酸式盐,D是一种气体,且B遇盐酸有气体产生。在加热条件下,当A过量时反应①的离子方程式是 ;
(4)若反应①在溶液中进行,A是一种强酸,B是一种含有两种金属元素的盐,且B的水溶液显碱性,A、B均由短周期元素构成。则A过量时反应①的化学方程式是 。
8.(10分)室温下,单质A、B、C分别为固体、黄绿色气体与无色气体,在合适条件下,它们可以按下面的流程进行反应。又知E溶液是无色的。请回答:

(1)写出下列物质的化学式:
A 、B 、C 。
(2)写出G→H的化学方程式 。
(3)写出B+F→D的离子方程式 。
7.
 (8分)右图中所涉及的物质均为中学化学中的常见物质,其中C为单质,且为空气的主要成分之一;D为黄绿色气体;E为日常生活中应用最广泛的金属单质之一,其余为化合物。它们存在如图所示的转化关系,反应中生成的水及次要产物均已略去。
(8分)右图中所涉及的物质均为中学化学中的常见物质,其中C为单质,且为空气的主要成分之一;D为黄绿色气体;E为日常生活中应用最广泛的金属单质之一,其余为化合物。它们存在如图所示的转化关系,反应中生成的水及次要产物均已略去。
(1)指出MnO2在相关反应中的作用:反应①中是 剂,反应②中是 剂。
(2)若反应①是在加热条件下进行,则A是 ;若反应①是在常温条件下进行,则A是 。
(3)写出B与MnO2共热获得D的化学方程式 。
(4)写出B与F反应的离子方程式 。
6.(11分)下图为中学化学中几种常见物质的转化关系(部分产物已略去)。已知:A、C是气体单质,B为金属;气体E极易溶于水、液态常做致冷剂。D为黑色固体,H的固体受热分解生成两种气体E和y,y的组成元素均为短周期元素。
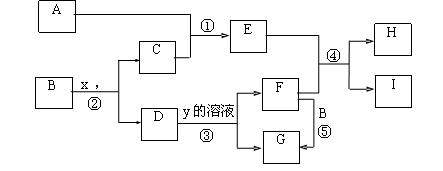
(1)写出:G的化学式 ,y的电子式 ;
(2)反应②的化学方程式为 ,
反应④的离子方程式为 ;
(3)鉴定H中阳离子的实验方法和现象 。
5.(14分)A、B、C、D、E均为中学化学常见物质,它们之间的反应关系如图所示:

(1)若A是短周期原子半径最大的元素(稀有气体除外)构成的单质,E既可溶于盐酸又可溶于NaOH溶液,则E溶于NaOH溶液的离子方程式为 ;工业上冶炼A的化学反应方程式为 ;气体C在使用前需要检验纯度,操作方法是 。
(2)若C是一种四原子分子,燃烧时有浓烈的黑烟,且A与B的溶液反应时只生成气体C、CaCO3和H2O。C的电子式为 ;B的名称为 ;实验室制取C的化学反应方程式为 ;C的燃烧热为1300kJ·mol-1,则C燃烧的热化学方程式为 。
4、(12分 )现有A、B、C三种白色固体及一种无色气体D。A、B、C均可溶于水,其中C的溶液为碱溶液,焰色反应均呈黄色,且四种物质中间存在如下反应关系:
① ②
②
③ ④
④
试推断:A是 B是
C是 D是 。 (写化学式)
写出③ 的化学方程式:
的化学方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com