
题目列表(包括答案和解析)
4.下列各图所示装置的气密性检查中,一定漏气的是 D

3.已知外电路中,电子由铜流向a极。有关下图所示的装置分析合理的一项是( B )
 A.该装之中Cu极为正极
A.该装之中Cu极为正极
B.当铜片的质量变化为12.8g时,
a极上消耗的O2在标准状况下
的体积为2.24L
C.b极的电极反应式:H2-2e-=2H+
D.一段时间后锌片质量减少
2.下列实验操作中所用仪器合理的是 A
A.用25mL的碱式滴定管量取14.80mLNaOH溶液
B.用100mL量筒量取5.2mL盐酸
C.用托盘天平称取25.20g氯化钠
D.用100mL容量瓶配制 盐酸
盐酸
1.下列实验方案合理的是B
A.向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体
B.测定工业烧碱的含量(含杂质碳酸钠)可称取一定量样品放入锥形瓶中,加适量水溶解,再加入稍过量氯化钡溶液,用酚酞作指示剂,用标准浓度的盐酸滴定
C.用分液漏斗分离苯与硝基苯
D.用蒸馏的方法分离乙醇和乙酸
21.(共20分,每空2分)
(1)防倒吸
(2)2H2S + O2 == 2S ↓ + 2 H2O
(3)溶液由无色变成蓝色;
I2 +5Cl2+6H2O ===12H++2IO3- + 10Cl-
(4)产生白色沉淀 Al3++3NH3.H2O === Al(OH)3 ↓+ 3NH4+
(5)AL 溶液由无色变成红色
(6)C 溶液由浑浊变澄清
本资料由《七彩教育网》 提供!
21. (20分)用如图所示装置进行实验,将液体A逐滴加入到固体B中,回答下列问题:
(20分)用如图所示装置进行实验,将液体A逐滴加入到固体B中,回答下列问题:
⑴图中D装置在实验中的作用是 。
⑵若 A为30%H2O2溶液,B为MnO2 ,C盛有氢硫酸(H2S)饱和溶液,旋开E后,C中出现浅黄色浑浊的现象,写出C中发生反应的化学方程式为 。
⑶若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开E后,C中的现是 ;继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3,写出该反应的离子反应方程式 。
⑷若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是 ,C中发生反应的离子方程式为 。
⑸若A为浓H2SO4,B为第三周期金属元素组成的片状金属单质,它在常温下难与水反应,C为品红溶液,实验中观察到溶液红色褪去,则B为__________;然后向烧杯中注入沸水,又可观察到的现象是 。
⑹若B为块状大理石,C为C6H5ONa溶液,实验中观察到溶液变浑浊,则
①酸A不宜用下列的________。
A.HCl B.HNO3 C.H2SO4 D.CH3COOH
②然后向烧杯中加入沸水,可观察到的现象是 。
20.(共6分,每个现象、方程式各1分)
e:氯酸钾与浓盐酸反应产生黄绿色气体 ClO3-+6H++5Cl-=3Cl2↑+3H2O
a:无色溴化钾溶液渐变成黄色 2Br-+Cl2=2Cl-+Br2
c:氢氧化钠酚酞溶液的红色渐渐褪去 2OH-+Cl2=Cl-+ClO-+H2O
20. (6分)为了减少污染,使实验绿色化,学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeSO4(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如右图所示),在圆心处放置2粒芝麻大小的KClO3晶体,盖好表面皿。
(6分)为了减少污染,使实验绿色化,学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeSO4(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如右图所示),在圆心处放置2粒芝麻大小的KClO3晶体,盖好表面皿。
打开表面皿,向KClO3晶体滴加一滴浓盐
酸,再立即将表面皿盖好,试描述各处反应
的现象,并写出相应的离子反应方程式。
e处:
a处:
c处:
19.(共9分)
(1)NO2 (3分)
(2)比较碳酸、醋酸、硅酸的酸性强弱;(3分)B中固体溶解,产生无色气体,C试管中产生白色沉淀(3分)。
19.(9分)某兴趣小组同学共同设计了如图所示的多功能实验装置。该装置既可用于制取气体,又可用于验证物质的性质。
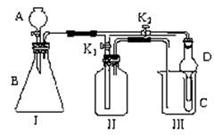
(1)现有以下药品:锌粒、铜片、浓H2SO4、浓HNO3、蒸馏水、NaOH溶液。打开K1关闭K2,可制取 气体。
(2)某同学用石灰石、醋酸、硅酸钠溶液等药品设计了另一实验。他的实验目的是__________________________________________________;打开K2关闭K1,将A中液体加入B中后,观察到的实验现象为___________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com