
题目列表(包括答案和解析)
13.Na3N是离子化合物,它能与水反应生成氨气。下列关于Na3N的说法中不正确的是
A.Na3N与盐酸反应时可生成两种盐
B.在Na3N与水的反应中Na3N是还原剂
C.在Na3N晶体中Na+的半径比N3-的半径大
D.Na+与N3-的电子层结构都与氖原子相同
12.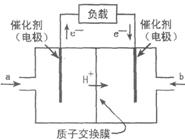 右图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为: 2CH3OH+3O2=====2CO2+4H2O
右图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为: 2CH3OH+3O2=====2CO2+4H2O
下列说法正确的是
A.右电极为电池的正极,b处通人的物质是空气
B.左电极为电池的负极,a处通入的物质是空气
C.负极反应式为:CH3OH+H2O-6e-=====CO2+6H+
D.正极反应式为:O2+4e-====2O2-
11.下列离子方程式中不正确的是
A.碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
B.用Pt电极电解MgCl2溶液2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.碳酸氢钠溶液与硫酸氢钠溶液反应HCO3-+H+=CO2↑+H2O
D.氯化铵与氢氧化钠两种浓溶液混合加热:NH4++OH- H2O+NH3↑
H2O+NH3↑
10.由于碘是卤素中原子半径较大的元素,可能呈现金属性。下列事实最能够说明这个结论的是
A.已经制得IBr、ICl等卤素互化物 B.已经制得I2O5等碘的氧化物
C.已经制得I(NO3)3、I(ClO4)3﹒2H2O等含I3+离子化合物
D.碘(I2)易溶于KI等碘化物溶液,形成I3-离子
9.设NA表示阿伏加德罗常数,下列说法中不正确的是
A.一定量的Fe与含1molHNO3的稀硝酸恰好反应,如还原产物为NO,则被还原的氮原子数小于NA
B.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
C.常温常压下,NA个臭氧分子的体积大于22.4L
D.1.8g水中含有的电子总数为NA
8、断裂一个给定的键时所消耗的能量称为离解能,提供下列烷烃的C-H键的离解能:
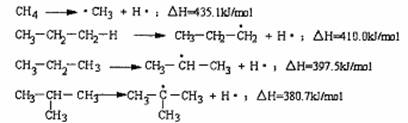
根据提供数据判断下列说法不正确的是
A、离解能愈小,C-H键易断裂,氢原子越易被取代
B、在光照条件下丙烷与氯气发生取代反应CH3CH2CH2Cl与CH3CHClCH3的物质的量之比为1:1
C、异丁烷与氯气发生取代反应,(CH3)3CCl占一氯代物的物质的量分数大于105
D、C2H6中C-H的离解能介于410.0 kJ /mol~435.1kJ/mol
7、用NA表示阿伏加德罗常数,下列说法正确是
A、每molFeS2在沸腾炉中完全燃烧,转移44NA个电子
B、标准状况下B2H6和C2H4的混合气体22.4L,所含电子数约为16NA
C、138.8gNa2SO4与Na2SO3的混合物,若含1mol硫原子,则含3.5NA个氧原子
D、1LPH=9的CH3COONa溶液中,由水电离出的氢离子数为10-9NA个
6、下列各组离子在指定条件下,一定能大量共存的是
A、能使红色石蕊试纸显蓝色的溶液:K+、Fe2+、SO42-、NO3-、Cl-
B、能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br-
C、水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、NO3-、Cl-
D、加入铝条有氢气放出的溶液:Na+、NH4+、HCO3-、NO3-
5、下列实验方案设计正确的是
A、分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤
B、失去标签的硝酸银溶液、稀盐酸、氢氧化钠溶液、氯化铝溶液可选用碳酸铵溶液作鉴别试剂
C、用铜丝代替铂丝做焰色反应
D、在裂化汽油中加入酸性高锰酸钾、振荡后若紫色褪去即可证明其中含甲苯等苯的同系物
4、桶烯(Barrelene)结构简式如右图所示,有关说法不正确的是
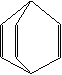 A、桶烯分子中所有的原子在同一平面内
A、桶烯分子中所有的原子在同一平面内
B、桶烯在一定条件下能发生加聚反应
C、桶烯与苯乙烯(C6H5CH=CH2)互为同分异构体
D、桶烯中的一个氢原子被氯原子取代,所得产物只有两种
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com