
题目列表(包括答案和解析)
1.化学与生活是紧密相联的,下列关于生活与化学的说法正确的是
A.随着人们生活节奏的加快,方便的小包装食品已被广泛接受,为了防止中秋月饼等富脂食品氧化变质,延长食品的保质期,在包装袋中常放入生石灰
B.现在用的清洁燃料主要有两类:一类是压缩天然气,另一类为液化石油气,它们属于碳氢化合物
C.福尔马林是一种良好的杀毒剂,也可用来消毒自来水
D.保护加酶洗衣粉的洗涤效果,应用沸水溶解洗衣粉
12. 1,3 ―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:
CH2=CH2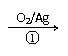

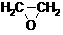
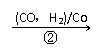
 HOCH2CH2CHO
HOCH2CH2CHO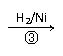
 HOCH2CH2CH2OH
HOCH2CH2CH2OH
⑴通过反应①用乙烯和空气混合气体制备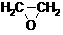 ,测得反应前和某一时刻气体的体积分数如下表。
,测得反应前和某一时刻气体的体积分数如下表。
|
|
C2H4 |
O2 |
N2 |
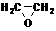 |
|
反应前体积分数 |
25.0% |
15.0% |
60.0% |
0 |
|
某一时刻体积分数 |
5.56% |
5.54% |
66.7% |
22.2% |
计算此时乙烯的转化率。
⑵某化工厂已购得乙烯14t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O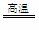 CO+H2 CH4+H2O
CO+H2 CH4+H2O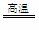 CO+3H2
CO+3H2
假设在生产过程中,反应②中CO和H2、反应③中H2均过量20%,且反应①、②、③中各有机物的转化率均为100%。
计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
11.为测定某工厂排放的污水中苯酚的含量,进行如下实验:取污水试样10.00mL加水稀释至100mL,加入10.0mL一定浓度的KBrO3和KBr的混合溶液,立即加入5mL盐酸,摇匀后加入1gKI固体(足量),再摇匀,放置5min。用0.01000mol/LNa2S2O3标准溶液滴定至淡黄色,加入1mL淀粉溶液,继续滴定至蓝色刚好褪去,用去Na2S2O3标准溶液14.46mL。同时以水代替污水试样做对比实验,用去Na2S2O3标准溶液38.46 mL。
⑴已知上述实验中发生的反应有:
KBrO3+5KBr+6HCl=3Br2+3H2O+6KCl
2Na2S2O3+I2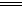 Na2S4O6+2NaI
Na2S4O6+2NaI
请写出实验中还涉及的另两个反应的化学方程式: 、
。
⑵试计算此污水中苯酚的含量(以mg/L表示,苯酚的相对分子质量为94.00)。
10.I.在一定条件下,一些含羰基的化合物能发生如下反应:
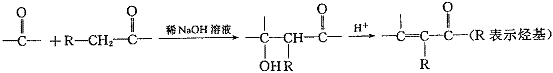
II.格氏试剂(RMgX,X表示卤原子)与含羰基的化合物能发生如下反应:
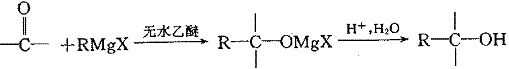
⑴以柠檬醛为原料,按以下反应流程图合成维生素A:
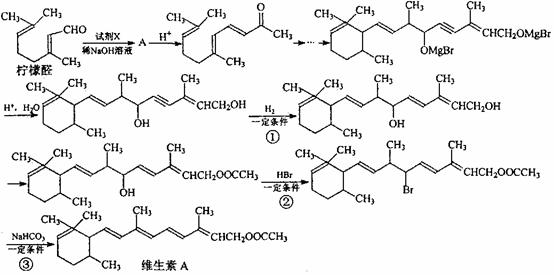
上述流程中,试剂X的结构简式为 ,①、②、③的反应类型分别是 、 、 。
⑵利用题目所给信息和学府的反应原理,以 、CH3CHO和CH3MgBr为有机原料(其他无机试剂任选),可以分5步合成
、CH3CHO和CH3MgBr为有机原料(其他无机试剂任选),可以分5步合成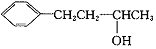 ,用反应流程图表示。
,用反应流程图表示。
。
9.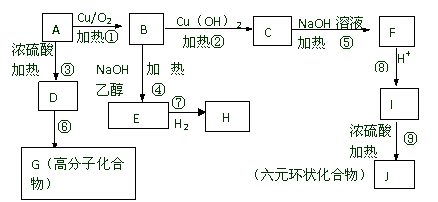 某有机物A的相对分子质量为94.5,在一定条件下可以发生如下转化(其他产物和水以省略)。请回答下列问题:
某有机物A的相对分子质量为94.5,在一定条件下可以发生如下转化(其他产物和水以省略)。请回答下列问题:
(1)按要求写化学式: A的分子式 J的结构简式
(2)在上述反应中①-⑨反应中,属于取代反应的是 ,属于消去反应的是
(3)写出下列反应的化学方程式:
B→C
C→F
(4)有机物I在一定条件下,可合成一种环保型的高分子材料,则该高分子材料的结构简式为
(5)写出 I的一种同分异构体(能与金属钠、NaOH溶液和银氨溶液均能反应)的结构简式
8.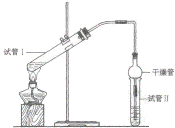 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制备乙酸乙酯的化学方程式如下:
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制备乙酸乙酯的化学方程式如下:
CH3COOH+C2H5OH CH3COOC2H5+H2O
CH3COOC2H5+H2O
为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下四个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
|
实验编号 |
试管Ⅰ中的试剂 |
试管Ⅱ中试剂 |
测得有机层的厚度/cm |
|
A |
2mL乙醇、2mL乙酸、1mL 18mol/L浓硫酸 |
饱和碳酸钠溶液 |
5.0 |
|
B |
3mL乙醇、2mL乙酸 |
0.1 |
|
|
C |
3mL乙醇、2mL乙酸、6mL 3mol/L硫酸 |
1.2 |
|
|
D |
3mL乙醇、2mL乙酸、盐酸 |
1.2 |
(1).实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是 mL和 mol/L。
(2).分析实验 (填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是 。
(3).加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是 。
7.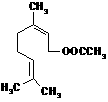 乙酸橙花酯是一种食用香料,结构如图所示。下列关于该物质的说法有:
乙酸橙花酯是一种食用香料,结构如图所示。下列关于该物质的说法有:
①该化合物属于酯类;②分子式C11H18O2;③1 mol该化合物最多可与2 mol H2反应;④化合物能发生的反应类型有:加成、取代、氧化、聚合;⑤该化合物有一种同分异构体属于酚类。其中正确的是
A.①③④ B.②③⑤ C.①④⑤ D.①③⑤
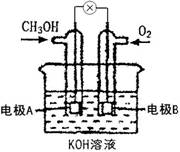
6.右下图是一燃料电池化学原理示意图,该燃料电池总反应化学方程式为:
 2CH3OH+3O2+4KOH
2K2CO3+6H2O以下判断不合理的是
2CH3OH+3O2+4KOH
2K2CO3+6H2O以下判断不合理的是
A.电极A为电池负极
B.电极B表面上发生还原反应
C.溶液pH保持不变
D.燃料电池工作时不会出现火焰
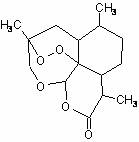
5.中国国家主席胡锦涛在中非合作论坛北京峰会上承诺:“提供3亿元人民币无偿援款帮助非洲防治疟疾,用于提供青蒿素药品及设立30个抗疟中心”。中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示。目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求。下列关于青蒿素的说法正确的是
 A. 是一种烃
B.属于高分子化合物
A. 是一种烃
B.属于高分子化合物
C.属于芳香族化合物 D.分子式是C15H22O5
4.香柠檬油可用于化妆品。香柠檬油含微量的香柠檬酚和香柠檬醚,其结构如右图。下列说法正确的是
A.香柠檬醚的分子式为C13H6O4
B.1mol香柠檬酚最多可与2molBr2发生反应
 C.香柠檬酚通过取代反应可转化成香柠檬醚
C.香柠檬酚通过取代反应可转化成香柠檬醚
D.1mol香柠檬酚在NaOH溶液中水解时能消耗2molNaOH
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com