
题目列表(包括答案和解析)
8.X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层电子总数少4,Z的最外层电子数是内层电子总数的3倍。有关下列叙述正确的是
A.X肯定为碱金属元素 B.稳定性:Y的氢化物>Z的氢化物
C.X、Y两元素形成的化合物可能为离子晶体
D.Y、Z两元素形成的化合物熔点较低
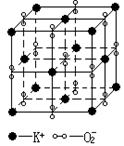
7.高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0
价,部分为-2价。下图为超氧化钾晶体的晶胞,下列说法正确的是
A.超氧化钾的化学式为KO2,每个晶胞平均含有4个K+和4个O2-
B.晶体中K+和O2-的配位数均为8 C.晶体中与每个K+距离相等且最近的K+有8个
D.晶体中,0价氧粒子与-2价氧粒子的数目比为3∶1
6.膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。以下关于PH3的叙述正确的是
A.PH3分子中有未成键的孤对电子 B.PH3是非极性分子
 C.它的分子构型是平面三角形
D.磷原子采用sp2杂化方式
C.它的分子构型是平面三角形
D.磷原子采用sp2杂化方式
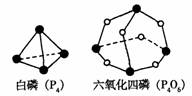
5.化学反应可视为旧键断裂和新键形成的过程。化学键的键能 是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如下图所示;现提供以下化学键的键能:P-P 198KJ·mol-1、P-O 360kJ·mol-1、氧气分子内氧原子间的键能为498kJ·mol-1则P4+3O2==P4O6的反应热△H为
A.+1638 kJ·mol-1 B、-1638 kJ·mol-1 C.-126 kJ·mol-1 D.+126 kJ·mol-1
4.元素R的最高价含氧酸化学式为HnRO2n-2,则在其最低价气态氢化物中,R元素的化合价为
A.-10+3n B.-6+3n C.-12+3n D.-4+2n
3.表示一个原子在第三电子层上有10个电子可以写成
 A. 310
B. 3d10
C. 3s23p63d2 D.
3s23p64s2
A. 310
B. 3d10
C. 3s23p63d2 D.
3s23p64s2
2.两种短周元素X和Y可组成XY2型化合物,则X、Y原子序数差不可能是
A.1 B.2 C.3 D.4
1.将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入HCl气体6.72L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是
A.反应过程中得到6.72L(标准状况)的气体 B.最终得到7.8g的沉淀
C.最终得到的溶液中c(NaCl)=1.5mo/L D.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-)
10.下列关于化学反应的自发性叙述中正确的是
A.焓变小于0而熵变大于0的反应肯定是自发的
B.焓变和熵变都小于0的反应肯定是自发的
C.焓变和熵变都大于0的反应肯定是自发的
D熵变小于0而焓变大于0的反应肯定是自发的
本资料由《七彩教育网》 提供!
9.NaF,Nal,MgO均为离子化合物,根据下列数据,这 三种化合物的熔点高低顺序是
|
物质 |
①NaF |
②NaI |
③MgO |
|
离子电荷数 |
1 |
1 |
3 |
 m m |
2.31 |
3.18 |
2.10 |
A.①>②>③ B.③>①>② C.③>②>① D.②>①>③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com