
题目列表(包括答案和解析)
9.在pH=0的无色透明溶液中,因发生氧化还原反应而不能大量共存的离子组是

8.某能使石蕊试液变红的溶液中,能大量存在的离子是
A.Al3+ NH4+ SO42- CI- B.Na+ Mg2+ HCO3- NO3-
C.K+ Na+ AlO2- Cl- D.Fe2+ K+ NO3- Cl-
7.下列各组离子在溶液中不能大量共存,且加入过量NaOH溶液或过量稀盐酸均能得到澄清溶液的是
A. Fe3+、CI-、Na+、SO42- B. AI3+、Na+、CO32-、NO3-
C. Ag+、Na+、SO42-、NO3- D. AIO2-、CO32-、K+、Na+
6.(2003南通市高三二模10.)某溶液由水电离出的c(H+)=10-12mol/L,则此溶液中可能大量共存的离子组是
A.HCO3-、Cl-、NH4+、Mg2+ B.Na+、K+、NO3-、Cl-
C.K+、Ba2+、I-、NO3- D.Ba2+、Na+、Cl-、SO42-
5.(2003南通市高三一模13.)在含有I-且能使酚酞变红的无色溶液中,可大量存在的离子组是
A.Na+、Cu2+、Br-、Cl- B.AlO2-、K+、NH4+、Na+
C.K+、Na+、NO3-、H+ D.K+、S2-、SO42-、OH-
4.(2003江苏卷12.)对某酸性溶液(可能含有Br-,SO42-,H2SO3,NH4+)分别进行如下实验:①加热时放出的气体可以使品红溶液褪色;②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸,对于下列物质不能确认其在溶液中是否存在的是
A.Br- B.SO42- C.H2SO3 D.NH4+
3.(2003江苏卷11.)若溶液中由水电离产生的c(OH-)=1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是
A.Al3+ Na+ NO-3 Cl- B.K+ Na+ Cl- NO3-
C.K+ Na+ Cl- AlO2- D.K+ NH4+ SO42- NO3-
2.(2001上海卷12.)下列离子在溶液中因发生氧化还原反应而不能大量共存的是
A.H3O+、NO3-、Fe2+、Na+ B.Ag+、NO3-、Cl-、K+
C.K+、Ba2+、OH-、SO42- D.Cu2+、NH4+、Br-、OH-
1.(2001全国卷13.)下列各组离子,在强碱性溶液中可以大量共存的是
A.I-、AlO2-、Cl-、 S2- B.Na+、K+、NH4+、Ba2+
C.Br-、S2-、Cl-、CO32- D.SO32-、NO3-、SO42-、HCO3-
15.(10分)硫铁矿高温下空气氧化产生二氧化硫:4FeS2+11O2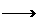 8SO2+2Fe2O3
8SO2+2Fe2O3
设空气中N2、O2的含量分别为0.800和0.200(体积分数,以下气体含量均用体积分数表示),试完成下列各题:
(1)1.00 mol FeS2完全氧化,需要空气的体积(标准状况)为 L。
(2)55 L空气和足量FeS2完全反应后,气体体积(同温同压)变为 L。
(3)用空气氧化FeS2产生的气体混合物中,O2的含量为0.0800,计算SO2的含量。
(4)设FeS2氧化产生的气体混合物为100 L,其中O2为a L,SO2为b L。
①写出a和b的关系式。
②在下图中画出a和b的关系曲线(FeS2氧化时,空气过量20%)。
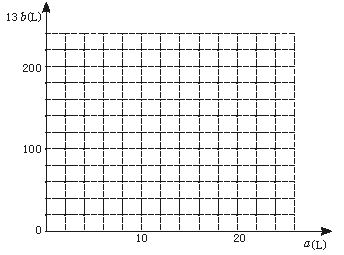
说明:为方便作图,纵坐标用13b表示。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com