
题目列表(包括答案和解析)
15.一定质量的氯酸钾与二氧化锰的混合物加热至无气体放出时,将残余的固体与足量的浓硫酸共热,并把此时生成的气体通入500 mL某浓度的亚硫酸钠溶液中,设气体被完全吸收且无SO2逸出,也无游离氯分子存在,测得溶液的pH=0(不计溶液体积变化),最后向溶液中加入足量的BaCl2溶液,生成不溶于酸的白色沉淀16.31 g。求原混合物中氯酸钾、二氧化锰的质量及亚硫酸钠溶液的物质的量浓度。
14.用纯度为92.5%(杂质不与Cl2反应)的消石灰与Cl2反应制漂白粉,消石灰的转化率为80%,要求某游泳池消毒一次需要4.26 kg Cl2,现改用上述漂白粉,假定起消毒作用的是HClO,要达到与Cl2相当的消毒效果,需向游泳池中投放这种漂白粉多少千克?
13.KClO3和浓盐酸在一定温度条件下反应会生成黄绿色的易爆物二氧化氯,其变化可表示为:
KClO3+ HCl(浓)-- KCl+ ClO2↑+ Cl2↑+
(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)。
(2)浓盐酸在反应中显示出来的性质是 (填写序号)。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)产生0.1 mol Cl2,则转移的电子的物质的量为 mol
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是Cl2的多少倍?
12.用下图所示装置(酒精灯、铁架台等未画出)制取三氯化磷,在短颈分馏烧瓶d中放入足量白磷,将Cl2迅速而又不间断地通入d中,氯气与白磷会发生反应,产生火焰。
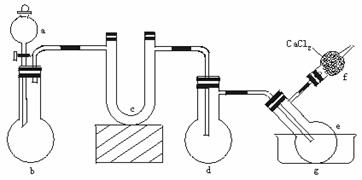
物质制备装置
三氯化磷和五氯化磷的物理常数如下表。
物质熔沸点
|
|
熔点 |
沸点 |
|
三氯化磷 |
-122℃ |
76℃ |
|
五氯化磷 |
148℃ |
200℃分解 |
图中,a,b应该装入的试剂或药品分别是浓盐酸和二氧化锰,在b仪器处加热。请据此回答下列回答:
(1)在蒸馏烧瓶e中收集生成的三氯化磷,为保证三氯化磷蒸气冷凝,应在水槽g中加入 。
(2)三氯化磷遇到水蒸气强烈反应,甚至发生爆炸,所以d,e仪器及装入其中的物质都不能含有水分。为除去Cl2中的水分,c中应装入 作干燥剂。
(3)实验室将白磷保存于水中,取出的白磷用滤纸吸干表面水分,浸入无水酒精中片刻,再浸入乙醚中片刻即可完全除去水分。已知水与酒精互溶,酒精与乙醚互溶,乙醚极易挥发,用上述方法除去水分的原因是 。
(4)为防止Cl2污染空气,装置末端导出的气体应如何净化处理,画出装置图并注明使用药品: 。
11.下图中的每一方格表示有关的一种反应物或生成物。反应时加入或生成的水,以及生成无色溶液M、白色沉淀N和黄绿色气体C时的其他产物均已略去。H为短周期元素组成的单质。A的焰色反应为浅紫色(透过蓝色钴玻璃观察)。
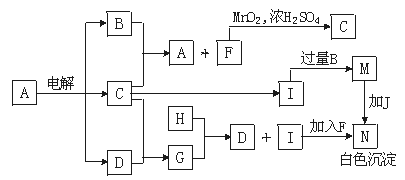
回答下列问题:
(1)A、H、N的化学式分别为A ,H ,N 。
(2)A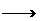 B+C+D的化学方程式:
。
B+C+D的化学方程式:
。
(3)F+I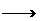 N的离子方程式:
。
N的离子方程式:
。
10. 写出下列物质与新制氯水反应的现象和化学方程式。
(1)紫色石蕊试液
(2)FeCl2溶液
(3)AgNO3溶液
(4)Na2CO3溶液
(5)SO2
(6)镁粉
9.在一定条件下,氯气可与氯化铵发生如下反应:
xCl2+yNH4Cl===yNClx+(x+y)HCl
当消耗6.72 L(标准状况下)的氯气时,生成0.10 mol氮的氯化物,则此氮的氯化物的化学式为
A.NCl2 B.NCl3
C.NCl4 D.NCl5
8.F2是氧化性最强的非金属单质。在加热条件下,等物质的量的F2与烧碱完全反应,生成NaF、H2O和另一种气体。该气体可能是
A.H2 B.HF
C.O2 D.OF2
7.将0.15 mol的MnO2与过量的12 mol·L-1的浓盐酸反应,和50 mL 12 mol·L-1的浓盐酸与足量的MnO2反应两者产生的Cl2相比(其他反应条件相同)
A.一样多 B.前者较后者多
C.后者较前者多 D.无法比较
6.今有甲、乙、丙三瓶等体积的新制氯水,浓度均为0.1 mol·L-1。如果在甲瓶中加入少量的NaHCO3晶体(m mol),在乙瓶中加入少量的NaHSO3晶体(m mol),丙瓶不变。片刻后,甲、乙、丙三瓶溶液中HClO的物质的量浓度大小关系是(溶液体积变化忽略不计)
A.甲=乙>丙 B.甲>丙>乙
C.丙>甲=乙 D.乙>丙>甲
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com