
题目列表(包括答案和解析)
4.已知热化学方程式:SO2(g)+ 1/2O2(g) 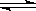 SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为
A. <196.64kJ B. 196.64kJ/mol C. 196.64kJ D. >196.64kJ
3.据最新报道,清华才女朱令11年前离奇的铊中毒案,再次引起人们关注。铊盐与氰化钾被列为A级危险品。铊(Tl)的原子序数为81,Tl3+与Ag在酸性条件介质中发生反应:Tl3++2Ag=Tl++2Ag+,Ag++Fe2+=Ag+Fe3+.下列推断不正确的是
A.Tl+最外层有2个电子 B.氧化性:Tl3+>Fe3+>Ag+>Fe2+>Al3+
C.还原性:Tl>Fe>Ag D.铊位于第六周期,第IIIA族
2.向200mL 0.5mol/L的稀硝酸溶液中加入0.54g铝粉,放出448mL (标况) NO气体,经充分反应后,向所得溶液中,加入0.5mol/L NaOH溶液,生成 0.78g沉淀。加入氢氧化钠溶液体积可能为
A.100mL B.150mL C.180mL D.200mL
1.在NaOH溶液中还可能大量存在的离子组是:
A.Ag+,K+ B. NH4+,SO42- C.Mg2+,C1- D.Ba2+,ClO-
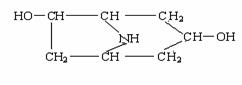
10.如图,除氢原子外,采取sp3杂化的原子数为
A .8 B .9 C .10 D.7
本资料由《七彩教育网》 提供!
9. 下列表达式错误的是
下列表达式错误的是
A.甲烷的电子式:
B.氮原子的L层电子轨道表示式:
C.硫离子的核外电子排布式:1s22s22p63s23p4
D.碳-12原子:12 6C
8.向pH=1的某酸溶液和pH=13的氢氧化钠溶液中,加入足量的铝片,放出H2的物质的量之比为3: 1其原因可能是
A.两溶液的体积相同,酸是多元强酸
B.若酸为一元强酸,酸溶液的体积是碱溶液体积的3倍
C.两溶液的体积相同,酸是弱酸
D.酸是强酸,且酸溶液的浓度比NaOH溶液浓度大
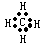
7.将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入HCl气体6.72L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是
A.反应过程中得到6.72L(标准状况)的气体 B.最终得到7.8g的沉淀
C.最终得到的溶液中c(NaCl)=1.5mo/L D.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-)
6.硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。硅氧四面体可以用投影图表示成:
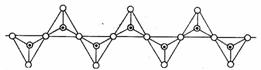
其中○表示氧原子,中心黑点表示硅原子。硅氧四面体通过不同方式的连接可以组成各种不同的硅酸根离子。试确定在无限长的单链阴离子中(见图),硅原子与氧原子的个数之比为 B
A.1:2 B.1:3 C.2:5 D.2:7
5.将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如右图所示。.则下列说法不正确的是
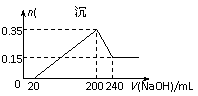 A.镁和铝的总质量为9 g
A.镁和铝的总质量为9 g
B.最初20 mLNaOH溶液用于中和过量的硫酸
C.硫酸的物质的量浓度为2.5 mol·L-1
D.生成的氢气在标准状况下的体积为11.2 L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com