
题目列表(包括答案和解析)
11、2005年9月始,“禽流感”在全球部分地区爆发,引起了人们继“非典型性肺炎”之后的世界范围内的恐慌。做好环境消毒是预防“禽流感”的重要措施,常用的消毒剂是ClO2或Cl2等的稀溶液,其中ClO2溶液的消毒效果较好。已知ClO2常温下呈气态,其分子构型与水分子的分子构型相似,在自然环境中ClO2最终变为Cl-。下列有关说法中正确的是
A、ClO2的分子结构呈V型,属非极性分子
B、ClO2中氯元素显+4价,具有很强的氧化性,其消毒效率(以单位气体体积得电子的数目表示)是Cl2的5倍
C、ClO2、Cl2的稀溶液用于环境消毒,具有广谱高效的特点,对人畜无任何危害
D、常用Na2SO3在H2SO4的酸性条件下,还原NaClO3来制ClO2,这一反应的化学方程式可表示为Na2SO3 + 2NaClO3 + H2SO4 = 2Na2SO4 + 2ClO2↑+ H2O
10、下列反应的离子方程式正确的是
A、在Mn2+的溶液中加入HNO3再加入PbO2,得紫红色溶液:
5PbO2+2Mn2++4H+ = 5Pb2++2MnO4-+2H2O
B、4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合:
4AlO2-+7H++H2O = 3Al(OH)3↓+Al3+
C、Ba(OH)2溶液中加入少量的NaHSO4溶液:
Ba2++2OH- +2H++SO42-=BaSO4↓+2H2O
 D、NaHCO3的水解:HCO3-+H2O CO32-+H3O+
D、NaHCO3的水解:HCO3-+H2O CO32-+H3O+
9、下列各组溶液中,不用任何其它试剂不能鉴别的是
A、 NaOH FeCl3 MgCl2 K2SO4 B、HCl NaOH K2SO4 NaHCO3
C、 NaAlO2 KHCO3 NaCl NaHSO4 D、Na2SO4 H2SO4 AlCl3 BaCl2
8、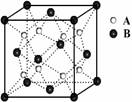 某离子晶体的晶体结构中最小重复单元如图所示:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为
某离子晶体的晶体结构中最小重复单元如图所示:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为
A、B2A B、BA2
C、B7A4 D、B4A7
7、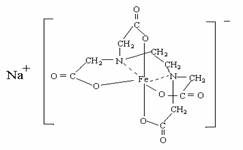 联合国世界卫生组织调查,当今缺铁性贫血是世界上最流行的营养性问题,我国缺铁性贫血发生率达到15%至20%,为此2004年10月9日卫生部启动和推广铁强化酱油计划,以预防缺铁性贫血。所谓铁强化酱油即在普通酱油中加入无铁腥味、极易被人体吸收的添加剂--EDTAFeNa(化学名:乙二胺四乙酸铁钠,通常带三个结晶水,分子式为:C10H12FeN2NaO8.3H2O),EDTAFe是一种其中络合铁, EDTAFeNa 的结构式为:
联合国世界卫生组织调查,当今缺铁性贫血是世界上最流行的营养性问题,我国缺铁性贫血发生率达到15%至20%,为此2004年10月9日卫生部启动和推广铁强化酱油计划,以预防缺铁性贫血。所谓铁强化酱油即在普通酱油中加入无铁腥味、极易被人体吸收的添加剂--EDTAFeNa(化学名:乙二胺四乙酸铁钠,通常带三个结晶水,分子式为:C10H12FeN2NaO8.3H2O),EDTAFe是一种其中络合铁, EDTAFeNa 的结构式为:
,EDTA的结构简式为:(HOOCCH2)2NCH2CH2N(CH2COOH)2,
下列说法正确的是
A、EDTAFeNa的化学式为C10H16N2O8FeNa
B、EDTAFeNa中铁为+2价
C、EDTA属于有机物
D、人体血液中血红蛋白中铁为+3价
6、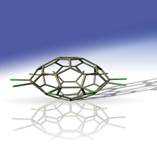 Science304,p.699(2004)报道,厦门大学的郑兰荪院士及其
Science304,p.699(2004)报道,厦门大学的郑兰荪院士及其
在北京和武汉中科院的同事,成功的利用电弧放电法稳定地制备出C50衍生物,C50由于结构中存在五元环与五元环连接,故很活泼难捕捉。它们制取的方法是在不锈钢的腔体之中,加入0.013atm的四氯化碳(tetrachloride)气体及0.395atm的氦气,然后外加24v的偏压,石墨电弧方法放电,产生约90g的煤灰,经纯化之后得到2mg纯度99.5%的C50Cl10。研究人员表示,C50Cl10外型像艘宇宙飞船,带有10根可产生反应的碳氯悬臂,它跟C60或C70一样很容易和不同的有机物形成物理或化学性质相当有趣的新化合物. 已知:多面体的顶点数、面数和棱这数的关系,遵循欧拉定理:顶点数 + 面数-棱边数 = 2。结合题中信息,下列有关C50Cl10推测肯定不正确的是
A、1molC50Cl10最多与25molF2发生加成反应
B、根据欧拉公式,由C50组成的环中,有12个正五边形,15个六边形构成
C、C50Cl10在一定条件可发生取代反应,从而为定向合成开辟新路
D、四氯化碳作用是作为氯源,以此捕获和稳定C50分子
5、100℃时,将0.1molN2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) 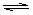 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①烧瓶内气体的颜色不再加深,②N2O4 的消耗速率与NO2的生成速率之比为1∶2,③NO2的生成速率与NO2消耗速率相等,④NO2的物质的量浓度不变,⑤烧瓶内气体的质量不再变化,⑥烧瓶内气体的压强不再变化,⑦烧瓶内气体的密度不再变化,⑧烧瓶内气体的平均相对分子质量不再变化
A、②⑤⑦ B、①③④⑥⑧ C、只有③ D、只有⑤
4、下列有关物质分类或归类正确的是
①混合物:石炭酸、福尔马林、水玻璃、水银
②化合物:CaCl2、烧碱、聚苯乙烯、HD
③电解质:明矾、胆矾、冰醋酸、硫酸钡
④同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
⑤同素异形体:C60、C70、金刚石、石墨
A、①③④ B、③⑤ C、②③④ D、②④
3、2005年10月12日我国成功发射了第二艘载人航天飞船--“神州六号”,实现了双人多天太空旅行。这标志着中国人的太空时代又前进了一大步。发射“神六”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。
已知:N2(g) + 2O2(g) = 2NO2(g); △H = + 67.7kJ/mol
N2H4(g) + O2(g) = N2(g) + 2H2O(g); △H = – 534kJ/mol
下列关于肼和NO2反应的热化学方程式中,正确的是
A、2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(l);△H = – 1135.7kJ/mol
B、2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g);△H = – 1000.3kJ/mol
C、N2H4(g) + NO2(g) = 3/2N2(g) + 2H2O(l);△H = – 1135.7kJ/mol
D、2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g);△H = – 1135.7kJ/mol
2、下列各化学式既能表示物质的化学组成,又能表示物质分子式的是
① Mg ②NH4NO3 ③CH2O ④SiO2 ⑤C6H5NO2 ⑥Al2O3 ⑦NH3·H2O
⑧P ⑨Ag(NH3)2OH ⑩S8
A、①②⑤⑧ B、③⑤⑦⑩ C、③④⑦⑧ D、③⑤⑥⑨
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com