
题目列表(包括答案和解析)
2、下列各种溶液中,能大量共存的无色透明的离子组( )
A.使PH=0的溶液: Fe2+ 、NO3-、SO42-、I-
B.C(H+)=10-14mol· L-1的溶液中:Na+ 、AlO2-、S2-、SO32-
C.酸性环境下:Na+ 、 Cu2+ 、NO3-、SO42-、
D.使紫色石蕊试液变红的溶液中:K+ 、Na+ 、Ca2+ 、HCO3-
1、在下述条件下,一定能大量共存的离子组是( )
A.无色透明的水溶液中:K+、Mg2+、I-、MnO4-
B.pH=1的NaNO3水溶液中:NH4+、Fe2+、SO42-、Cl-
C.c(HCO3-)=0.1mol/L的溶液中:Na+、K+、CO32-、Br-
D.由水电离产生的c(OH-)=1×10-14mol/L的溶液中:H+、Al3+、Cl-、NO3-
3、下列离子方程式正确的是( )
A.向碘化亚铁溶液中通入少量氯气 2Fe2++Cl2=2Fe3++2Cl-
B.向次氯酸钙溶液中通入过量二氧化硫 Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
C.向硫酸氢钠溶液中滴入氢氧化钠溶液至中性 H++SO +Ba2++OH-=BaSO4↓+H2O
+Ba2++OH-=BaSO4↓+H2O
D.将氢氧化铁粉末加入氢碘酸中 Fe(OH)3+3H=Fe3++3H2O
2、下列反应的离子方程式正确的是( )
(A)金属钠跟水反应:Na+2H2O=Na++2OH-+H2↑
(B)在漂白粉溶液中通入过量SO2 :ClO¯+SO2+H2O=HSO3━+HClO
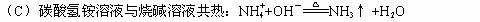
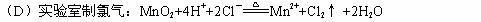
1、下列离子方程式正确的是( )
A.等物质的量的Ba(OH)2与明矾溶液混合:3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓
B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
C.H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2↑
D.CuCl2溶液中加入NaHS溶液:Cu2++2HS-+2H2O=Cu(OH)2↓+2H2S↑
3、已知胆矾溶于水时溶液温度降低。胆矾分解的热化学方程式为:
CuSO4·5H2O(s)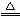 CuSO4(s)+5H2O(l);ΔH= +Q1 kJ/mol
CuSO4(s)+5H2O(l);ΔH= +Q1 kJ/mol
室温下,若将1mol无水硫酸铜溶解为溶液时放热Q2 kJ,则Q1与Q2的关系为( )
A.Q1>Q2 B.Q1=Q2 C.Q1<Q2 D.无法比较
2、已知H+(aq)+OH-(aq)=H2O(l);ΔH= -57.3 kJ/mol。若向三份等体积、等物质的量浓度的NaOH溶液中分别加入:①稀醋酸;②浓硫酸;③稀硝酸至恰好完全反应,并将上述过程中放出的热量分别记为Ql、Q2、Q3。下列关系式中正确的是( )
A.Q1<Q3<Q2 B.Ql<Q2<Q3 C.Q1<Q2=Q3 D.Q1=Q2=Q3
1、下列说法或表示方法正确的是( )
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(石墨)→C(金刚石);ΔH= +119 kJ/mol可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l);ΔH= -57.3 kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1 mol NaOH的稀溶液混合,放出的热量大于57.3 kJ
D.在101kPa、25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l);ΔH= -285.8 kJ/mol
3、羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原。现用25.00mL0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.65mL 0.020mol/L的KMnO4酸性溶液完全作用(已知:FeSO4+ KMnO4+ H2SO4= Fe2(SO4)3+ K2SO4+ MnSO4+ H2O(未配平)),则在上述反应中,羟胺的氧化产物是( )
(A)N2 (B)N2O (C)NO (D)NO2
2. 将一定量的锌与100mL 18.5mol/L浓硫酸充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的pH=1,则下列叙述中错误的是( )
A. 气体A为SO2和H2的混合物 B. 气体A中SO2与H2的体积比为4:1
C. 反应中共消耗Zn 97.5g D. 反应中共转移电子3mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com