
题目列表(包括答案和解析)
4.除去下列物质中所含少量杂质的方法正确的是( )。
|
|
物质 |
杂质 |
试剂 |
提纯方法 |
|
A |
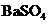 |
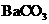 |
稀盐酸 |
溶解、过滤、洗涤 |
|
B |
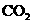 |
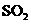 |
饱和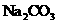 溶液 溶液 |
洗气 |
|
C |
乙酸乙酯 |
乙酸 |
稀 溶液 溶液 |
混合振荡、静置分液 |
|
D |
蛋白质 |
蔗糖 |
浓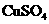 溶液 溶液 |
盐析、过滤、洗涤 |
3.下列说法正确的是( )。
A.硝酸、纯碱、胆矾和生石灰分别属于酸、碱、盐和氧化物
B.碳酸钙和水分别属于强电解质和弱电解质
C.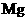 、
、 、
、 可以分别用置换法、直接加热法和电解法冶炼得到
可以分别用置换法、直接加热法和电解法冶炼得到
D. 、
、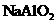 、
、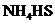 、
、 均既能与盐酸又能与
均既能与盐酸又能与 溶液反应而呈两性
溶液反应而呈两性
2.在化学实验中必须注意安全,以下实验操作或事故处理中正确的是( )。
①在点燃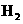 、
、 、
、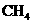 等易燃性气体前,必须检验气体的纯度
等易燃性气体前,必须检验气体的纯度
②在稀释浓硫酸时,应将浓硫酸沿器壁慢慢注入水中并不断用玻璃棒搅拌
③浓碱液对皮肤有腐蚀性,如不慎沾到皮肤上,应用较多的水冲洗,再涂上硼酸溶液
④给试管中的液体加热时,液体应不超过试管容积的 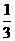
⑤点燃添满酒精的酒精灯
⑥苯酚溶液不慎沾到皮肤上,立即用浓氢氧化钠溶液洗涤
⑦给装在试管中的液体加热时,试管口不能对着自己或他人
⑧配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加人浓硫酸
A.仅⑤⑥⑧ B.仅①②③ C.仅①②③④⑦ D.全部
1.背景材料:①“神舟七号”的防护层由聚四氟乙烯和玻璃纤维布组合而成;②据不完全统计。目前我国年产垃圾总量约5亿吨,其中三分之二的垃圾是可以回收再利用的;③汞是有毒的金属;④据环境质量监测所抽查显示,新装修住房甲醛含量七成超标。⑤在广东、香港海域.渤海湾均出现过大面积的赤潮。⑤绿色化学(Green Chemistry)又称环境无害化学(Environmental Benign Chemistry)或清洁化学,是从源头上防止污染产生或把化学过程对环境的负面影响降低到最低程度的化学。
据此判断,下列说法正确的是( )。
(1)“神舟七号”的防护层是复合材料,四氟乙烯属于不饱和烃。
(2)将垃圾分类并回收再利用,既节约自然资源,又防止污染,符合可持续发展的要求,正成为垃圾处理的发展方向。
(3)无机汞(如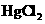 )会在水中微生物的作用下转化为毒性更大的有机汞(如
)会在水中微生物的作用下转化为毒性更大的有机汞(如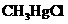 )。
)。
(4)为降低甲醛含量,新装修住房应紧闭门窗,并放置一盆水。
(5)赤潮是指在一定条件下海洋中某些生物短时间内大量繁殖或聚集,使海水变红色、褐色的现象。
(6)绿色化学就是生产绿色化学物质的工艺。
A.(1)(3)(6) B.(1)(4)(5) C.(2)(3)(5) D.(2)(4)(6)
27.(8分)将32 g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO 和NO2混合气体在标准状况下的体积为13.44 L。请回答:
(1)NO的体积为 L, NO2的体积为 L。
(2)待产生的气体全部释放后,向溶液中加入VmLa mol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为 mol·L-1 。
(3) 欲使铜与硝酸反应生成的气体在溶液中全部转化为NaNO3,至少需要通入标准状况下氧气 L。
26.(6分)有硫酸、硫酸铜、硫酸铁的混合溶液100mL,已知溶液中各阳离子的物质的量浓度相等,硫酸根离子的浓度为6.0mol·L-1。求此溶液理论上最多可溶解铁粉的质量。
25.(12分)某兴趣小组设计如下图所示装置模拟工业接触法制硫酸,并测定此条件下二氧化硫的转化率。实验时观察到E中溶液褪色。回答下列问题:

(1)写出A中发生的化学方程式:
(2)装置B有三个作用①使SO2、O2充分混合;② ③ 。
(3)装置C、D分别再现了工业制硫酸中 、 (填设备名称)中的反应。
(4)SO2能使品红溶液褪色,且加热后能恢复原颜色。若对E褪色后的溶液加热,能恢复原颜色吗?为什么?
,
(5)若实验结束后,装置D、E、F质量分别增加了a、b、c g,则SO2的转化率为: (用a、b、c中的一个或几个字母的代数式表示)。
(6)若控制SO2、O2比例时,O2速率过快,可使SO2的转化率:
(填“偏小”“偏大”“不变”)。
24.(8分)现有下列短周期元素性质的数据:
 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径(10-10m) |
0.74 |
1.60 |
1.52 |
1.10 |
0.99 |
1.86 |
0.75 |
1.43 |
|
最高或最低化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
-2 |
|
|
-3 |
-1 |
|
-3 |
|
试回答下列问题:
(1)上述元素中处于ⅤA族的有: (用编号表示)
(2)处于第2周期的元素有: 被称为“矾”的一类化合物中肯定含有表中 。(以上均用编号表示)
(3)写出②、⑤的元素符号: 、 。
(4)上述元素中金属性最强的是: (用元素符号表示)
(5)④和⑤两元素中非金属性较强的是(写元素符号) 。写出证明这一结论的一个实验事实 。
23.(8分)下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。
常温下X是固体,且是一种正盐,B和G是液体,其余均为气体。根据右图关系推断:
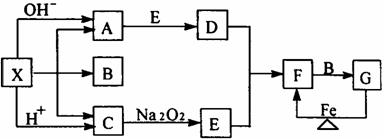
(1)写出下列物质化学式:
X____________,A___________
(2)写出A的结构式,C的电子式:A C 。
(3)写出A与E反应生成D的化学方程式_______________________________。
(4)写出G与足量Fe在加热条件下转化为F的离子方程式: 。
22.(8分)有几种元素的微粒电子层结构如图 所示,其中:
(1)某电中性微粒一般不和其他元素的原子反应,这种微粒符号是______ __。
(2)某微粒的盐溶液,加入AgNO3溶液时会出现白色浑浊,这种微粒符号是___ 。
(3)某微粒氧化性甚弱,但得到电子后还原性强且这种原子最外层有一个电子,这种微粒符号是__ _。
(4)某微粒具有还原性,且这种微粒失去2个电子即变为原子,这种微粒的符号是__
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com