
题目列表(包括答案和解析)
4. 实验室需要配制0.5mol·L-1的烧碱溶液500mL,根据溶液配制的过程,回答下列问题:
(1)实验中除了托盘天平(带砝码)、药匙、量筒和玻璃棒外,还需要的其它玻璃仪器有: ;
(2)根据计算得知,所需NaOH固体的质量为 g;
(3)配制溶液的过程中,有以下操作。其中,正确的是 (填代号)。
A.将氢氧化钠固体放在纸片上称量;
B.在烧杯中溶解氢氧化钠固体后,立即将溶液倒入容量瓶中;
C.将溶解氢氧化钠的烧杯中用蒸馏水洗涤2-3次,并将洗涤液转移到容量瓶中。
(4)玻璃棒在该实验中的作用有:①
。
②
3. 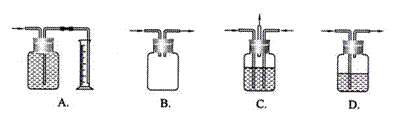 广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其它简单仪器组成各种功能的装置。下列各图中能用作防倒吸安全瓶的是
广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其它简单仪器组成各种功能的装置。下列各图中能用作防倒吸安全瓶的是
2.下列实验操作或所记录的数据合理的是
A.NaOH溶液可保存在玻璃塞的试剂瓶中
B.液溴应盛放在用水密封且用玻璃塞塞紧的棕色试剂瓶中
C.一学生用广泛pH试纸测得某浓度的稀盐酸pH为2.3
D.配制硫酸亚铁溶液,是将绿矾晶体溶于蒸馏水再加入一定量的铁粉
1. 某实验报告记录了如下数据,其中数据合理的是
A.用广泛试纸测得氯水的pH值为2.1 B.用50mL量筒量取23.00 mL浓盐酸
C.用温度计测量出酒精的沸点为78.5℃ D.用托盘天平称量氧化铜粉末为11.70g
(1)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是
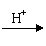
种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+ Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu2O。
;
(2)在解决了问题(1)后,又有同学提出:Cu2O与CuO的热稳定性哪个更强?于是他们进行了如下实验:取98Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变为红色粉末A。冷却后称量,A的质量为72g。据此可推得,A的化学式为 。由此,得到的结论是
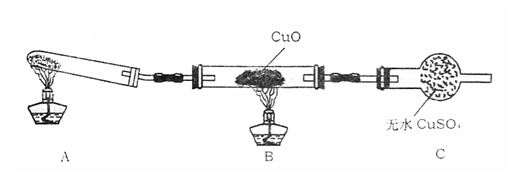
(1)该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是
。
(2)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与CuO反应的化学方程式
。
(1)写出实验制取氨气的化学方程式 ;
(2)在实验室中,还可以用浓氨水与 (填写一种试剂)快速制取少量氨气;
(3)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的? (填“能”或“否”),理由是
。
3. 水垢可以看作由多种物质组成的混合物,为研究含有Ca2+、Mg2+、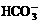 的水所形成的水垢的化学组成,取干燥的水垢6.32 g ,加热使其失去结晶水,得到5.78 g 剩余固体A;高温灼烧A至恒重,残余固体为CaO和MgO,放出的气体用过量的Ba(OH)2溶液吸收,得到的11.82 g沉淀。
的水所形成的水垢的化学组成,取干燥的水垢6.32 g ,加热使其失去结晶水,得到5.78 g 剩余固体A;高温灼烧A至恒重,残余固体为CaO和MgO,放出的气体用过量的Ba(OH)2溶液吸收,得到的11.82 g沉淀。
(1)通过计算确定A中是否含有碳酸镁;
(2)5.78 g剩余固体A灼烧至恒重时产生的气体完全被碱石灰吸收,碱石灰增重2.82 g,通过计算确定A中各成分的物质的量,并计算出水垢中碳酸盐质量分数。
2. 较低温度下,氯气通入石灰乳中可制得漂白粉,该反应为放热反应。某校甲、乙两化学研究性学习小组均用200 mL 12 mol / L盐酸与17.4 g MnO2在加热条件下反应制备氯气,并将制备的氯气与过量的石灰乳反应制取漂白粉,用稀氢氧化钠溶液吸收残余的氯气。分析实验结果发现:① 甲、乙两组制得的漂白粉中Ca(ClO)2的质量明显小于理论值,② 甲组在较高温度下将氯气与过量的石灰乳反应,所制得的产品中Ca(ClO3)2的含量较高。试回答下列问题:
(1)上述实验中理论上最多可制得Ca(ClO)2多少克?
(2)实验中所得到的Ca(ClO)2的质量明显小于理论值,试简要分析其可能原因,并写出可能涉及到的化学方程式。
1. 将3.20g Cu溶于B mol/L过量的硝酸溶液30.0 mL中,假设硝酸的还原产物只有NO2和NO,反应结束后,将所剩溶液加水稀释至1000 mL,测得c(NO3-)=0.200 mol/L。
(1)试求稀释后溶液的pH。
(2)生成的气体中NO2和NO的物质的量(可以含有B的代数式表示)。
(3)用NaOH溶液吸收氮的氧化物是防止NOx污染的一种方法。原理为:
2NO2+2NaOH=NaNO3+NaNO2+H2O,NO+NO2+2NaOH=2NaNO2+H2O
若生成的混合气体能被NaOH溶液完全吸收,试讨论B的取值范围。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com