
题目列表(包括答案和解析)
6.下列微粒对水的电离平衡不产生影响的是
A. B.
B.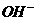 C.
C. D.
D.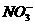
29.(14分)将羧酸的碱金属盐溶液用惰性电极电解可得到烃类化合物,例如:
2CH3COOK+2H2O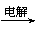
 CH3CH3↑+2CO2↑+H2↑+2KOH
CH3CH3↑+2CO2↑+H2↑+2KOH
现有下列衍变关系(A、B、C、D、E、F、G均为有机物):

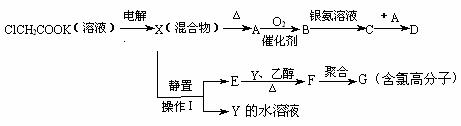
回答下列问题:
(1)写出电解ClCH2COOK溶液时的阳极的电极反应式_____________________。
(2)操作Ⅰ的名称是_____________,G的结构简式是_________________。
(3)写出B与银氨溶液按物质的量1:4反应生成C的化学方程式________________。
(4)A和C在不同条件下反应,会生成不同的D。
①若D的相对分子质量是B的2倍,则D的结构简式是_____________________;
②若D是高分子化合物,则D的结构简式是____________________。
28.(16分)(1)工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体:


①在步骤a中,还需要通入氧气和水,其目的是 。
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在 范围。
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ Cu2+ |
1.9 4.7 |
3.2 6.7 |
不用加水的方法调节溶液pH的原因是 。
③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明) 。
(2)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是 。
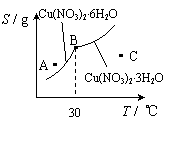 (3)右图是某小组同学查阅资料所绘出的硝酸铜晶体[ Cu(NO3)2·nH2O
]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是
(填字母)。
(3)右图是某小组同学查阅资料所绘出的硝酸铜晶体[ Cu(NO3)2·nH2O
]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是
(填字母)。
a. A点时的溶液为不饱和溶液
b. B点时两种晶体可以共存
c. 按上述流程最终得到的晶体是Cu(NO3)2·3H2O
d.若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2·6H2O晶体
(4)某些共价化合物(如H2O、NH3、N2O4等)在液态时有微弱的导电性,主要是因为发生了电离,如:2NH3 NH
NH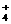 +NH
+NH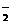 ,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应。液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是 ;Cu与液态N2O4反应制得无水硝酸铜的化学方程式是 。
,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应。液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是 ;Cu与液态N2O4反应制得无水硝酸铜的化学方程式是 。
27.(10分) 已知H2B在水溶液中存在以下电离:

 一级电离:H2B H++HB-,二级电离:HB- H++B2-
一级电离:H2B H++HB-,二级电离:HB- H++B2-
请回答以下问题:
(1)NaHB溶液 (填“呈酸性”、“呈碱性”或“无法确定”),原因是
。
(2)若0.1mol·L-1的H2B溶液在某温度下的pH=3,c(B2-)=1×10-6mol·L-1,则H2B的一级电离的电离度为 。
(3)某温度下,在0.1mol·L-1的NaHB溶液中,以下关系一定不正确的( )
A.c(H+)·c(OH-)=1×10-14 B.pH>1
C.c(OH-)=2c(H2B)+c(HB-)+c(H+) D.c(Na+)=0.1mol·L-1≥c(B2-)

 (4)某温度下,FeB(s) Fe2+(aq)+B2-(aq)
(4)某温度下,FeB(s) Fe2+(aq)+B2-(aq)
的平衡常数表达式为KSP=c(Fe2+)·c(B2-),
FeB在水中的沉淀溶解平衡曲线如右图所示。
下列说法错误的是( )
A.a点对应的KSP等于b点对应的KSP
B.d点无沉淀生成
C.可以通过升温实现由c点变到a点
D.此温度下,KSP=4×10-18
13.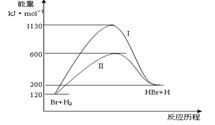 参照反应Br + H2
参照反应Br + H2 HBr +H的能量对反应历程的示意图,下列对上述正反应叙述中正确的 ( )
HBr +H的能量对反应历程的示意图,下列对上述正反应叙述中正确的 ( )
A. 反应热:过程I>过程Ⅱ B. 反应速率:过程Ⅱ=过程I
C. 该反应为吸热反应 D. 过程I使用了催化剂
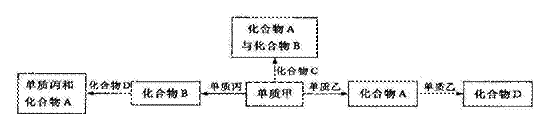 26、(18分)化合物A、B、C、D各由两种元素组成,甲、乙、丙是前两周期元素的三种单质。这些常见的化合物与单质之间存在如下关系(已知化合物C是一种有机物),回答以下问题:
26、(18分)化合物A、B、C、D各由两种元素组成,甲、乙、丙是前两周期元素的三种单质。这些常见的化合物与单质之间存在如下关系(已知化合物C是一种有机物),回答以下问题:
Ⅰ、(1)化合物物A的电子式为 ;化合物A、B、D的熔沸点从大到大小的顺序为 (用字母表示)。
(2)下列说法正确的是
 。
。
A、图中五个转化关系,有三个是化合反应 B、上述所涉及的化合物中有两种是电解质
B、上述所涉及的化合物中有两种是电解质
C、上述所涉及的化合物的晶体均是分子晶体 D、图中五个转化关系均为氧化还原反应
D、图中五个转化关系均为氧化还原反应
(3)用甲、丙、乙、氢氧化钾溶液可以构成一原电池,则电极材料可以为 ,负极的电极反应式为 。
Ⅱ.设反应①Fe(s)+CO2(g) FeO(s)+CO(g);△H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g);△H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)
 FeO(s)+H2(g);△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g);△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
|
T/K |
K1 |
K2 |
|
973 |
1.47 |
2.38 |
|
1 173 |
2.15 |
1.67 |
(1)从上表可推断,反应①是 (填“放”或“吸”)热反应。
(2)现有反应③H2(g)+CO2(g) CO(g)+H2O(g);△H=Q3平衡常数为K3。
CO(g)+H2O(g);△H=Q3平衡常数为K3。
①根据反应①与②,可推断反应③是 (填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有 。
A.缩小容器体积 B.降低温度 C.使用合适的催化剂
D.设法减少CO的量 E.升高温度
②根据反应①与②推导出Q1、Q2、Q3的关系式Q3= 。
12. 2008年9月25日晚9时10分神七发射成功,9月27日下午,01号航天员翟志刚担任出舱航天员,成中国太空行走第一人。神舟七号圆满完成中国航天员出舱等四大科学试验,创下了中国航天领域的四个第一。由解放军总装备部军事医学院研究所研制的小分子团水,解决了航天员的如厕难题。新型小分子团水,具有饮用量少、渗透力强、生物利用率高、在人体内储存时间长、排放量少的特点。一次饮用125mL小分子团水,可维持人体6小时正常需水量。下列关于小分子团水的说法正确的是
A.水分子的化学性质改变 B.水分子中氢氧键缩短
C.水分子间的作用力减小 D.水分子间结构、物理性质改变
11.下列各组离子在指定条件下,-定能大量共存的是
A.在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、HCO3-、Na+
 B.pH=1的溶液中:Cu2+、Al3+、SO42-、NO3-
B.pH=1的溶液中:Cu2+、Al3+、SO42-、NO3-
 C.能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH4+、S2-、Br-
C.能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH4+、S2-、Br-
 D.水电离出的c(H+)=10-12mol/L的溶液中:Na+、Mg2+、Cl-、S2-
D.水电离出的c(H+)=10-12mol/L的溶液中:Na+、Mg2+、Cl-、S2-
10.下列实验操作或原理不正确的是 ( )
A.纸层析法中的展开剂之所以能够展开的主要原理是毛细现象
B.分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较
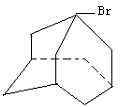
9. 阻断病毒附着于敏感细胞的金刚乙胺,对于多种甲型流感病毒都具很好的抑制作用,金刚乙胺可由金刚烷制得。1-溴金刚烷的结构如图所示,若它与NaOH醇溶液反应后所得物质的同分异构体中,含有苯环且只有一个取代基的同分异构体有:
A.5种 B.4种 C.3种 D.2种
8.化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语错误的是 ( ) 网
A.氢气燃烧的热化学方程式为:2H2(g)+O2(g)===2H2O(g);△H=571.6kJ·mol-1
 B.明矾水解的离子方程式:Al3++3H2O Al(OH)3+3H+
B.明矾水解的离子方程式:Al3++3H2O Al(OH)3+3H+
C.NaOH(aq)与NaHCO3(aq)反应离子方程式:HCO-3+OH-===CO32-+H2O
 D.钢铁电化腐蚀时,负极反应为:Fe-2e-=Fe2+
D.钢铁电化腐蚀时,负极反应为:Fe-2e-=Fe2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com