
题目列表(包括答案和解析)
22.(8分)化学中用类比的方法可预测许多物质的性质。如根据H2+C12=2HCl推测:H2+Br2=2HBr。但类比是相对的,如根据2Na2O2+2CO2=2Na2CO3+O2类推:2Na2O2+2SO2=2Na2SO3+O2是错误的,应该为:Na2O2+SO2=Na2SO4。
(1)下列各组类比中正确的是 (填序号);
|
|
B.由2Fe+3Cl2==2FeCl3 推测: 2Fe+3Br2==2FeBr3
C.由Na2SO3+2HCl=2NaCl + H2O+SO2↑ 推测:Na2SO3+2HNO3==2NaNO3+H2O+SO2↑
D.由I2易溶于KI溶液 推测: C12易溶于NaCl溶液
(2)由氧化铁与盐酸反应生成氯化铁和水,应用有关知识推断写出氧化亚铁与稀硝酸反应的化学方程式 ;
(3)电镀厂向含氰化物的电镀废液中加入漂白粉以消除有毒的CN-的化学方程式为 □CN-+□ClO-+□H2O =□HCO3-+□N2 +□Cl-,配平该反应的化学方程式,在方框中填上系数;
(4)(CN)2被称为拟卤素,它的阴离子CN-作为配体形成的配合物有重要用途。HgCl2 和Hg(CN)2反应可制得Hg2Cl2 和(CN)2,该反应的氧化产物是 。
21.(13分)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者的混合物。限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹、铁钉、3 mol·L-1H2SO4、0.01 mol·L-1KMnO4、NaOH稀溶液、0.1 mol·L-1KI、20%KSCN、蒸馏水。探究过程如下:
(1)查阅资料:Cu2O溶于稀硫酸生成Cu和CuSO4:Cu2O+2H+ = Cu + Cu2++ H2O;单质Cu能将Fe3+还原成Fe2+:2Fe3+ + Cu = 2Fe2+ + Cu2+。
(2)提出假设:
假设l:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是______________;
(3)实验过程:
设计实验方案证明你的假设;根据设计的实验方案,进行实验。请在答题卡上按下表格式写出实验操作步骤、预期现象。
|
|
实验操作 |
预期现象 |
结 论 |
|
操作1: |
|
|
假设1或假设3成立 |
|
操作2: |
|
|
假设1成立 |
|
|
假设3成立 |
||
|
操作3: |
|
|
假设2或假设3成立 |
|
操作4 |
|
|
假设2成立 |
|
|
假设3成立 |
20.(11分)某实验小组对FeCl3的性质和用途展开了实验。
实验一:
实验步骤
①往锥形瓶中加入50 mL、3.0%的双氧水。
②分别往锥形瓶中加0.5 g不同的催化剂粉末,立即塞上橡皮塞。
③采集和记录数据。
④整理数据得出下表。
表:不同催化剂催化双氧水分解产生O2的压强对反应时间的斜率
|
催化剂 |
氯化铁 |
二氧化锰 |
猪肝 |
马铃薯 |
|
压强对时间的斜率 |
0.0605 |
3.8214 |
0.3981 |
0.0049 |
(1)该“实验一”的实验名称是 ;
(2)催化效果最好的催化剂是 ;
实验二:氯化铁催化分解双氧水的最佳条件
该实验小组的同学在进行实验二时,得到了如下的数据。
表:不同浓度的双氧水在不同用量的FeCl3·6H2O作用下完全反应所需时间
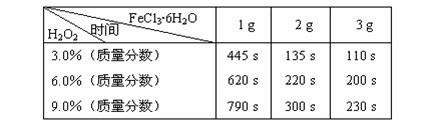
分析表中数据我们可以得出:
(3)如果从实验结果和节省药品的角度综合分析,当选用6.0%的双氧水时,加入______g FeCl3·6H2O能使实验效果最佳;
(4)进行该实验时,控制不变的因素有反应温度、 等;
(5)如图是2 gFeCl3·6H2O催化分解50 ml3.0%的
双氧水时收集到的O2体积对反应时间示意图,
请分别画出相同条件下1 g、3 g FeCl3·6H2O催
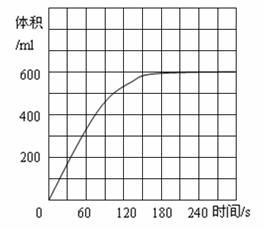 化分解50 ml3.0%的双氧水时收集到的同温同
化分解50 ml3.0%的双氧水时收集到的同温同
压下O2体积对反应时间示意图,并作必要的
标注;
讨论:有关FeCl3参加的可逆反应的两个问题:
(6)分别取若干毫升稀FeCl3溶液与稀KSCN
溶液,混合,溶液呈血红色。限用FeCl3、KSCN、
KCl三种试剂,仪器不限,为证明FeCl3溶液与
KSCN溶液的反应是一个可逆反应,至少还要进行
次实验;
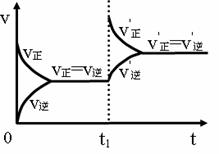 (7)一定浓度的FeCl3与KSCN两溶液反应达到
(7)一定浓度的FeCl3与KSCN两溶液反应达到
平衡,在t1时刻加入一些FeCl3固体,反应重新达
到平衡。若其反应过程可用如下的速率v-时间t
图像表示。请根据此图像和平衡移动规律求证新平衡下FeCl3的浓度比原平衡大
。
19.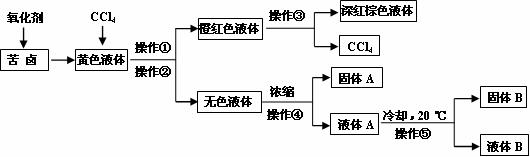 (11分)广东海岸线漫长,海洋盐矿资源丰富。有一研究性学习小组拟取某盐场制盐后的苦卤浓缩液(富含Mg2+、Br-、SO42-、Cl-等)制取较纯净的氯化镁晶体及液溴(Br2),他们设计了如下流程:
(11分)广东海岸线漫长,海洋盐矿资源丰富。有一研究性学习小组拟取某盐场制盐后的苦卤浓缩液(富含Mg2+、Br-、SO42-、Cl-等)制取较纯净的氯化镁晶体及液溴(Br2),他们设计了如下流程:
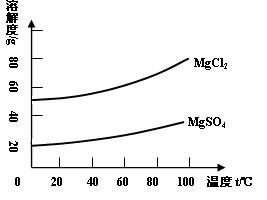
请根据以上流程和右图溶解度曲线,
回答相关问题:
(1)操作①的名称是 ,
操作②名称是 ,操作③的
名称是 ,操作④的名称
是 ;
(2)氯化镁晶体是固体
(选填 “A”或“B”);
(3)在对无色液体浓缩之后,进行操作④之前,往往先向浓缩液中加入少量水,目的是 ;
(4)若用化学方法对上述操作②后无色溶液进行除杂提纯,则需要用到的试剂是(填序号) ;
A.BaCl2 B.NaOH C.Na2CO3 D.HCl
(5)该研究性学习小组发现,冬天时该盐场制盐后的苦卤浓缩液会自行析出晶体,经分析该晶体是MgCl2,几乎不含其他盐类,原因是 。
17.某元素X的相对原子质量为a,它的含氧酸化学式为HmXOn(m>1)。下列有关说法中一定正确的是
A.HmXOn 水溶液中n(H+):n(XOnm-) = m:1
B.500 mL 2 mol·L-1的HmXOn溶液中溶质的质量是(m+a+16n) g
C.1 L 0.1 mol·L-1的HmXOn溶液正好中和0.1 mol的KOH
D.若0.1 mol·L-1的HmXOn溶液的pH = 1,则0.1 mol·L-1KmXOn溶液的pH > 7
18.常温下,下列各溶液的叙述中正确的是
A.0.1 mol/L的醋酸钠溶液20 mL与0.1 mol/L盐酸10 mL混合后溶液显酸性,则
c (CH3COO-)>c (Cl-)>c (H+)>c (CH3COOH)
B.pH=7的醋酸钠和醋酸混合液中:c(Na+)=c(CH3COO-)
C.0.1 mol/L的醋酸的pH=a,0.01 mol/L的醋酸的pH=b,则a+1>b
D.已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,
[c(Na+)-c(F-)]< [c(K+)-c(CH3COO-)]
16.对数据的分析归纳可得到科学的结论和规律。下列为某同学对数据的利用情况,其中不正确的是
A.根据非金属单质与氢气化合生成1 mol产物时反应热的大小推测生成物的稳定性
B.用沸点数据推测用蒸馏法分离两种液体混合物的可能性
C.用熔点数据分析不同分子的稳定性
D.用同周期元素的原子(离子)半径数据推断某些原子(离子)氧化性或还原性的相对强弱
15. 某有机物的分子结构如图(图中棍表示单键、双键或叁键),它属烃或烃的含氧衍生物。关于该有机物的叙述正确的是
某有机物的分子结构如图(图中棍表示单键、双键或叁键),它属烃或烃的含氧衍生物。关于该有机物的叙述正确的是
A.该有机物的化学式为C4H8O2
B.该有机物可使溴水褪色,也可与NaOH溶液反应
C.该有机物可发生取代反应和加成反应
D.该有机物是乙酸的同系物
14.向一容积为5L的恒容密闭容器中充入5molA与8molB,在一定条件下反应:
 2A(g) + 3B(g) xC(g) + yD(g) (x、y为正整数),反应进行2min后达到平衡,这2min内平均反应速率v(C)=0.3mol/(L·min),D的平衡浓度为0.3mol/L,又知v(B) : v(C)=3
: 2,则下列说法中正确的是
2A(g) + 3B(g) xC(g) + yD(g) (x、y为正整数),反应进行2min后达到平衡,这2min内平均反应速率v(C)=0.3mol/(L·min),D的平衡浓度为0.3mol/L,又知v(B) : v(C)=3
: 2,则下列说法中正确的是
A.x : y=2 : 1 B.v(A) : v(C)=2 : 1
C.A的平衡浓度为0.4mol/L D.A与B的平衡浓度之比为3 : 2
13.据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学方程式为:5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是
A.上述反应是放热反应
B.产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾)
C.因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替
D.上述反应中消耗3molP时,转移电子的物质的量为15mol
12.下列物质的性质比较,正确的是
A.酸性:H2SO4>HClO4>HBrO4 B.碱性:NaOH>KOH>RbOH
C.非金属性: P>S>Cl D.气态氢化物稳定性:HF>HCl>H2S
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com