
题目列表(包括答案和解析)
19、(12分)氯普鲁卡因盐酸盐是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,以甲苯为初始原料的合成氯普鲁卡因盐酸盐的路线如下:
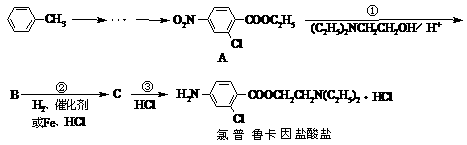
回答下列问题:
⑴ 当原料的核磁共振氢谱有 个峰时,可以判断原料是纯净的。
 ⑵ B的结构简式是 ,反应②的类型是 。
⑵ B的结构简式是 ,反应②的类型是 。
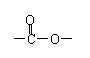
⑶ A的同分异构体中,含有-NO2、-Cl、酯基( ),且为1,3,5-三取代苯结构的有6种,其中4种结构如下:
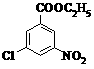
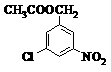
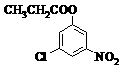
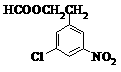
请写出另外两种同分异构体的结构简式: ▲ 。
⑷ 已知:
①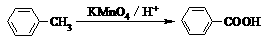
② 当苯环上已有一个“-CH3”或“-Cl”时,新引入的取代基一般在原有取代基的邻位或对位;当苯环上已有一个“-NO2”或“-COOH”时,新引入的取代基一般在原有取代基的间位。
请用合成反应流程图表示出由甲苯和其他物质合成A的最佳方案,请在答题纸的方框中表示。
合成反应流程图表示方法示例如下:

18、(10分)合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料。从天然气获得合成气过程中可能发生的反应有:
① CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
② CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH2=+247.3 kJ/mol
2CO(g)+2H2(g) ΔH2=+247.3 kJ/mol
 ③ CO(g)+H2O(g)
③ CO(g)+H2O(g) CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
请回答下列问题:
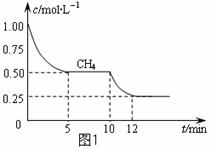
⑴ 在一密闭容器中进行反应①,测得CH4的物质的
量浓度随反应时间的变化如图1所示。反应进行的
前5 min内, v(H2)= ;10 min时,改变的
外界条件可能是 。
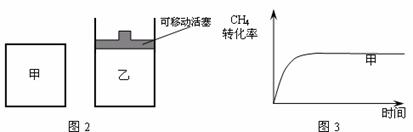
⑵ 如图2所示,在甲、乙两容器中分别充入等物质
的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间变化的图像如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像。
⑶ 反应③中ΔH3= 。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
|
CO |
H2O |
CO2 |
H2 |
|
0.5
mol |
8.5
mol |
2.0
mol |
2.0
mol |
此时反应③中正、逆反应速率的关系式是 (填代号)。
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
17、(12分)铬(Cr)属于重金属元素,含铬废水和废渣排放必须经过处理达到有关的安全标准。
(1)铬原子核中质子数为24,铬位于周期表中第_______周期_______族。
|
|
 Cr(OH)3
Cr(OH)3 CrO2-
CrO2-
① FeSO4还原Cr2O72-的离子方程式为_____________________________________。
② Cr2 (SO4) 3溶液中加入过量NaOH浓溶液,反应的离子方程式为_____________。
③ 沉淀法分离废水中的Cr3+离子,pH应控制在 范围内。
④ 下列关于铬及其化合物的说法中正确的是 。
A.K2Cr2O7是一种常用的强氧化剂 B.NaCrO2溶液与AlCl3溶液混合有沉淀生成
C.酸性K2Cr2O7溶液可用于检验司机是否酒后驾车
D.金属铬硬度大、耐腐蚀,是常用的镀层金属
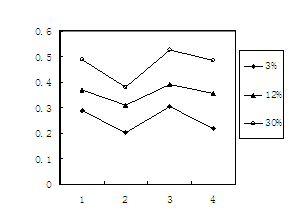 (3)铬冶炼工业的废渣粉碎后掺入煤矸石经过高温处理可以制砖,为了探究其中的铬元素在使用过程中是否会重新污染环境,研究组在一定条件下浸溶砖样,检测浸出液中Cr元素浓度,结果如图:
(3)铬冶炼工业的废渣粉碎后掺入煤矸石经过高温处理可以制砖,为了探究其中的铬元素在使用过程中是否会重新污染环境,研究组在一定条件下浸溶砖样,检测浸出液中Cr元素浓度,结果如图:
说明:1--用蒸馏水浸溶,2--用稀硫酸浸溶,3--冻融后用蒸馏水浸溶,4--曝晒后用蒸馏水浸溶;
3%等--制砖时含铬废渣掺入的比例。
已知我国规定“固体废弃物浸出标准值含铬不得超过10 mg·L-1”。分析图表,可得出多个结论:
① 实验取用的砖样是否符合上述标准: 。
② 还能得出的其它结论是(写出2条即可)
______________________________________________________________________;
______________________________________________________________________。
16.(8分)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
 ⑴冶炼铜的反应为:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
⑴冶炼铜的反应为:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
⑵上述冶炼过程产生大量SO2。下列处理方案中合理的是 (填代号)。
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO4 d.用浓硫酸吸收
⑶过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:
S2O82-+2I-=2SO42-+I2
通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应催化的过程。
、 (不必配平)
⑷利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
a.除去Al3+的离子方程式是 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 。
证明炉渣中含有FeO的实验现象为 。
15.(10分)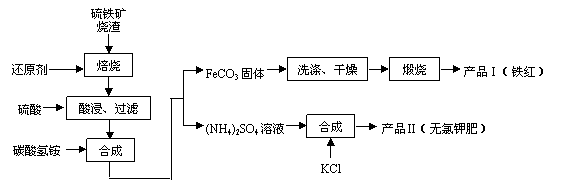 硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用硫铁矿烧渣制备铁红等产品的实验流程如下:
硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用硫铁矿烧渣制备铁红等产品的实验流程如下:
已知几种盐的溶解度随温度变化的曲线如下图所示:
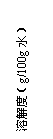
回答下列问题:
(1)酸浸、过滤后滤液中的金属阳离子是________________。
(2)煅烧FeCO3生成产品I的化学反应方程式为________________________________。实验室进行煅烧操作所需仪器除了酒精灯、泥三角、三脚架、玻璃棒外,还有__________。
(3)产品Ⅱ的化学式为_______________,为了获得产品Ⅱ,向(NH4)2SO4溶液中加入KCl溶液后,还需要进行的操作是: 、趁热过滤、 、干燥。
(4)检验产品II中是否含有氯化物杂质的实验操作是:取少量产品Ⅱ于试管中配成溶液, 。
14、对于平衡体系 A(g)+
A(g)+ 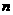 B(g)=
B(g)=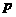 C(g)+
C(g)+ 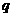 D(g);ΔH<0。下列结论中不正确的是
D(g);ΔH<0。下列结论中不正确的是
A. 若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则
 +
+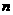 <
<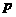 +
+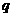
B.
若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为 ∶
∶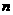
C.
若 +
+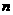 =
=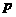 +
+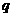 ,则往含有
,则往含有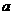 mol气体的平衡体系中再加入
mol气体的平衡体系中再加入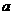 mol的B,达到新平衡时,
mol的B,达到新平衡时,
气体的总物质的量等于2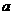
D.若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小
第II卷 非选择题(共72分)
13、下列反应的离子方程式书写正确的是
A.过量的铁与浓硝酸反应: Fe + 6H++ 3NO3- = Fe3+ 十3NO2↑+ 3H2O
B. 次氯酸钙溶液中通入过量CO2 : ClO-+CO2 + H2O= HClO+ HCO3-
C. 1mol·L-1 的 NaAlO2 溶液和2.5mol· L-1 的盐酸等体积混合:
2AlO2- + 5 H+= Al(OH)3 ↓+ Al3+ + H2 O
D.在碳酸氢镁溶液中加入足量Ca(OH)2 溶液:
Mg2+ +2HCO3-+Ca2+ +2OH-= MgCO3↓ + CaCO3↓ + 2H2O
12、天然油脂结构的核心为甘油(HOCH2CH(OH)CH2OH),有一瘦身用的非天然油脂,其结构的核心则为蔗糖(C12H22O11)。该非天然油脂可由直链型的不饱和油酸(C17H33COOH)与蔗糖反应而得,其反应示意图如下图所示(注意:图中的反应式不完整)
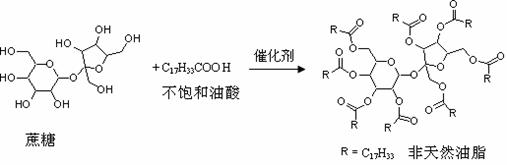
下列说法正确的是
A.蔗糖酯也是高级脂肪酸的甘油酯,属于油脂类物质
B.该非天然油脂与氢氧化钠溶液共热,其水解产物可与溴水反应
C.非天然油脂为高分子化合物
D.该蔗糖酯在稀硫酸的作用下水解,最终可生成三种有机化合物
11、下列各图均为检查装置气密性的方法,根据实验现象判断,其中漏气的是
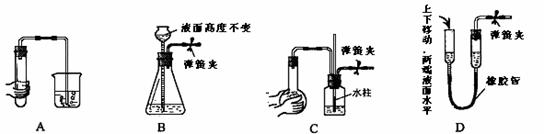
10、有人认为CH2 = CH2与Br2的加成反应,实质是Br2先断裂为Br+和Br-,然后Br+首先与CH2 = CH2一端碳原子结合,第二步才是Br-与另一端碳原子结合。根据该观点如果让CH2 = CH2与Br2在盛有NaCl和NaI的水溶液中反应,则得到的有机物不可能是
A.ClCH2CH2Cl B.BrCH2CH2Br C.BrCH2CH2I D.BrCH2CH2Cl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com