
题目列表(包括答案和解析)
13. pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为:1×10-3mol/L,则该溶液 中该溶质的pC=-lg1×10-3=3。
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为:1×10-3mol/L,则该溶液 中该溶质的pC=-lg1×10-3=3。
 右图为H2CO3溶液的pC-pH图,在 pH=4时,溶液中主要存在的离子有:
右图为H2CO3溶液的pC-pH图,在 pH=4时,溶液中主要存在的离子有:

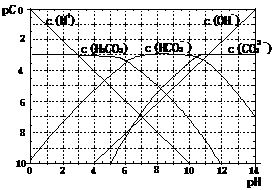
 A.H+、HCO3- 、CO32-
A.H+、HCO3- 、CO32-
 B.H+、CO32-
B.H+、CO32-
 C.H+、HCO3-
C.H+、HCO3-
 D.CO32-、HCO3-
D.CO32-、HCO3-

12. 下列反应离子方程式正确的是
下列反应离子方程式正确的是
 A. 氧化铁溶于氢碘酸:Fe2O3+6H+ = 2Fe3++3H2O
A. 氧化铁溶于氢碘酸:Fe2O3+6H+ = 2Fe3++3H2O
 B. 等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+ Ba2++OH-
= BaCO3↓ + H2O
B. 等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+ Ba2++OH-
= BaCO3↓ + H2O
 C. NaHSO3溶液显酸性的原因是:HSO3- = SO32-
+ H+
C. NaHSO3溶液显酸性的原因是:HSO3- = SO32-
+ H+
 D. AgNO3溶液中加入过量氨水:Ag++NH3·H2O=AgOH↓+NH4+
D. AgNO3溶液中加入过量氨水:Ag++NH3·H2O=AgOH↓+NH4+
11. 根据元素周期表知识,下列说法不正确的是
根据元素周期表知识,下列说法不正确的是
 A.最外层电子数为3-7的原子一定是主族元素的原子
A.最外层电子数为3-7的原子一定是主族元素的原子
 B.短周期元素X、Y,若X、Y的最外层电子数相同,且X原子半径小于Y,当X (OH)n为强碱时,Y(OH)n必为强碱
B.短周期元素X、Y,若X、Y的最外层电子数相同,且X原子半径小于Y,当X (OH)n为强碱时,Y(OH)n必为强碱
 C.短周期元素A、B,若A、B电子层数相同,且A原子半径小于B,当HnAOm为强酸时,B必为活泼非金属元素
C.短周期元素A、B,若A、B电子层数相同,且A原子半径小于B,当HnAOm为强酸时,B必为活泼非金属元素
 D.2007年3月21日,中国科学技术名词审定委员会公布了111号元素Rg的中文名称,111号元素属于过渡元素
D.2007年3月21日,中国科学技术名词审定委员会公布了111号元素Rg的中文名称,111号元素属于过渡元素
10.
 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为
 3Zn + 2K2FeO4 + 8H2O
3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn + 2K2FeO4 + 8H2O
3Zn(OH)2 + 2Fe(OH)3 + 4KOH
 下列叙述错误的是
下列叙述错误的是
 A.放电时负极反应为:Zn ―
2e-+ 2OH-= Zn(OH)2
A.放电时负极反应为:Zn ―
2e-+ 2OH-= Zn(OH)2
 B.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
B.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
 C.充电时阳极反应为:Fe(OH)3 ― 3e- + 5 OH- =
FeO
C.充电时阳极反应为:Fe(OH)3 ― 3e- + 5 OH- =
FeO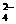 + 4H2O
+ 4H2O
 D.充电时阴极附近溶液的碱性减弱
D.充电时阴极附近溶液的碱性减弱
8.
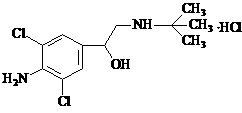 今年2月18日,广州市再度出现瘦肉精中毒事件,70余人住院治疗。原因是食用“瘦肉精”喂养的猪肉而中毒,己知瘦肉精的结构如右图,则它可能发生的化学反应有:①
酯化反应 ②
取代反应
今年2月18日,广州市再度出现瘦肉精中毒事件,70余人住院治疗。原因是食用“瘦肉精”喂养的猪肉而中毒,己知瘦肉精的结构如右图,则它可能发生的化学反应有:①
酯化反应 ②
取代反应
 ③ 氧化反应 ④加成反应
③ 氧化反应 ④加成反应
 A.②④
B.②③
A.②④
B.②③
 C.①②③
D.①②③④
C.①②③
D.①②③④
 9.生活中遇到的某些问题,常常涉及到化学知识,下列说法错误的是
9.生活中遇到的某些问题,常常涉及到化学知识,下列说法错误的是
 A.硅酸钠是最简单的硅酸盐,是制备硅胶和木材防火剂等的原料
A.硅酸钠是最简单的硅酸盐,是制备硅胶和木材防火剂等的原料
 B.铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝
B.铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝
 C.黄铜(铜锌合金)制作的铜锣不易产生铜绿
C.黄铜(铜锌合金)制作的铜锣不易产生铜绿
 D.含氯的漂白液可通过电解饱和食盐水获得
D.含氯的漂白液可通过电解饱和食盐水获得
7. 某合作学习小组讨论辨析:①漂白粉和酸雨都是混合物 ②煤和石油都是可再生能源 ③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 ④不锈钢和目前流通的硬币都是合金 ⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 ⑥豆浆和雾都是胶体。 上述说法正确的是
某合作学习小组讨论辨析:①漂白粉和酸雨都是混合物 ②煤和石油都是可再生能源 ③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 ④不锈钢和目前流通的硬币都是合金 ⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 ⑥豆浆和雾都是胶体。 上述说法正确的是
 A.①②④ B.①⑤⑥
C.①③④⑥
D.②③④⑤
A.①②④ B.①⑤⑥
C.①③④⑥
D.②③④⑤
6.设NA为阿伏加德罗常数,下列叙述中错误的是
 A. 0.1 mol Na2O2与水反应时,转移的电子数为0.1 NA
A. 0.1 mol Na2O2与水反应时,转移的电子数为0.1 NA
 B. 在含4molSi-O键的石英晶体中,氧原子的数目为2NA
B. 在含4molSi-O键的石英晶体中,氧原子的数目为2NA
 C. 28g乙烯和28g丙烯中均含有6NA对共用电子对
C. 28g乙烯和28g丙烯中均含有6NA对共用电子对
 D. 含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2︰3
D. 含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2︰3

5. 下述实验不能达到预期实验目的的是
下述实验不能达到预期实验目的的是
|
序号 |
实验内容 |
实验目的 |
|
A |
将2.5g CuSO4·5H2O溶解在97.5g 水中 |
配制质量分数为1.6%的CuSO4溶液 |
|
B |
向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 |
说明一种沉淀能转化为另一种溶解度更小的沉淀 |
|
C |
室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH |
比较HClO和CH3COOH的酸性强弱 |
|
D |
室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 |
研究浓度对反应速率的影响 |
4.一定条件下,在容积为10L的密闭容器中,1molX和1molY进行如下反应:
 2X(g)+Y(g)
Z(g)
2X(g)+Y(g)
Z(g)
经60s达到平衡,生成0.3molZ,下列说法正确的是
A.以X浓度变化表示的反应速率为0.001mol/(L·s)
B.将容器容积变为20L,Z的平衡浓度为原来的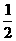
C.若增大压强,则正反应速率增大,逆反应速率减小
D.若升高温度,X的体积分数增大,则该反应的△H>0
3.中科大陈乾旺教授等人发明RTX-r合成金刚石的新方法,化学原理为:
① Na+CO2  C(金刚石)+C(石墨)+Na2CO3(未配平);
C(金刚石)+C(石墨)+Na2CO3(未配平);
该方法比1955年人工首次制得金刚石的旧方法容易得多,其化学原理是:
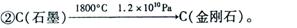
以下表述中正确的是
A.反应①中既有旧化学键的断裂又有新化学键的形成
B.新方法利用的是化学变化,旧方法利用的是物理变化
C.在反应①中每生成12g金刚石需要消耗23g金属钠
D.反应①和反应②中所得的金刚石都是还原产物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com